
����Ŀ����2.3g Na��2.7g Alͬʱ���뵽������ˮ�г�ַ�Ӧ������Ӧ�����Һϡ�͡�����Ϊ500mL������˵����ȷ����
A.������Ӧ�����й�ת�Ƶ���0.4 mol
B.��Ӧ�����������ڱ�״���µ������1.12L
C.��Ӧ������Һ������CO2��Ӧ�����ӷ���ʽ��2AlO2����CO2��3H2O=2Al��OH��3����CO32��
D.��ϡ�͡����ݲ������õ���ȫ���������У��ձ�����������500mL����ƿ
���𰸡�A
��������
�ù����з����ķ�Ӧ��2Na��2H2O=2NaOH��H2����2Al��2NaOH��2H2O=2NaAlO2��3H2����2.3g�����ƣ�Na�����ʵ���Ϊ2.3g��23g/mol=0.1mol��������0.1molNaOH��2.7g��������Al�����ʵ���Ϊ2.7g��27g/mol=0.1mol����0.1molNaOHǡ����ȫ��Ӧ����0.1molNaAlO2��
A.������Ӧ�����е���ת�Ƶ����ʵ���Ϊ0.1mol��1��0.1mol��3=0.4mol��A��ȷ��
B.�������������ʵ���Ϊ![]() mol��
mol��![]() ��0.1mol=0.2mol����״�������Ϊ0.2mol��22.4L/mol=4.48L��B����
��0.1mol=0.2mol����״�������Ϊ0.2mol��22.4L/mol=4.48L��B����
C.NaAlO2��Һ��ͨ��������CO2����Ӧ�����ӷ���ʽΪAlO2-+CO2+2H2O=Al��OH��3��+HCO3-��C����
D����ϡ�͡����ݲ������õ���ȫ�����������У��ձ�����������500mL����ƿ����ͷ�ιܣ�D����
��ѡA��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ķ����в��ϣ��������С�⡣
����Kolbe's��ⷨ��ȡ��Ȳ�ķ�Ӧԭ��Ϊ�� +2H2O
+2H2O 2CO2��+C2H2��+H2��+2KOH
2CO2��+C2H2��+H2��+2KOH
��1�����б�ʾ��Ӧ��������Ļ�ѧ���������ǣ� ��
A.������Ϊ20�ļ�ԭ�ӣ�![]() K
K
B.K+�Ľṹʾ��ͼ��
C.CO2�ĵ���ʽ��![]()
D.C2H2�Ľṹʽ��H��C![]() C��H
C��H
��2���йظ÷�Ӧ������˵����ȷ���ǣ� ��
A.��ѧ��ת��Ϊ����
B.������������Ǩ�Ƶ���Ҫ��H+
C.����������ҺpH���ϼ�С
D.�����ĵ缫��ӦʽΪ2H2O+2e-=2OH-+H2��
��3��������������У���ˮ��Һ������ɵ�����Ҫ��CH2=CH2���ǣ� ��
A.CH3COOKB.CH3CH2COOKC.CH2=CHCOOKD.KOOCCH2CH2COOK
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Fe2����I����Br������Һ��ͨ��������������Һ�����������ӵ����ʵ����������������ʵ����ı仯����ͼ��ʾ������˵������ȷ����(����)
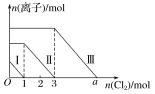
A.�߶�������Fe2���ı仯���
B.�߶�������Br���ı仯���
C.aֵ����6
D.ԭ�����Һ��n(FeBr2)��4mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪0.1 mol��L��1�Ĵ�����Һ�д��ڵ���ƽ�⣺CH3COOH![]() CH3COO����H����Ҫʹ��Һ��c(H��)/c(CH3COOH)ֵ�����Բ�ȡ�Ĵ�ʩ��( )
CH3COO����H����Ҫʹ��Һ��c(H��)/c(CH3COOH)ֵ�����Բ�ȡ�Ĵ�ʩ��( )
���������ռ���� �������¶� �������������� ����ˮ
A.�٢�B.�ڢ�C.�ۢ�D.�ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڻ�ѧ��Ӧ�ķ�������˵���������(����)
A.���¶ȡ�ѹǿһ���������£����������ع�ͬ����һ����ѧ��Ӧ�ķ���
B.�¶ȡ�ѹǿһ��ʱ�����ȵ������ӷ�Ӧ һ�����Է�����
C.��Ӧ![]() ��H < 0�����������ڷ�Ӧ�Է�����
��H < 0�����������ڷ�Ӧ�Է�����
D.�����ܽ�������ʱ��й�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����1.0Lcmol/LCH3COOH��Һ��0.1molNaOH�����ϣ�ʹ֮��ַ�Ӧ��Ȼ����û����Һ�м���CH3COOH ��CH3COONa����(����������¶ȱ仯)��������ҺpH�ı仯��ͼ��ʾ�����������������

A. ���¶��£�����ĵ���ƽ�ⳣ��Ka=![]()
B. a���Ӧ�Ļ����Һ��c(CH3COOH)>c(Na+)>c(OH-)
C. ˮ�ĵ���̶�:c>b>a
D. �������Һ������ʱ��c(Na+)=c(CH3COO-)>c(H+)=c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͬ��ͬѹ�£�m g�������2m g��������ռ���֮��Ϊ1��2�����ݰ����ӵ������жϣ�������������ȷ����(����)
A. �����ҵ���Է�������֮��Ϊ1��1
B. ͬ��ͬѹ�£����ҵ��ܶ�֮����1��1
C. ͬ��ͬ����£��������ļ��ҵ�ѹǿ֮����1��1
D. �������ļ����е�ԭ����֮����1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����4L�ܱ������г���6molA�����5molB���壬��һ�������·�����Ӧ��![]() ���ﵽƽ��ʱ��������2molC�����ⶨD��Ũ��Ϊ0.5mol/L�������ж���ȷ���� �� ��
���ﵽƽ��ʱ��������2molC�����ⶨD��Ũ��Ϊ0.5mol/L�������ж���ȷ���� �� ��
A.x=1
B.B��ת����Ϊ20%
C.�ﵽƽ��ʱ������ͬ�¶��������ڻ�������ѹǿ�Ƿ�Ӧǰ��85%
D.ƽ��ʱA��Ũ��Ϊ0.75mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʳ����һ�����������������е�����֮һ����ʳ��Ϊԭ�Ͽ�����ȡ�����ơ��������������ռ�ȱ���Ļ�ѧ��Ʒ�ͻ���ԭ�ϡ�
��1��д����ҵ�Ʊ������ƵĻ�ѧ����ʽ��________��
��2�����________���Ƶ��ռ���������������Ϊ________��ҵ��д���ù�ҵ�еĵ缫��Ӧʽ���ܷ�Ӧʽ������_________������________���ܷ�Ӧʽ________��
��3���ҹ������Ļ���ר�Һ�°������������Ƽ�����Ҳ��ʳ��Ϊ����ԭ�ϣ��÷���Ϊ����ʳ��ˮ��ͨ��![]() ����ͨ��
����ͨ��![]() ���壬����
���壬����![]() ���壬��ѧ����ʽΪ________����������
���壬��ѧ����ʽΪ________����������![]() �������ռ��ô����ѧ����ʽΪ___________��
�������ռ��ô����ѧ����ʽΪ___________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com