
| A.利用太阳能等清洁能源代替化石燃料,有利于节约资源.保护环境 |
| B.凡含有食品添加剂的食物对人体健康均有害,不可食用 |
| C.为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术 |
| D.几千万年前地球上一条恐龙体内的某个原子可能在你的身体里 |
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| A.H2O | B.稀H2SO4 |
| C.98.3%H2SO4 | D.NH3·H2O溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

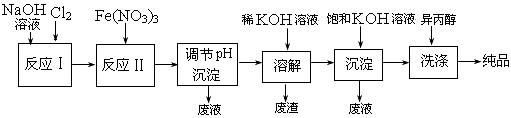
| 湿法 | 强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液 |
| 干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物 |
 :
:
|
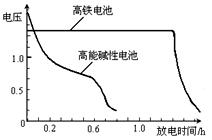
 ,上图为该电池和常用的高能碱性电池的放电曲线,由此可得出的高铁电池的优点有 ▲ 、 ▲ 。
,上图为该电池和常用的高能碱性电池的放电曲线,由此可得出的高铁电池的优点有 ▲ 、 ▲ 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.石油属于可再生矿物能源 | B.石油主要含有碳、氢两种元素 |
| C.石油的裂化属于物理变化 | D.裂化汽油不能使溴水褪色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
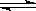 2NH3(g);已知:反应2min达到平衡,此时N2的浓度减少了2/3。
2NH3(g);已知:反应2min达到平衡,此时N2的浓度减少了2/3。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.乙醇和汽油都是可再生资源,应大力推广“乙醇汽油” |
| B.可以用聚乙烯塑料作食品包装袋 |
| C.食品加工、消毒防腐常使用福尔马林 |
| D.钢铁在海水中比在河水中更易腐蚀,主要原因是海水含氧量高于河水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

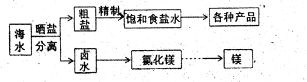
 镁制取镁的化学方程式
镁制取镁的化学方程式 : 。
: 。 。
。 2+、
2+、 Mg
Mg 2+、SO
2+、SO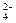 ,加入试剂的合理顺序为
,加入试剂的合理顺序为  (选填a,b,c)
(选填a,b,c) ,再加Na2CO3
,再加Na2CO3查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com