
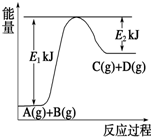
 Ⅰ.已知某反应A(g)+B(g)?C(g)+D(g),过程中的能量变化如图所示,回答下列问题.
Ⅰ.已知某反应A(g)+B(g)?C(g)+D(g),过程中的能量变化如图所示,回答下列问题.

 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案科目:高中化学 来源: 题型:
 已知某反应A(g)+B(g)?C(g)+D(g) 过程中的能量变化如图所示,回答下列问题.
已知某反应A(g)+B(g)?C(g)+D(g) 过程中的能量变化如图所示,回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
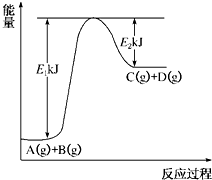 已知某反应A(g)+B(g)?C(g)+D(g)进行过程中的能量变化如图所示,请回答下列问题:
已知某反应A(g)+B(g)?C(g)+D(g)进行过程中的能量变化如图所示,请回答下列问题:| A | B | C | D | |
| 甲 | a mol | a mol | 0 | 0 |
| 乙 | 2a mol | a mol | 0 | 0 |
| 丙 | a mol | a mol | a mol | a mol |
| 丁 | a mol | 0 | a mol | a mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某可逆反应A(g)+B(g)![]() C(g)在密闭容器中进行。A的含量和温度
C(g)在密闭容器中进行。A的含量和温度
的关系如图所示,则下列结论正确的是( )

A.T1<T2,正反应是吸热反应 B.T1>T2,正反应是吸热反应
C.T1>T2,正反应是放热反应 D.T1<T2,正反应是放热反应
查看答案和解析>>
科目:高中化学 来源:2013届江西省高二上学期期末联考化学试卷 题型:填空题
(8分) 已知某反应A(g)+B(g)⇌C(g)+D(g)进行过程中的能量变化如图所示,请回答下列问题:

(1)该反应的ΔH=________kJ·mol-1(用含E1、E2的代数式表示)。(1分)
(2)若在反应体系中加入催化剂使逆反应速率增大,则E1________(填“增大”、“减小”或“不变”,下同),ΔH________。(2分)
(3)在相同温度和压强下,对反应A(g)+B(g)??C(g)+D(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表:
|
|
A |
B |
C |
D |
|
甲 |
a mol |
a mol |
0 |
0 |
|
乙 |
2a mol |
a mol |
0 |
0 |
|
丙 |
a mol |
a mol |
a mol |
a mol |
|
丁 |
a mol |
0 |
a mol |
a mol |
上述四种情况达到平衡后,C(D)的大小顺序是________。(2分)
A.乙=丁>丙=甲 B.乙>丁>甲>丙 C.丁>乙>丙=甲 D.丁>丙>乙>甲
(4)若上述反应达到平衡,为了提高A的转化率,可以采用的措施有(写一条):________________________________________________________________________。(1分)
(5)在恒温恒容条件下进行上述反应。下列情况可以判断该反应达到平衡状态的是____(2分)
A.气体平均摩尔质量不再变化 B. 气体压强不再变化
C. 气体密度不再变化 D. 消耗A的速率等于消耗D的速率
E. 各组分浓度之比为1:1:1:1 F. C生成的速率等于B消耗的速率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com