
| A.NaCl溶液能导电,所以NaCl溶液是电解质 |
| B.若某种电解质溶液中含有未电离的分子,则该电解质一定是弱电解质 |
| C.氯气和氨气的水溶液导电性都很好,所以它们是电解质 |
| D.CaCO3在水中溶解度很小,但溶解的 CaCO3全部电离,所以 CaCO3是强电解质 |
科目:高中化学 来源:不详 题型:单选题
| A.甲基橙的变色PH范围在4.4~6.2之间。 |
| B.保护海轮外壳以及石油管道通常是用牺牲阳极的阴极保护法。 |
| C.电离常数可以表示弱酸的相对强弱,电离常数越小,弱酸的酸性越强。 |
| D.弱电解质的电离是一个放热过程。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
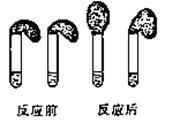
 l溶液各100mL;
l溶液各100mL;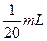 )分别稀释至100mL,
)分别稀释至100mL, ·L-1H2SO4 D.2mol·L-1HA
·L-1H2SO4 D.2mol·L-1HA ,其pH与溶液体积V的关系如右图所示,则下列说法不正确的有
,其pH与溶液体积V的关系如右图所示,则下列说法不正确的有 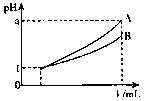
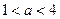 ,则A、B都是弱酸
,则A、B都是弱酸查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
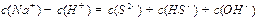
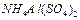 、②
、②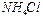 、③
、③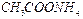 、
、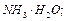
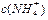 由大到小的顺序是:①>②>③>④
由大到小的顺序是:①>②>③>④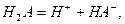
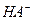

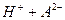 则在NaHA溶液中:
则在NaHA溶液中: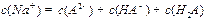
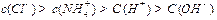
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com