
【题目】一定温度下,在容积不变的密闭容器中,反应I2(g) + H2(g)![]() 2HI(g)达到平衡的标志是( )
2HI(g)达到平衡的标志是( )
A.v正(I2)=2v逆(HI)
B.容器中气体的压强不再改变,气体的密度和摩尔质量不再改变
C.I2、H2、HI的分子数之比为1∶1∶2;
D.容器内气体的颜色不再发生改变
科目:高中化学 来源: 题型:
【题目】在一个1L的密闭容器中加2molA和1molB发生反应: 2A(g)+B(g)![]() 3C(g)+D(s),达到平衡时C的浓度为1.2mol/L , C的体积分数为a% 。维持容器的体积和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度仍是1.2mol/L,C的体积分数仍为a% 的是
3C(g)+D(s),达到平衡时C的浓度为1.2mol/L , C的体积分数为a% 。维持容器的体积和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度仍是1.2mol/L,C的体积分数仍为a% 的是
A. 6mol C+2mol D B. 4mol A+2mol B
C. 1mol A+0.5mol B+1.5mol C D. 3mol C+5mol D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化锂(LiH)在干燥的空气中能稳定存在,遇水或酸剧烈反应,能够引起燃烧。某化学科研小组准备使用下列装置制备LiH固体。下列说法正确的是
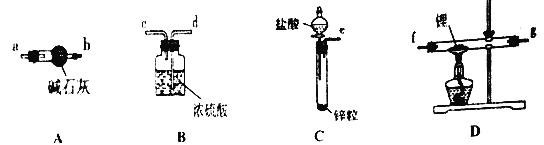
A. 上述仪器装置按气流从左到右连接顺序为:e接d,c接f,g接a,b(和g调换也可以)
B. 实验中所用的金属锂保存在煤油中
C. 在加热D处的石英管之前,应先通入一段时间氢气,排尽装置内的空气
D. 干燥管中的碱石灰可以用无水CaCl2代替
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物在科学研究和化工生产等领域都有着广泛的应用。请回答下列问题:
(1)与氮元素同族的第四周期元素的基态原子价层电子轨道表达式为___________。
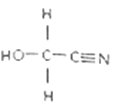
(2)HOCH2CN的结构简式如图,该分子中σ键与π键数目之比为___________,其分子中碳原子的杂化方式为___________,该物质中除氢以外的元素的第一电离能由大到小的顺序为______________________。
(3)[Cu(NH3)4]SO4是一种重要的配合物。与SO42-互为等电子体的分子的化学式为___________(任写一种)。NH3的 VSEPR模型为___________。[Cu(NH3)4]2+的结构可用示意图表示为______________________。
(4)①已知:2UO2+5NH4HF2![]() 2UF4·NH4F+3NH3↑+4H2O↑,NH4HF2中不含有的作用力为___________(填选项字母)。
2UF4·NH4F+3NH3↑+4H2O↑,NH4HF2中不含有的作用力为___________(填选项字母)。
A.共价键 B.配位键 C.金属键 D.离子键 E.氢键
②NH3和H2O的键角由大到小的顺序为______________________(用分子式表示),原因是_______________________________________________________。
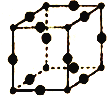
(5)Cu3N的晶胞结构如图所示,N3-的配位数为___________,Cu+半径为apm,N3-的半径为bpm,Cu3N晶胞的密度为___________g/cm3(列出计算式即可,阿伏加德罗常数的值用NA表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,其中甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O,下列说法正确的是
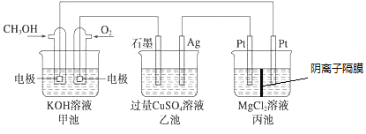
A. 甲池是电能转化为化学能的装置,乙、丙池是化学能转化电能的装置
B. 甲池通入CH3OH的电极反应式为CH3OH-6e-+2H2O=CO32-+8H+
C. 反应一段时间后,向乙池中加入一定量Cu(OH)2固体能使溶液恢复原浓度
D. 甲池中消耗4.48L(标准状况下)O2,此时丙池中理论上最多产生23.2 g固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固态或气态碘分别与氢气反应的热化学方程式如下:
① H2(g) +I2(?)![]() 2HI(g) △Hl=-9.48kJ/mol
2HI(g) △Hl=-9.48kJ/mol
②H2(g) +I2(?)![]() 2HI(g) △H2=+26.48kJ/mol
2HI(g) △H2=+26.48kJ/mol
下列判断不正确的是
A. ①中的I2为气态,②中的I2为固态
B. ②的反应物总能量比①的反应物总能量低
C. 反应①的产物比反应②的产物热稳定性更好
D. lmol固态碘升华时将吸热35.96kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在反应3Cl2+6KOH![]() KClO3+5KCl+3H2O中,下列说法正确的是 ( )
KClO3+5KCl+3H2O中,下列说法正确的是 ( )
A.Cl2是氧化剂,KOH是还原剂
B.KCl是氧化产物,KClO3是还原产物
C.被还原氯气与被氧化氯气的质量比为5:1
D.反应中转移电子的物质的量为6mol时,消耗3molCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用还原法可以将硝酸厂烟气中的大量氮氧化物(NOx),转化为无害物质。常温下,将NO与H2的混合气体通入Ce(SO4)2与Ce2(SO4)3的混合溶液中,其转化过程如下图所示。下列说法不正确的是
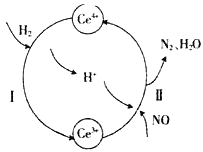
A. 反应I的离子反应方程式为2Ce4++H2=2Ce3++2H+
B. 反应II中氧化剂与还原剂的物质的量之比为1:2
C. 反应前溶液中c(Ce4+)一定等于反应后溶液中的c(Ce4+)
D. 反应过程中混合溶液内Ce3+和Ce4+离子的总数一定保持不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com