
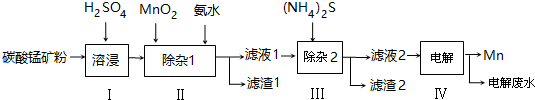
| ���� | Mn��OH��2 | Co��OH��2 | Ni��OH��2 | MnS | CoS | NiS |
| Ksp | 2.1��10-13 | 3.0��10-16 | 5.0��10-16 | 1.0��10-11 | 5.0��10-22 | 1.0��10-22 |
���� ��̼���̿���Ҫ�ɷ�ΪMnCO3�����������������ܵ�̼�������ʣ��м������ᣬ���Է�����Ӧ���������Σ������о�����������ԵĶ������̣����Խ�������������Ϊ�����ӣ�����pH���Խ�����������������������Һ�м�����泥����Խ������ӡ��������γ�����������������Եõ��ĺ��������ӵ��ε�⣬���Եõ������̣�
��� �⣺��̼���̿���Ҫ�ɷ�ΪMnCO3�����������������ܵ�̼�������ʣ��м������ᣬ���Է�����Ӧ���������Σ������о�����������ԵĶ������̣����Խ�������������Ϊ�����ӣ�����pH���Խ�����������������������Һ�м�����泥����Խ������ӡ��������γ�����������������Եõ��ĺ��������ӵ��ε�⣬���Եõ������̣�
��1����������Һ��Ļ��������¶ȡ�����Ũ�ȵȣ��ɼӿ췴Ӧ���ʣ�����Ϊ����߽�ȡ�ʿɲ�ȡ�Ĵ�ʩ�м��Ȼ�������������Ũ�ȵȣ�
�ʴ�Ϊ�������¶ȡ��ʵ���������Ũ�ȡ���С��ۿ���ֱ����
��2��������У�MnO2�����������¿ɽ�Fe2+��������ΪFe3+����Ӧ�����ӷ���ʽMnO2+2Fe2++4H+=Mn2++2Fe3++2H2O�����백ˮ����pHΪ5.0��6.0������Fe3++3NH3�qH2O=Fe��OH��3��+3NH4+���ɵõ�����Fe��OH��3��
�ʴ�Ϊ��Fe��OH��3��2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O��Fe3++3NH3�qH2O=Fe��OH��3��+3NH4+��
��3������Һ�е��������ģ�NH4��2S��Һ��Ŀ���dz�ȥCu2+��Zn2+������NH4��2S��Ũ�ȹ�����MnS��������ɲ�Ʒ��ʧ��
�ʴ�Ϊ������NH4��2S��Ũ�ȹ�����MnS��������ɲ�Ʒ��ʧ��
��4��CoS��NiS��Ksp�ֱ�Ϊ5.0��10-22��1.0��10-22������������NH4��2S��Һ������CoS��NiS��������Һ��c��Co2+����c��Ni2+��=5.0��10-22��1.0��10-22=5��1��
�ʴ�Ϊ��5��1��
��5������1ΪΪFe��OH��3������Ϊc kg����n��Fe3+��=n��Fe��OH��3��=$\frac{1000c}{107}$mol����2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O��֪n��MnO2��=$\frac{1}{2}$��$\frac{1000c}{107}$mol��
������Ϊa�K��̼���̿��������̴�����õ�����Mn b kg��n��Mn��=$\frac{1000b}{55}$mol��
��֪n��MnCO3��=$\frac{1000b}{55}$mol-$\frac{1}{2}$��$\frac{1000c}{107}$mol��
m��MnCO3��=��$\frac{1000b}{55}$mol-$\frac{1}{2}$��$\frac{1000c}{107}$mol����115g/mol��
��ԭ̼���̿���MnCO3����������Ϊ$\frac{��b-\frac{c}{107}��\frac{1}{2}��55����\frac{115}{55}}{a}$��100%��
�ʴ�Ϊ��$\frac{��b-\frac{c}{107}��\frac{1}{2}��55����\frac{115}{55}}{a}$��100%��
���� ���⿼�����Ʊ���������ƣ�Ϊ�߿��������ͣ���Ŀ�Ѷ��еȣ������Ʊ�������ȷ�Ʊ�ԭ��Ϊ���ؼ�������������ѧ���ķ�����������������ѧʵ��������


 Ӧ�����������Ĵ���ѧ������ϵ�д�
Ӧ�����������Ĵ���ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 ��֪A��B��C��D��E��F��G����Ԫ�أ����ǵ�ԭ��������������A������Ԫ����ԭ�Ӱ뾶��С��Bԭ�Ӻ��������6�ֲ�ͬ�˶�״̬��D��C��E�����ڣ�A��D��E����Ԫ�ص�ԭ������֮��Ϊ25��E2-��F+����ͬ�ĺ�������Ų���G����������25����ش��������⣺
��֪A��B��C��D��E��F��G����Ԫ�أ����ǵ�ԭ��������������A������Ԫ����ԭ�Ӱ뾶��С��Bԭ�Ӻ��������6�ֲ�ͬ�˶�״̬��D��C��E�����ڣ�A��D��E����Ԫ�ص�ԭ������֮��Ϊ25��E2-��F+����ͬ�ĺ�������Ų���G����������25����ش��������⣺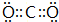 ��
��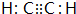 ����дһ�֣���
����дһ�֣����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
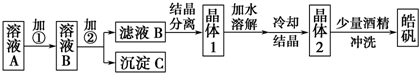
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ƿ������Ʊ�ľ�ķ���� | B�� | �赥�ʹ㷺���ڹ���ͨѶ | ||
| C�� | ������ɶ���������ˮ��Ӧ�Ƶ� | D�� | ˮ�������ǹ�������Ʒ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
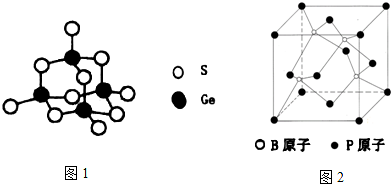
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
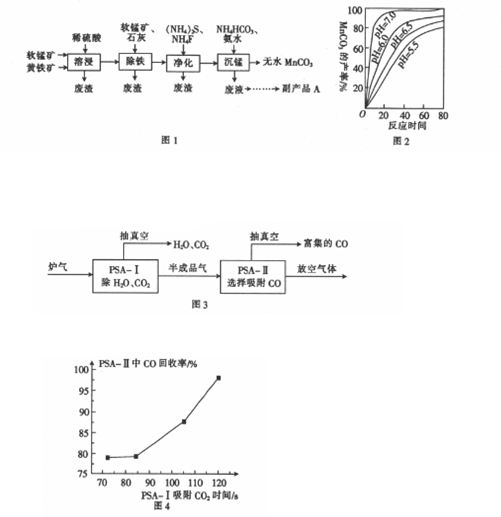
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ca��OH��2����ˮ������Ca��OH��2��������� | |
| B�� | ǿ�������Һ�ĵ����������ܱ����������Һ���������� | |
| C�� | Cu��NaCl��Һ���ǵ���ʣ������Ƿǵ���� | |
| D�� | SO3����ˮ�磬����SO3�ǵ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com