
【题目】已知Ksp(CaCO3)=2.8×10-9及表中有关信息:
弱酸 | CH3COOH | H2CO3 |
电离平衡常数(常温) | Ka=1.8×10-5 | Ka1=4.3×10-7; Ka2=5.6×10-11 |
下列判断正确的是
A. 向Na2CO3溶液中滴入酚酞,溶液变红,主要原因是CO32-+2H2O![]() H2CO3+2OH-
H2CO3+2OH-
B. 常温时,CH3COOH与CH3COONa混合溶液的pH=6,则c(CH3COOH)/c(CH3COO-)=18
C. NaHCO3溶液中:c(OH-)-c(H+)=c(H2CO3)-c(CO32-)
D. 2×10-4 mol/L的Na2CO3溶液与CaCl2溶液等体积混合出现沉淀,则CaCl2溶液的浓度一定是5.6×10-5 mol/L
【答案】C
【解析】
A. 向Na2CO3溶液中滴入酚酞,溶液变红,是因为碳酸根离子水解使溶液显碱性,离子方程式为:CO32-+H2O![]() HCO3-+OH-,故错误;B. 常温时,CH3COOH与CH3COONa混合溶液的pH=6,Ka=1.8×10-5,则有Ka=1.8×10-5=
HCO3-+OH-,故错误;B. 常温时,CH3COOH与CH3COONa混合溶液的pH=6,Ka=1.8×10-5,则有Ka=1.8×10-5= ![]() =
= ![]() ,则c(CH3COO-)/c(CH3COOH)=18,故错误;C. NaHCO3溶液中物料守恒有c(Na+)= c(HCO3-)+ c(H2CO3)+ c(CO32-),电荷守恒有,c(Na+)+c(H+)= c(HCO3-)+ c(OH-)+ 2c(CO32-),将钠离子浓度消去即可得c(OH-)-c(H+)=c(H2CO3)-c(CO32-),故正确;D. 2×10-4 mol/L的Na2CO3溶液与CaCl2溶液等体积混合出现沉淀,则需要的钙离子最小的浓度
,则c(CH3COO-)/c(CH3COOH)=18,故错误;C. NaHCO3溶液中物料守恒有c(Na+)= c(HCO3-)+ c(H2CO3)+ c(CO32-),电荷守恒有,c(Na+)+c(H+)= c(HCO3-)+ c(OH-)+ 2c(CO32-),将钠离子浓度消去即可得c(OH-)-c(H+)=c(H2CO3)-c(CO32-),故正确;D. 2×10-4 mol/L的Na2CO3溶液与CaCl2溶液等体积混合出现沉淀,则需要的钙离子最小的浓度![]() ×2= 5.6×10-5 mol/L,钙离子浓度大于就可以出现沉淀,故错误。故选C。
×2= 5.6×10-5 mol/L,钙离子浓度大于就可以出现沉淀,故错误。故选C。


科目:高中化学 来源: 题型:
【题目】关于基本营养物质的说法不正确的是( )。
A.所有蛋白质均可通过遇浓硝酸变黄色来鉴别
B.我国居民传统膳食结构中能量的主要来源是糖类
C.人体血糖含量指的是血液中含葡萄糖的多少
D.油脂在碱性条件下的水解产物可以用来制取肥皂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铁、氧化铜、稀硫酸、氢氧化钠溶液和硫酸铜溶液五种物质构成了如下图所示的关系网络(图中的“——”表示相连的两种物质常温下能发生反应)。下列说法不正确的是( )
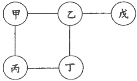
A.甲可能为氢氧化钠溶液B.乙可以使紫色石蕊溶液变红
C.丙和丁的反应一定是置换反应D.戊一定是氧化铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在10 mL 0.1 mol·L-1 Na2CO3溶液中逐滴加入0.1 mol·L-1 HCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示(CO2因逸出未画出,忽略因气体逸出引起的溶液体积变化),下列说法正确的是

A. 在0.1 mol/L Na2CO3溶液中:c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-)
B. 当溶液的pH为7时,溶液的总体积为20 mL
C. 在B点所示的溶液中,浓度最大的阳离子是Na+
D. 在 A点所示的溶液中:c(CO32-)=c(HCO3-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵晶体[(NH4)2Fe(SO4)2·6H2O]是分析化学中重要的试剂,常用于代替硫酸亚铁。硫酸亚铁铵晶体在500°C时隔绝空气加热完全分解。回答下列问题:
(1)硫酸亚铁铵晶体隔绝空气加热完全分解,发生了氧化还原反应,固体产物可能有FeO和Fe2O3,气体产物可能有NH3、SO3、H2O、N2和__________________
(2)为检验分解产物的成分,设计如下实脸装置进行实验,加热A中的硫酸亚铁铵晶体至分解完全。

①A中固体充分加热较长时间后,通入氮气,目的是_______________________________。
②为检验A中残留物是否含有FeO,需要选用的试剂有______________(填标号)。
A.KSCN溶液 B.稀硫酸 C.浓盐酸 D.KMnO4溶液
(3)通入酸性高锰酸钾溶液,溶液褪色,该反应中SO2表现出化学性质是_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘和铁均是人体必需的微量元素。
(1)海带中含有丰富的以碘离子形式存在的碘元素。在实验室中,从海藻中提取碘的流程如下:

①上述流程中涉及下列操作,其中错误的是________________(填标号)。
A.将海藻灼烧成灰
B.过滤含I-溶液
C.下口放出含碘的苯溶液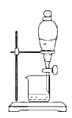
D.分离碘并回收苯
②写出步骤④发生反应的离子方程式:_______________________________________
③要证明步骤④所得溶液中含有碘单质,可加入___________________(填试剂名称),观察到________________________(填现象)说明溶液中存在碘。
(2)探究铁与稀硝酸的反应。用5.6gFe粉和含有0.3 mol HNO3的稀硝酸进行实验,若两种物质恰好完全反应,且HNO3只被还原成NO。回答下列问题:
①Fe粉与稀硝酸反应生成硝酸铁的化学方程式为___________________________________
②反应结束后的溶液中Fe3+、Fe2+的物质的量之比n(Fe3+):n(Fe2+)=_________________。
③标准状况下,生成NO气体的体积为_________________L(保留两位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关甲烷的描述正确的是( )
A.甲烷是最简单的有机物,也是含碳量最高的有机物
B.甲烷是一种无色无味,密度比空气小,易溶于水的气体
C.甲烷是天然气、坑道气、沼气的主要成分
D.甲烷性质不活泼,除可燃外,不与其他物质反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的定容容器中,当下列的物理量不再发生变化时,表明反应A(固)+2B(气)![]() C(气)+D(气)已达到平衡状态的是( )
C(气)+D(气)已达到平衡状态的是( )
A. 混合气体的压强 B. 混合气体的密度
C. 气体的总物质的量 D. A的物质的量浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示物质A~F之间的转化关系,其中A为淡黄色固体物质,B、C为无色溶液,D为气体,E、F为白色沉淀。请填写下列各空:
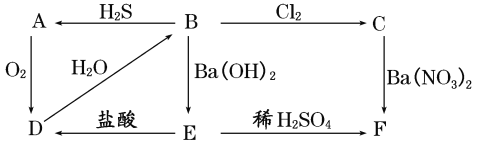
(1)写出各物质的化学式:
A为______,B为_____,C为_____,D为_____,E为_____,F为______。
(2)写出下列反应的化学方程式:
B→A:________________________。
B→C:___________________________。
(3)写出C→F的离子方程式:___________________。
(4)在A~F六种物质中,既有氧化性又有还原性的是(填字母代号)______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com