
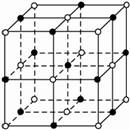
?
(1)请将其代表Na+的用笔涂黑圆点,以完成 NaCl晶体结构示意图。并确定晶体的晶胞,分析其构成。?
(2)从晶胞中分Na+周围与它最近时且距离相等的 Na+共有多少个??
解析:将下图中心圆涂黑为Na+,与之相隔均要涂黑?

?
(1)图由8个小立方体构成,为晶体的晶胞,计算在该晶胞中含有Na+的数目。在晶胞中心有1个Na+,在棱上共有4个Na+,一个晶胞有6个面,与这6个面相接的其他晶胞还有6个面,共12个面。又因棱上每个Na+又为周围4个晶胞所共有,所以该晶胞独占的Na+是12×1/4=3个。该晶胞共有的Na+为4个。?
晶胞中含有的Cl-数:Cl-位于顶点及面心处,每个平面上有4个顶点与1个面心,而每个顶点上的氯离子又为8个晶胞(本层4个,上层4个)所共有,因此该晶胞独占8×1/8=1个。一个晶胞有6个面,每面有一个面心氯离子,又为两个晶胞共有,所以该晶胞中独占的Cl-数为6×1/2=3。即该晶胞共有的Cl-为4个。?
不难推出,![]() (Na+)∶
(Na+)∶![]() (Cl-)=4∶4=1∶1。化学式为NaCl。?
(Cl-)=4∶4=1∶1。化学式为NaCl。?
(2)以中心Na+为依据,画上或找出三个平面(三个平面互相垂直)。在每个平面上的Na+都与中心 Na+最近且为等距离。?
每个平面上又都有4个Na+,所以与Na+最近相邻且等距的Na+为3×4=12个。?
答案:(1)含8个小立方体的NaCl晶体示意图为一个晶胞;在晶胞中Na+与Cl-个数比为1∶1。(2)12个。


 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案科目:高中化学 来源: 题型:
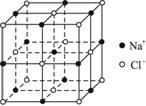
(1)请将其中代表Na+的圆圈用笔涂黑,以完成氯化钠晶体结构示意图并确定晶体的晶胞。
(2)从晶胞中分析氯化钠化学式为NaCl。
(3)在每个Na+周围与它最近的且距离相等的Na+有多少个?
查看答案和解析>>
科目:高中化学 来源:2012年苏教版高中化学选修3 4.2配合物是如何形成的(解析版) 题型:简答题
下图为氯化钠晶体结构图,图中直线交点处为NaCl晶体中Na+与Cl-所处的位置(不考虑体积的大小)。
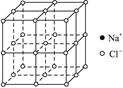
(1)请将其中代表Na+的圆圈用笔涂黑,以完成氯化钠晶体结构示意图并确定晶体的晶胞。
(2)从晶胞中分析氯化钠化学式为NaCl。
(3)在每个Na+周围与它最近的且距离相等的Na+有多少个?
查看答案和解析>>
科目:高中化学 来源:2013届吉林长春实验中学高二下学期期末考试化学试卷(解析版) 题型:填空题
(9分)氮元素可形成多种离子,如N3—、N3—、NH2—、NH4+、N2H5+、N2H62+等。
(1)与N相邻的两种元素C、O,三者第一电离能由大到小为_______
(2)N≡N的键能为942 kJ·mol-1,N-N单键的键能为247 kJ·mol-1,说明N2中的 键比 键稳定(填“σ”或“π”)。
(3)液态氨可电离出NH2-。NH2-的电子式为 。
(4)已知NH4H为离子化合物,写出其与重水D2O反应的生成物(加热) ;Na3N也为离子化合物,则Na3N与水反应的化学方程式为 ,反应类型为 。
(5)X+中所有电子正好充满K、L、M三个电子层,它与N3—形成的晶体结构如图所示。与同一个N3—相连的X+ 有 个。X原子的基态电子排布式为_____________
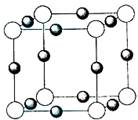
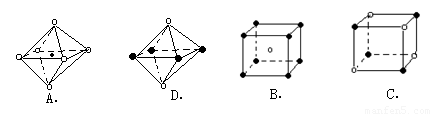
(6)最近科学家研制出某元素Z与N元素形成的晶体ZN,已知ZN晶体具有与NaCl相似的晶体结构。下图是从ZN晶体结构图中分割出来的部分结构图,试判断符合ZN晶体结构图的是_______
|
查看答案和解析>>
科目:高中化学 来源: 题型:
镁、铜等金属离子是人体内多种酶的辅因子。工业上从海水中提取镁时,先制备无水氯化镁,然后将其熔融电解,得到金属镁。
(1)以MgCl2为原料用熔融盐电解法制备镁时,常加入NaCl、KCl或CaCl2等金属氯化物,其主要作用除了降低熔点之外还有 。
(2)已知MgO的晶体结构属于NaCl型。某同学画出的MgO晶胞结构示意图如下图所示,请改正图中错误: 。

(3)用镁粉、碱金属盐及碱土金属盐等可以做成焰火。燃放时,焰火发出五颜六色的光,请用原子结构的知识解释发光的原因: 。
(4)Mg是第三周期元素,该周期部分元素氟化物的熔点见下表:
| 氧化物 | NaF | MgF2 | SiF4 |
| 熔点/K | 1266 | 1534 | 183 |
解释表中氟化物熔点差异的原因: 。
(5)人工模拟是当前研究的热点。有研究表明,化合物X可用于研究模拟酶,当其结
![]() 或Cu(I)(I表示化合价为+1)时,分别形成a和b:
或Cu(I)(I表示化合价为+1)时,分别形成a和b:

①a中连接相邻含N杂环的碳碳键可以旋转,说明该碳碳键具有 键的特性。
②微粒间的相互作用包括化学键和分子间相互作用,比较a和b中微粒间相互作用力的差异
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com