
| ||


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
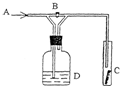 如图是一种试验氯气化学性质的实验装置,图中B为开关. 如先打开B,再让一种含氯气的气体从A处通入,C中干燥红色布条颜色褪色;当关闭B时,C处红色布条颜色无变化.则D瓶中盛有的溶液是( )
如图是一种试验氯气化学性质的实验装置,图中B为开关. 如先打开B,再让一种含氯气的气体从A处通入,C中干燥红色布条颜色褪色;当关闭B时,C处红色布条颜色无变化.则D瓶中盛有的溶液是( )| A、①②③ | B、②③④ |
| C、①②④ | D、①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com