
��������(ClO2)��һ�ֻ���ɫ�д̼�����ζ�����壬���۵�Ϊ��59�棬�е�Ϊ11.0�棬������ˮ����ҵ�����Գ�ʪ��KClO3�Ͳ���(H2C2O4)��60��ʱ��Ӧ�Ƶã�ijѧ��������ͼ1��ʾװ��ģ�ҵ��ȡ���ռ�ClO2��
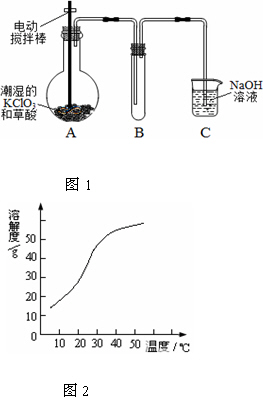
(1)A�з�Ӧ������K2CO3��ClO2��CO2�ȣ���д���÷�Ӧ�Ļ�ѧ����ʽ��________��
(2)A���������¶ȿ���װ�ã����ƾ����⣬����Ҫ�IJ���������________��BҲ���������¶ȿ���װ�ã�Ӧ����________װ�ã�
(3)��Ӧ����װ��C�пɵ�NaClO2��Һ����֪NaClO2������Һ�����¶ȵ���38��ʱ����������NaClO2��3H2O�����¶ȸ���38��ʱ����������NaClO2������ͼ2��ʾ��NaClO2���ܽ�����ߣ��벹���NaClO2��Һ���Ƶ�NaClO2�IJ������裺
��________����________����ϴ�ӣ��ܸ��
(4)ClO2�ܲ��ȶ������������ƣ�������ˮ���յõ�ClO2��Һ��Ϊ�ⶨ������Һ��ClO2�ĺ���������������ʵ�飺
����1��ȷ��ȡClO2��Һ10 mL��ϡ�ͳ�100 mL��������ȡV1 mL�������뵽��ƿ�У�
����2������������pH��2.0������������KI���壬����Ƭ�̣�
����3���������ָʾ������c mol/L��Na2S2O3��Һ�ζ����յ㣬����Na2S2O3��ҺV2 mL��(��֪2 Na2S2O3��I2��Na2S4O6��2NaI)
�ٵζ������У��������������ƽ�вⶨ��ԭ����________��
��ԭClO2��Һ��Ũ��Ϊ________g/L(�ú���ĸ�Ĵ���ʽ��ʾ)��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A.ClO2��ǿ������
B.ClO2��ǿ��ԭ��
C.ClO2�����ӻ�����
D.ClO2����������1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������֯��WHO������������ClO2��ΪA����Ч��ȫ���������������ʳƷ���ʡ�����ˮ�����ȷ������Ź㷺Ӧ�á�����˵����ȷ���ǣ� ��
A.����������ǿ������ B.����������ǿ��ԭ��
C.�������������ӻ����� D.�������ȷ�������Ϊ-1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������������ˮ����ʹˮ�е��л�����Ȼ���Ӧ�������л����Ȼ�����������к������绷�����˽����ƹ���ø�Ч��������������(ClO2)������
(1)ʹ��ClO2������ˮ���������ŵ���_____________________________��
(2)Ŀǰ�������NaClO3��ŨHCl��Ӧ��ȡClO2��ͬʱ��Cl2���ɣ������ΪClO2��һ�룬д����Ӧ�Ļ�ѧ����ʽ��__________________________________________________
(3)������Ӧ�в���0.1 mol Cl2��ת�Ƶĵ��ӵ����ʵ���Ϊ_________ mol��
(4)��H2SO4���������£���Na2SO3��ԭNaClO3���Ƶ�ClO2����ӦΪ��2NaClO3+Na2SO3 +H2SO4====2ClO2��+2Na2SO4+H2O
���ַ������ŵ���____________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ��ɽ��ʡ�����и���1���¿���ѧ�Ծ��������棩 ���ͣ������
(15��)��Դ�Ŀ������������������Ŀɳ�����չϢϢ��أ�����������ú���Դ�ǰ���������ǰ���ش���⡣
I����֪��Fe2O3(s)+3C(ʯī) =2Fe(s)+3CO(g) ��H=akJ��mol-1
CO(g)+1��2O2(g)= CO2(g) ��H=bkJ��mol-1
C(ʯī)+O2(g)=CO2(g) ��H=ckJ��mol-1
��Ӧ��4Fe(s)+3O2(g)= 2Fe2O3(s)���ʱ��H= kJ��mol-1��
��1������ԭ��صĹ���ԭ�������л�ѧ��Ӧ�������Ͽ�����Ƴ�ԭ��ص��� (�����)��
A��C(s)+CO2(g)=2CO(g)
B��NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)
C��2H2O(l)= 2H2(g)+O2(g)
D��CH4(g)+2O2(g)=CO2(g)+2H2O(l)
����KOH��ҺΪ�������Һ��������ѡ��Ӧ������Ƴ�һ��ԭ��أ���д����ԭ��صĵ缫��Ӧ��
������ ��
������ ��
��2����������(ClO2)��һ�ָ�Ч��ȫ������ˮ��������ClO2��һ�ֻ���ɫ���壬������ˮ��ʵ������NH4Cl�����ᡢNaClO2Ϊԭ���Ʊ�ClO2�������£�

��֪���������з����ķ�ӦΪ��
NH4Cl+2HCl NCl3+3H2��������NCl3�е�Ԫ��Ϊ+3�ۡ�
NCl3+3H2��������NCl3�е�Ԫ��Ϊ+3�ۡ�
��д�����ʱ�����ĵ缫��Ӧʽ ��
���������Ϸŵ������(������)�� ��
�۳�ȥClO2�е�NH3��ѡ�õ��Լ��� (�����)
A����ʯ�� B����ʯ�� C��ŨH2SO4 D��ˮ
�������������У�ÿ����1mol ClO2�������� mol NCl3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012���˽̰���л�ѧѡ��6 4.2����ѧ�����̽����ϰ���������棩 ���ͣ�ѡ����
����������֯(WHO)����������(ClO2)��ΪA����Ч��ȫ���������������ʳƷ���ʡ�����ˮ�����ȷ������Ź㷺Ӧ�ã��ɴ˿��ж϶�������(����)
A����ǿ������
B����ǿ��ԭ��
C�������ӻ�����
D����������Ԫ��Ϊ��1��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com