
| A. | ①③④⑥ | B. | ②③⑤ | C. | ①②④ | D. | ①③⑤ |
分析 配位化合物一般指由金属的原子或离子与含有孤对电子的分子或离子通过配位键结合形成的化合物.配离子或配合物可以在溶液中稳定存在.
解答 解:①CuSO4•5H2O实际组成为[Cu(H2O)4]SO4•H2O,含有[Cu(H2O)4]2+配离子,属于配合物;
②K2PtCl6 中存在配离子[PtCl6]2-,属于配合物;
③KCl•CuCl2在溶液中完全电离为钾离子、铜离子与离子,属于复盐,不属于配合物;
④Cu(NH2CH2COO)2 中N原子含有的孤对电子能与铜离子形成配位键,属于配合物;
⑤KCl•MgCl2•6H2O 属于复盐;
⑥Cu(CH3COO)2 为醋酸铜,溶于水电离出醋酸根,属于简单盐.
故选C.
点评 本题考查配合物概念,属易错题目,识记常见配合物,注意含有配位键的化合物就不一定是配位化合物,配离子或配合物可以在溶液中稳定存在.


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:选择题
| A. | 4mL | B. | 10.8mL | C. | 1.2mL或4mL | D. | 8mL或10.8mL |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
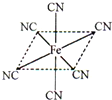 铁元素应用广泛,Fe2+与KCN溶液反应得Fe(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成黄血盐,其配离子结构如图;已知CN-与N2结构相似,1molCN-中π键数目为2NA.
铁元素应用广泛,Fe2+与KCN溶液反应得Fe(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成黄血盐,其配离子结构如图;已知CN-与N2结构相似,1molCN-中π键数目为2NA.查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元 素 | Mn | Fe | |
| 电离能 /kJ•mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯乙烯(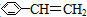 ) ) | B. | 苯甲酸( ) ) | C. | 苯甲醛( ) ) | D. | 苯乙酮( ) ) |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
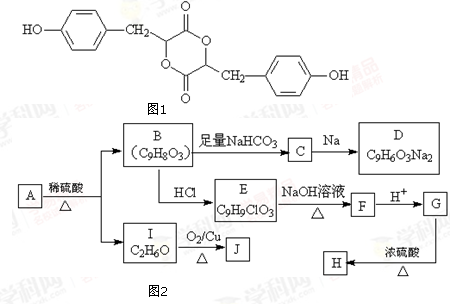
 .
. .
. +
+ $→_{△}^{催化剂}$
$→_{△}^{催化剂}$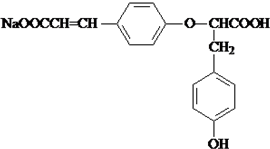 +HCl.
+HCl.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com