
���� ��1������һ�����ʵ���Ũ�ȵ���Һ��pH��С��ȷ������ʵĵ���̶ȣ�����ȷ��ǿ������ʣ�
��2����������Լ�����ѡ��0.1mol/L NH4Cl��Һ��pH��ֽ�����òⶨ��ҺPH�ж���Һ�����ԣ�֤��笠�����ˮ��֤��һˮ�ϰ���������ʣ�
��� �⣺��1�������ˮ��ǿ�0.01mol•L-1��ˮ��pHΪ10��˵��c��OH-��=10-4mol/L��NH3•H2Oû����ȫ���룬����ˮ�����
�ʴ�Ϊ���ǣ�����ǿ����ʣ���0.01mol•L-1��ˮ��c��OH-��Ϊ0.01mol•L-1����pH=12��
��2���������Ϣ��֪��ѡ��0.1mol/L NH4Cl��Һ��pH��ֽ������ʵ����֤һˮ�ϰ���������ʣ�PH�ⶨ�Ȼ����Һ�����ԣ�˵��笠�����ˮ�������ԣ�˵��һˮ�ϰ���������ʣ�
�ʴ�Ϊ���ò�����պȡ0.1mol•L-1NH4Cl��Һ����pH��ֽ�ϣ���ɫ�������ɫ���Ƚϣ����pH��pH��7��
���� ���⿼��������ʵ�ʵ��̽������Ҫ��������ƽ��Ĵ��ڣ����ü��跨��������ɣ��ѶȲ������ڿ���ѧ���ķ���������ʵ��̽��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ԣ�HNO3��H2CO3��H2SiO3 | B�� | �ȶ��ԣ�H2S��H2O��HF | ||
| C�� | ��ԭ�ԣ�Cl-��Br-��I- | D�� | ���ԣ�NaOH��Mg��OH��2��Ca��OH��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ͭ��ˮ��ͷ���Ӵ��ĸ���ˮ��������ʴ | |
| B�� | ������̼�����顢���������������ЧӦ������ | |
| C�� | �ڹ�ҵ�����У����Ƴ��ڽϵ��¶Ⱥ�ѹǿ����ʹ��ӦѸ�ٽ��еĴ��������ܺõĽ���Ч����������ʮ�˴�����ġ���ɫ��չ������ | |
| D�� | ʯ���ѽ⡢ú����������ˮ��þ��������ѧ�仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | A | B | C | D |
| n��CO2����mol�� | 2 | 3 | 4 | 6 |
| n����������mol�� | 2 | 2 | 3 | 3 |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
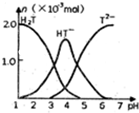 �����£���10ml0.2mol•L-1���ᣨ��H2T��ʾ����Һ����μ����Ũ�ȵ�NaOH��Һ���й��������ʵ���������Һ��PH����ͼ��ϵ������˵����ȷ���ǣ�������
�����£���10ml0.2mol•L-1���ᣨ��H2T��ʾ����Һ����μ����Ũ�ȵ�NaOH��Һ���й��������ʵ���������Һ��PH����ͼ��ϵ������˵����ȷ���ǣ�������| A�� | HT-����Һ��ˮ��̶ȴ��ڵ���̶� | |
| B�� | ��V��NaOH��=10mLʱ����Һ��ˮ�ĵ���̶ȱȴ�ˮ�� | |
| C�� | ��V��NaOH��=15mLʱ����Һ�д��ڣ�c��Na+����c��HT-����c��T2-����c��OH-����c��H+�� | |
| D�� | ��V��NaOH��=20mLʱ����Һ�д��ڣ�c��OH-��=c��HT-��+2c��H2T��+c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �к���ͬ�������������Һ����NaOH�����ʵ�����ͬ | |
| B�� | ������Һ��Ũ��С������ | |
| C�� | ������Һ����ˮ���������c��H+������ͬ | |
| D�� | �ֱ�������ˮϡ����ͬ�����������pH���ڴ����pH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com