
 ��Cl2���������л���ʱ�����HCl�����÷�Ӧ4HCl��g��+O2��g��?2Cl2��g��+2H2O��g����ʵ���ȵ�ѭ�����ã�
��Cl2���������л���ʱ�����HCl�����÷�Ӧ4HCl��g��+O2��g��?2Cl2��g��+2H2O��g����ʵ���ȵ�ѭ�����ã����� ��1�����Ӳ�Խ�࣬ԭ�Ӱ뾶Խ��ͬ����ԭ���������ԭ�Ӱ뾶С������Ԫ��ͬ��Ķ�����Ԫ��ԭ��ΪF��������9�����ӣ�
��2���ǽ�����Խǿ����Ӧ�⻯��Խ�ȶ������ʵ�������Խǿ�����������ʡ�������������أ�
��3�����û�ѧƽ����������ȡ��������������������жϣ�
��4��4HCl��g��+O2��g��?2Cl2��g��+2H2O��g��
��ʼ 4 1
ת�� 4x x 2x 2x
8min4-4x 1-x 2x 2x
�������������ѹǿ��С��10%����$\frac{4+1}{5-x}$=$\frac{1}{0.9}$�����x=0.5�����v=$\frac{��c}{��t}$���㣻
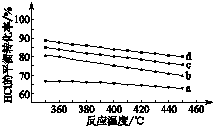
��5������������������ʱ��O2����Խ��HCl��ת����Խ��
����ͼ��֪����HCl��ת������ͬʱ���¶��ɵ͵��߶�Ӧ��Ͷ�ϱ�Ϊ4��1��2��1��1��1���ɴ˿�ȷ���¶���Ͷ�ϱȵĹ�ϵ��������ѹǿ��ƽ�������ƶ���ת��������
�����ݻ�ѧƽ������ʽ��ʽ����õ���
��� �⣺��1�����Ӳ�Խ�࣬ԭ�Ӱ뾶Խ��ͬ����ԭ���������ԭ�Ӱ뾶С����ԭ�Ӱ뾶ΪCl��O��H������Ԫ��ͬ��Ķ�����Ԫ��ԭ��ΪF��������9�����ӣ���������Ų�ʽΪ1s22s22p5��
�ʴ�Ϊ��Cl��O��H��1s22s22p5��
��2���ȡ���ǽ�����ǿ���������ǵ��ʵ������ԡ��⻯����ȶ��ԣ����۵㡢������������أ��ʴ�Ϊ��bc��
��3��a��2�ͣ�HCl����=�ͣ�Cl2���������淴Ӧ���ʲ��ȣ�ֻ�в�ͬ���ʵ����淴Ӧ����֮�ȵ��ڻ�ѧ������֮��Ϊƽ��״̬����A����
b������ʱ��ѹǿΪ����������ϵѹǿ���ٸı䣬�ﵽƽ��״̬����B��ȷ��
c�������������������䣬���ܶȲ��䣬��֪��������ܶȲ��䲻���ж�ƽ��״̬����C����
d����Ӧ���䣬$\frac{{c}^{2}��C{l}_{2}��•{c}^{2}��{H}_{2}O��}{{c}^{4}��HCl��•c��{O}_{2}��}$=K���䣬�����ж�ƽ�⣬��D����
�ʴ�Ϊ��b��
��4��4HCl��g��+O2��g��?2Cl2��g��+2H2O��g��
��ʼ 4 1
ת�� 4x x 2x 2x
8min4-4x 1-x 2x 2x
�������������ѹǿ��С��10%����$\frac{4+1}{5-x}$=$\frac{1}{0.9}$�����x=0.5��
����HCl��ʾ�ĸ÷�Ӧ�Ļ�ѧ��Ӧ����Ϊ$\frac{\frac{0.5mol��4}{2L}}{8min}$=0.125mol/��L��min����
�ʴ�Ϊ��0.125mol/��L��min����
��2������������������ʱ��O2����Խ��HCl��ת����Խ���ɴ˿�ȷ��aΪ6��1��bΪ4��1��cΪ2��1��dΪ1��1���ʴ�Ϊ��6��1��
����ͼ��֪����HCl��ת������ͬʱ���¶��ɵ͵��߶�Ӧ��Ͷ�ϱ�Ϊ4��1��2��1��1��1���ɴ˿�ȷ���¶���Ͷ�ϱȵĹ�ϵ�ǣ�Ͷ�ϱ�Խ�ߴﵽ��ͬת����������¶�Խ�ͣ���ʹ����b�ﵽ����d��ͬ��HClƽ��ת���ʣ��ɲ�ȡ�Ĵ�ʩ�н����¶ȣ�������ѹǿƽ�������ƶ������ѹ�ȣ�
�ʴ�Ϊ�������¶ȣ�����ѹǿ��
����ͼ�ɶ���Ͷ�ϱ�Ϊ2��1���¶�Ϊ400��ʱ��HCl��ת����Ϊ80%����Ͷ���HClΪ2 mol��O2Ϊ1 mol���ɴ˿ɽ�������ʽ��
4HCl��g��+O2��g��?2Cl2��g��+2H2O��g��
n����ʼ��/mol 2 1 0 0
n��ת����/mol 1.6 0.4 0.8 0.8
n��ƽ�㣩/mol 0.4 0.6 0.8 0.8
����ƽ��������Cl2�����ʵ�������=$\frac{0.8mol}{0.4mol+0.6mol+0.8mol+0.8mol}$��100%=30.8%��
�ʴ�Ϊ��30.8%��
���� ���⿼�黯ѧƽ����㼰ԭ�ӽṹ�������ɣ�Ϊ��Ƶ���㣬���ջ�ѧƽ�����η����㡢ƽ��״̬�ж���ԭ�ӽṹ��Ԫ�ص����ʵ�Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬�ۺ��Խ�ǿ����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ס�������ĵ��ʶ��ǽ��� | |
| B�� | �ҡ����������Ƿǽ���Ԫ�� | |
| C�� | �ҡ������������γ������� | |
| D�� | �ѵ�������ȿ�����KOH��Һ�ֿ�����H2SO4��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��̼��þ�еμ�ϡ���CO32-+2H+�TCO2��+H2O | |
| B�� | Ũ�ռ���Һ�м�����Ƭ��Al+2OH-�TAlO2-+H2�� | |
| C�� | �Ȼ�����̼�������Һ��ϣ�Ca2++CO32-�TCaCO3�� | |
| D�� | �ö��Ե缫����Ȼ�þ��Һ��Mg2++2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$Cl2��+H2��+Mg��OH��2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ˮ��Һ�����һ���Ƿ��Ӿ��� | B�� | ����̬�����һ�������Ӿ��� | ||
| C�� | ԭ�Ӿ����̬һ�������� | D�� | ���Ӿ�������̬һ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ũ������±�� | B�� | ��Ũ���Ṳ����ȥ | ||
| C�� | ͭ�������� | D�� | ����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ������ | ������ |
| A | 1-�����ķе�ȼ���ķе��89�� | 1-�����ͼ����ͨ������������� |
| B | ԭ��ؿɽ���ѧ��ת��Ϊ���� | ԭ�������ӵ�Դ���ܹ��� |
| C | H2SO4�����ӻ����� | ������Һ�ɵ��� |
| D | �Ҷ������KMnO4��Һ������Ӧ | �Ҷ���������� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
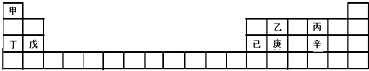
| A�� | XԪ�ؿ�����ɶ��ֵ��� | |
| B�� | Y��Z������ͬһ���� | |
| C�� | X��W�γɵĻ������Z��W�γɵĻ�����Ļ�ѧ�����Ͳ�ͬ | |
| D�� | Ԫ��X��Y��W������������Ӧˮ���������ǿ����X��Y��W |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com