
ʵ������Ҫ0.1 mol·L��1 NaOH��Һ450 mL��0.5 mol·L��1������Һ500 mL��������������Һ����������ش��������⣺
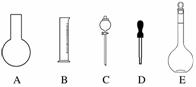
(1)��ͼ��ʾ��������������Һ�϶�����Ҫ����
(�����)������������Һ�����õ��IJ��������� (����������)��
(2)������NaOH��Һʱ��
�ٸ��ݼ�����������ƽ��ȡNaOH������Ϊ g��
����NaOH��Һ��ת��������ƿʱ����������������������ҺŨ�� (�>������<������)0.1 mol·L��1��
����NaOH�����ܽ��������������ƿ��ϴ�ձ���ϴ��Һ��������ƿ�����ݣ���������ҺŨ�� (�>������<������)0.1 mol·L��1��
(3)������������Һʱ��
��������������Ϊ98%���ܶ�Ϊ1.84 g·cm��3��Ũ��������Ϊ (����������һλС��)mL��
�����ʵ������15 mL��20 mL��50 mL��Ͳ��Ӧѡ�� mL��Ͳ��ã�
�����ƹ������������ձ��н�Ũ�������ϡ�ͣ�ϡ��ʱ���������� ��
�𰸡�(1)AC���ձ���������
(2)��2.0����<����>
(3)��13.6����15���۽�Ũ���������ڻ�������ˮ�У����ò��������Ͻ���
������(1)������Һ��Ҫ���ֲ�����������Ͳ���ձ�������������ͷ�ιܡ�����ƿ��
(2)������450 mL������ƿ������NaOH��ҺҪ��500 mL������ƿ��m(NaOH)��c·V·M��0.1 mol·L��1��0.5 L��40 g·mol��1��2.0 g����NaOH����ˮ�ų������ȣ�Ӧ������ȴ�����º�����������ƿ�У������ݺ���Һ��ȴ�����º������С��Ũ��ƫ�ߡ�
(3)��c(Ũ)·V(Ũ)��c(ϡ)·V(ϡ)����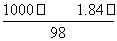 ��V(Ũ)��0.5��0.5����V(Ũ)��0.013 6 L��13.6 mL����ѡ��15 mL��Ͳ��ã����С����ע�����㣺����ˮ�������ڡ������衣
��V(Ũ)��0.5��0.5����V(Ũ)��0.013 6 L��13.6 mL����ѡ��15 mL��Ͳ��ã����С����ע�����㣺����ˮ�������ڡ������衣



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��Ҫ��ش��������⣺
(1) 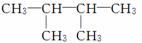 ��ϵͳ����Ϊ________��
��ϵͳ����Ϊ________��
(2)3��2��ϩ�Ľṹ��ʽΪ________��
(3) �ķ���ʽΪ________��
�ķ���ʽΪ________��
(4)ij���ķ���ʽΪC4H4�����Ǻϳ����м��壬���ж���ͬ���칹�塣
����д������һ����ʽ�ṹ��ͬ���칹��Ľṹ��ʽ____________��
������һ��ͬ���칹�壬ÿ��̼ԭ�Ӿ��ﱥ�ͣ���̼��̼�ļн���ͬ���÷�����̼ԭ���γɵĿռ乹��Ϊ____________�Ρ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����жϣ���ȷ�Ļ����̡�������Ļ�������
(1)1 Lˮ���ܽ�5.85 g NaCl���γɵ���Һ�����ʵ���Ũ����0.1 mol·L��1(����)
(2)��25 g CuSO4·5H2O��������75 gˮ���������ʵ���������Ϊ25%(����)
(3)��100 mL���ձ��У�����10 gʳ�Σ�Ȼ��ע��90 mL��ˮ������ܽ���������ʵ���������Ϊ90%(����)
(4)��40 g SO3����60 gˮ���������ʵ���������Ϊ40%(����)
(5)��62 g Na2O����ˮ�У����1 L��Һ���������ʵ����ʵ���Ũ��Ϊ1 mol·L��1(����)
(6)T ��ʱ100 g����ʳ��ˮ�У�����NaCl������Ϊm g������¶�ʱ��NaCl���ܽ����m g(����)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����жϣ���ȷ�Ļ����̡�������Ļ�������
(1)������ƿ����Һʱ������ˮ�����̶��ߣ������õι���������Һ��(����)
(2014·�¿α�ȫ������12D)
(2)������Һ����ʱ����������ƿ�̶Ȼ�ʹ��ҺŨ��ƫ��(����)
(2014·���ȫ������6C)
(3)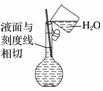 ������Һ(����)
������Һ(����)
(2014·ɽ�����ۣ�10A)
(4)��ΪKNO3���ܽ�ȴ����Կ����ؽᾧ����ȥKNO3�л��е�NaCl(����)
(2014·�㶫���ۣ�9A)
(5)��ΪCa(OH)2���Ƴɳ���ʯ��ˮ�����Կ�����2.0 mol·L��1��Ca(OH)2��Һ(����)
(2014·�㶫���ۣ�9D)
(6)����0.100 0 mol·L��1�Ȼ�����Һʱ����Һ��ת�Ƶ�����ƿ�����ò���������(����)
(2013·�������ۣ�10C)
(7)������ƿ������Һ������ʱ���ӿ̶��ߣ�������ҺŨ��ƫС(����)
(2013·������ۣ�4B)
(8)�ù���NaCl����0.5 mol·L��1����Һ�����õ������У��ձ�������������ͷ�ιܡ�����ƿ(����)
(2013·ɽ�����ۣ�11C)
(9)�� ����100 mL 0.100 0 mol·L��1 K2Cr2O7��Һ(����)
����100 mL 0.100 0 mol·L��1 K2Cr2O7��Һ(����)
(2012·������ۣ�4D)
(10)��50 mL��Ͳ������0.100 0 mol·L��1̼������Һ(����)
(2012·�������ۣ�6C)
(11)��100 mL����ƿ���ձ�������������ͷ�ιܺ�pH��1����������100 mL pH��2������(����)
(2012·�������ۣ�10B�ı�)
(12)����Ͳ��ȡ20 mL 0.500 0 mol·L��1 H2SO4��Һ���ձ��У���ˮ80 mL�����Ƴ�0.100 0 mol·L��1 H2SO4��Һ(����)
(2011·���գ�7B)
(13)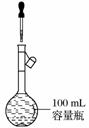 ���ݲ���(����)
���ݲ���(����)
(2010·�������ۣ�8B)
(14)������Һʱ������ˮ��������ƿ�̶ȣ�Ӧ�ý�ͷ�ιܽ�������Һ����(����)
(2010·ɽ�����ۣ�14B)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
20 ��ʱ������NaCl��Һ���ܶ�Ϊ�� g·cm��3�����ʵ���Ũ��Ϊc mol·L��1��������˵���д������(����)
A���¶ȵ���20 ��ʱ������NaCl��Һ��Ũ��С��c mol·L��1
B��20 ��ʱ������NaCl��Һ����������Ϊ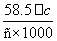 ��100%
��100%
C��20 ��ʱ���ܶ�С�ڦ� g·cm��3��NaCl��Һ�Dz�������Һ
D��20 ��ʱ������NaCl��Һ���ܽ��S��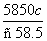 g/100 gˮ
g/100 gˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����йص����Ų�ͼ�ı�����ȷ���ǣ� ��
A. 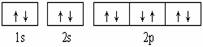 �ɱ�ʾ����10�������ӻ�̬ʱ�����Ų�
�ɱ�ʾ����10�������ӻ�̬ʱ�����Ų�
B. 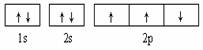 ��ͼ����Υ��������ԭ��
��ͼ����Υ��������ԭ��
C.  ��ʾ��̬Nԭ�ӵļ۵����Ų�
��ʾ��̬Nԭ�ӵļ۵����Ų�
D. 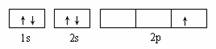 ��ʾ���ڼ���̬��B�ĵ����Ų�ͼ
��ʾ���ڼ���̬��B�ĵ����Ų�ͼ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�й������������ȷ���ǣ� ��
A��ÿһ��ˮ������ƽ�������������
B���������λ��һ����Ҳ�ǹ��ۼ���һ��
C������ǵ���Ũ�������ճ����ԭ��֮һ
D������H2O�к�����������ˮ��һ�ַdz��ȶ��Ļ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͼ���о�������ʴ��װ��ͼ������˵������ȷ����(����)
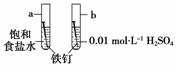
A��a��b�����ĸ�ʴ���ʣ�a��b
B��a��b���������е�̼��Ϊ����
C��a��b���������е�����ʧ���ӱ�����
D��a��b������������Ӧʽ��ΪO2��4e����4H��===2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�Կ��淴Ӧ4NH3(g) + 5O2(g) 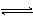 4NO(g) + 6H2O(g)������������ȷ���ǣ� ��
4NO(g) + 6H2O(g)������������ȷ���ǣ� ��
A���ﵽ��ѧƽ��ʱ��4v����O2�� = 5v�棨NO��
B������λʱ��������x mol NO��ͬʱ������x mol NH3����Ӧ�ﵽƽ��״̬
C���ﵽ��ѧƽ��ʱ�����������������������Ӧ���ʼ�С���淴Ӧ��������
D����ѧ��Ӧ���ʹ�ϵ�ǣ�v����NH3��= v����H2O��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com