
分析 由①Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=-24.8kJ/mol
②3Fe2O3(s)+CO(g)═2Fe3O4(s)+CO2(g)△H=-47.2kJ/mol
③Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=-19.4kJ/mol
结合盖斯定律可知,$\frac{①×3-②-③×2}{6}$得到FeO(s)+CO(g)=Fe(s)+CO2(g),以此来解答.
解答 解:由①Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=-24.8kJ/mol
②3Fe2O3(s)+CO(g)═2Fe3O4(s)+CO2(g)△H=-47.2kJ/mol
③Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=-19.4kJ/mol
结合盖斯定律可知,$\frac{①×3-②-③×2}{6}$得到FeO(s)+CO(g)=Fe(s)+CO2(g),△H=$\frac{(-24.8kJ/mol)×3-(-47.2kJ/mol)-2×(-19.4kJ/mol)}{6}$=-11kJ•mol-1,即热化学方程式为FeO(s)+CO(g)=Fe(s)+CO2(g)△H=-11kJ•mol-1,
故答案为:FeO(s)+CO(g)=Fe(s)+CO2(g)△H=-11kJ•mol-1.
点评 本题考查热化学方程式的书写,为高频考点,把握物质的量与热量的关系、焓变为解答的关键,侧重分析与应用能力的考查,注意盖斯定律的应用,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 13g 和 和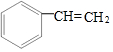 的混合物中含有的电子数为7NA 的混合物中含有的电子数为7NA | |
| B. | 60gSiO2中含有的共价键数目为4NA | |
| C. | 标准状况下,11.2LH2和Cl2反应后得到的气体中含有的原子总数为NA | |
| D. | 1molNaCO3溶于水后,所得溶液中CO32-和HCO3-的总数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| ①CH3COOH | ②H2CO3 | ③H2S | ④H3PO4 |
| K=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=9.1×10-8 K2=1.1×10-12 | K1=7.5×10-3 K2=6.2×10-8 K3=2.2×10-13 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu溶于稀HNO3:Cu+2H++NO3-═Cu2++NO2↑+H2O | |
| B. | 用石墨电极电解饱和食盐水:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑ | |
| C. | (NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-═Fe(OH)2↓ | |
| D. | 向Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-═2Fe2++I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D |
| 向一定量石灰石中滴加稀盐酸 | 向一定量硫酸铜溶液中不断加入铁粉 | 向足量盐酸中加等量的金属Zn、Fe | 向一定量过氧化氢溶液中加入少量二氧化锰 |
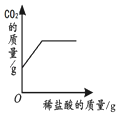 | 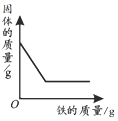 | 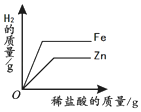 | 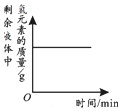 |
| A. | A | B. | B | C. | C | D. | DA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 用饱和食盐水和稀硫酸为原料制取HCl | |
| B. | 用大理石和稀硫酸制取CO2 | |
| C. | 用铁和盐酸为原料制取H2 | |
| D. | 用双氧水和二氧化锰为原料制取O2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com