
【题目】某烃的含氧衍生物的球棍模型如图所示(图中球与球之间连线代表化学键单键或双键)。下列关于该有机物的说法正确的是( )

A.该有机物的名称是乙酸乙酯
B.该有机物能使Br2的CCl4或酸性高锰酸钾褪色,原理相同
C.该有机物能发生取代反应、氧化反应和消去反应
D.该有机物的同分异构体中能与NaHCO3反应产生气体的链状结构只有3种
【答案】D
【解析】
由球棍模型可知有机物应为CH3COOCH=CH2,含有酯基和碳碳双键,结合酯和烯烃的性质解答该题。
A. 由球棍模型可知有机物应为CH3COOCH=CH2,不是乙酸乙酯,A项错误;
B. 含有碳碳双键,可与溴水发生加成反应,与高锰酸钾发生氧化反应,B项错误;
C. 含有酯基,可发生取代反应,含有碳碳双键,可发生氧化反应,不能发生消去反应,C项错误;
D. 该有机物的分子式为C4H6O2,不饱和度为2,其同分异构体能与NaHCO3反应放出CO2,应含有羧基,即C3H5-COOH,为链状结构,则烃基为丙烯基,该有机物为丁烯酸,而丙烯基有三种,则同分异构体为3种,分别为CH2=CHCH2COOH,CH2=C(CH3)COOH,HOOCCH=CHCH3, D项正确;
答案选D。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某同学用下列装置进行有关Cl2的实验。下列说法不正确的是
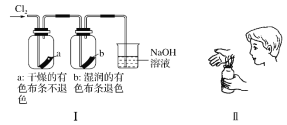
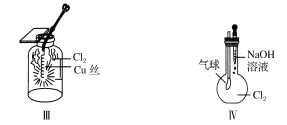
A. Ⅰ图中:实验现象证明氯气无漂白作用,氯水有漂白作用
B. Ⅱ图中:闻Cl2的气味
C. Ⅲ图中:生成棕黄色的烟
D. Ⅳ图中:若气球干瘪,证明Cl2可与NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生产Na2S2O5,通常是由NaHSO3过饱和溶液经结晶脱水制得。利用烟道气中的SO2生产Na2S2O5的工艺为:

下列说法正确的是( )
A.pH=4.1时,Ⅰ中为Na2SO3溶液
B.Na2S2O5用作食品的抗氧化剂和SO2作漂白剂时,均表现还原性
C.工艺中加入Na2CO3固体、并再次充入SO2的目的是得到NaHSO3过饱和溶液
D.葡萄酒中Na2S2O5用作食品的漂白剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】炼铁的反应原理为:Fe2O3+3CO![]() 3CO2+2Fe,当有2molFe生成时。下列说法中,错误的是( )
3CO2+2Fe,当有2molFe生成时。下列说法中,错误的是( )
A.参加反应的Fe2O3和CO物质的量分别为1mol、3mol
B.将生成67.2L标准状况下的CO2气体
C.参加反应的Fe2O3的质量为160g
D.参加反应的Fe2O3、CO与生成CO2的体积比为1:3:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】异丁烯与氯化氢可能发生的两种加成反应及相应的能量变化与反应过程如下图所示,下列说法错误的是( )


A.活化能:反应①大于反应②
B.中间产物的稳定性:中间体1小于中间体2
C.产物的能量:产物1大于产物2
D.△H大小:反应①小于反应②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)配平下列化学反应方程式,并用单线桥表示出电子转移的方向和数目。___。
3Cu+8HNO3![]() 3Cu(NO3)2+2NO↑+4H2O
3Cu(NO3)2+2NO↑+4H2O
(2)用KMnO4氧化盐制备氯气。反应方程式如下:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
此反应中氧化剂是__,氧化产物是__。若有1molKMnO4参加反应,转移电子的物质的量为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属镁在点燃条件下与二氧化碳反应:2Mg+CO2![]() 2MgO+C。当0.4mol Mg与0.1mol CO2充分反应后,物质的种类及其数量正确的是( )
2MgO+C。当0.4mol Mg与0.1mol CO2充分反应后,物质的种类及其数量正确的是( )
A.0.2 mol MgO + 0.1 molC
B.0.4 mol MgO + 0.2 molC
C.0.3 mol Mg + 0.2 mol MgO +0.1mol C
D.0.2 mol Mg + 0.2 mol MgO+0.1 molC
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,将3molA气体和1molB气体通入一容积固定为2L的密闭容器中,发生如下反应:3A(g)+B(g) ![]() xC(g),请填写下列空白:
xC(g),请填写下列空白:
(1)反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为_______;x为______。
(2)若反应经2min达到平衡,平衡时C的浓度______0.8mol/(填大于,小于或等于”)
(3)若已知达平衡时,该容器内混合气体总压强为P,混合气体起始压强为P0.请用P0、P来表示达平衡时反应物A的转化率a(A)为______%
(4)能够说明该反应达到平衡的标志是__________。
A .容器内混合气体的密度保持不变
B. v(A)=3v(B)
C .A、B的浓度之比为3:1
D .单位时间内消耗3n molA的同时生成n molB
E.体系的温度不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,下列说法正确的是
A.将pH均为a的氢氧化钠溶液和氨水分别加水稀释100倍,pH变为b和c,则a、b、c的大小关系是:a>b>c
B.KNO3溶液和CH3OOONH4溶液pH均为7,但两溶液中水的电离程度不相同
C.5.0×10-3 mol·L-1KHA溶液的pH=3.75,该溶液中c(A2-)<c(H2A)
D.己知某分散系中存在:M(OH)2(s)![]() M2+(aq)+2OH-(aq),K=a,c(M2+)=b mol·L-1时,溶液的pH等于
M2+(aq)+2OH-(aq),K=a,c(M2+)=b mol·L-1时,溶液的pH等于![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com