
Cu(OH)2在水溶液中存在着如下沉淀溶解平衡:Cu(OH)2(s)  Cu2+(aq)+2OH-(aq),在常温下Ksp=2×10-20。在常温下如果要生成Cu(OH)2沉淀,需要向0.02 mol/L的CuSO4溶液中加入碱溶液来调整溶液的pH,使溶液的pH大于
Cu2+(aq)+2OH-(aq),在常温下Ksp=2×10-20。在常温下如果要生成Cu(OH)2沉淀,需要向0.02 mol/L的CuSO4溶液中加入碱溶液来调整溶液的pH,使溶液的pH大于
( )
A.2 B.3
C.4 D.5
 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
现有浓度均为0.1 mol/L的下列溶液:
①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸铵、⑦硫酸氢铵、⑧氨水,请回答下列问题:
(1)①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)______________________。
(2)④、⑤、⑦、⑧四种溶液中NH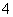 浓度由大到小的顺序是(填序号)________。
浓度由大到小的顺序是(填序号)________。
(3)将③和④等体积混合后,混合液中各离子浓度关系正确的是________。
A.c(Na+)=c(Cl-)>c(OH-)>c(NH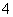 )
)
B.c(Na+)=0.1 mol/L
C.c(Na+)+c(NH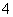 )=c(Cl-)+c(OH-)
)=c(Cl-)+c(OH-)
D.c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验方案设计中,可行的是
A.在水中加入氯化铁晶体,加热至沸腾,可得到氢氧化铁胶体
B.氢氧化铁胶体中的H+、Cl-可用过滤的方法除去
C.用蒸发的方法使NaCl从溶液中析出时,将蒸发皿中NaCl溶液全部加热蒸干
D.鉴别氯化铁溶液与氢氧化铁胶体较简便的方法是用激光束照射
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学学习小组为了解硫酸及其盐的某些性质和用途,进行了如下实验探究。
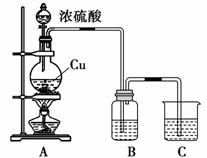
[实验一] 探究浓硫酸的氧化性:
(1)写出烧瓶中反应的化学方程式:____________________________________。
(2)B装置可用于探究SO2的还原性,则B中所用的试剂为:________________(任写一种即可);若B装置是品红溶液,则B中的现象是_______________________________。
[实验二] 检验(NH4)2Fe(SO4)2·6H2O中的金属离子:
(3)请结合化学用语和必要的文字说明如何检验出其中的金属离子(试剂、原理、现象等):______________________________________________________________________。
[实验三] 用KHSO4制取H2O2并测其质量分数:
查阅资料得知:工业上用如下原理制取H2O2:
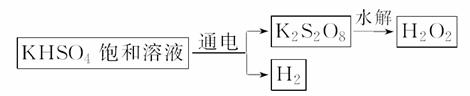
现用此法制取一定浓度的H2O2,并测定H2O2的质量分数。
已知:2MnO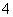 +5H2O2+6H+===2Mn2++8H2O+5O2↑
+5H2O2+6H+===2Mn2++8H2O+5O2↑
①取10.00 mL H2O2溶液(密度为1.00 g·mL-1)置于锥形瓶中加水稀释,并加稀硫酸酸化;
②用0.200 0 mol·L-1KMnO4溶液滴定;
③用同样方法滴定四次,消耗KMnO4溶液的体积分别为:40.00 mL、39.98 mL、42.02 mL、40.02 mL。
(4)用该原理制取H2O2的阳极电极反应式为_______________________________。
(5)进行操作②时,滴入第一滴KMnO4溶液,溶液的紫红色消失很慢,随着滴定的进行,溶液的紫红色消失速率加快,推测其原因可能是_____________________________。
(6)此H2O2溶液中溶质的质量分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
要使工业废水中的Pb2+沉淀,可用硫酸盐、碳酸盐、硫化物等作沉淀剂,已知Pb2+与这些离子形成的化合物的溶解度如下:
| 化合物 | PbSO4 | PbCO3 | PbS |
| 溶解度/g | 1.03×10-4 | 1.81×10-7 | 1.84×10-14 |
由上述数据可知,沉淀剂最好选用( )
A.硫化物 B.硫酸盐
C.碳酸盐 D.以上沉淀剂均可
查看答案和解析>>
科目:高中化学 来源: 题型:
已知常温下:Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.9×10-12,下列叙述正确 的是( )
的是( )
A.AgCl在饱和NaCl溶液中的Ksp和在纯水中的Ksp相同
B.向AgCl的悬浊液中加入NaBr溶液,白色沉淀转化为浅黄色,说明Ksp(AgCl)<Ksp(AgBr)
C.将0.001 mol/L的AgNO3溶液滴入0.001 mol/L的KCl和0.001 mol/L的K2CrO4溶液中先产生Ag2CrO4沉淀
D.向AgCl的悬浊液中滴加浓氨水,沉淀溶解,说明AgCl的溶解平衡向右移动
查看答案和解析>>
科目:高中化学 来源: 题型:
周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。回答下列问题;
(1)b、c、d中第一电离能最大的是________(填元素符号),e的价层电子轨道示意图为________。
(2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为______;分子中既含有极性共价键、又含有非极性共价键的化合物是________(填化学式,写出两种)。
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是________;酸根呈三角锥结构的酸是________。(填化学式)
(4)e和c形成的一种离子化合物的晶体结构如图(a),则e离子的电荷为________。
(5)这5种元素形成的一种1∶1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构[如图(b)所示]。
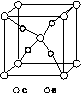
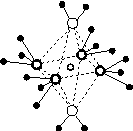
(a) (b)
该化合物中,阴离子为________,阳离子中存在的化学键类型有________;该化合物加热时首先失去的组分是________,判断理由是______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化合物中,含有非极性共价键的离子化合物是( )
A.CaC2 B.N2H4
C.Na2S2 D.NH4NO3
Ⅱ. [2013·海南卷] (14分)
图(a)所示的转化关系中(具体反应条件略),a、b、c和d分别为四种短周期元素的常见单质,其余均为它们的化合物,i的溶液为常见的酸。a的一种同素异形体的晶胞如图(b)所示。
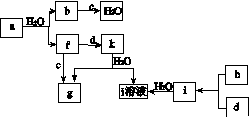
(a)

(b)
回答下列问题:
(1)图(b)对应的物质名称是________,其晶胞中的原子数为________,晶体的类型为________。
(2)d中元素的原子核外电子排布式为____________。
(3)图(a)中由二种元素组成的物质中,沸点最高的是________,原因是____________________,该物质的分子构型为________,中心原子的杂化轨道类型为________。
(4)图(a)中的双原子分子中,极性最大的分子是________。
(5)k的分子式为________,中心原子的杂化轨道类型为________,属于________分子(填“极性”或“非极性”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com