
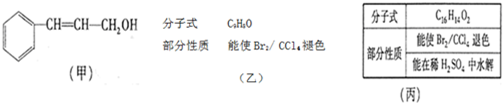
| 一定条件 |
| I |

| O2/Cu |
| △ |
| 一定条件 |
| Ⅱ |
| i.O3 |
| ii.Zn/H2O |
| i.浓NaOH |
| ii.H+ |

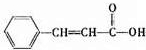 ,则C应为醇,因B为苯甲醛,则C为苯甲醇,E是相对分子质量为76,结合题给信息可知E应为OH-CH2-COOH,本身能发生缩聚反应生成
,则C应为醇,因B为苯甲醛,则C为苯甲醇,E是相对分子质量为76,结合题给信息可知E应为OH-CH2-COOH,本身能发生缩聚反应生成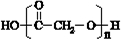 ,以此解答该题.
,以此解答该题.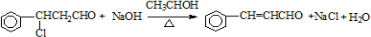 ,
,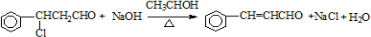 ;
;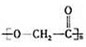 ,
,| 一定条件下 |
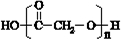 +(n-1)H2O,
+(n-1)H2O,| 一定条件下 |
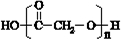 +(n-1)H2O;
+(n-1)H2O; ,故答案为:
,故答案为: ;
;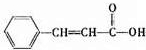 发生酯化反应生成丙,则丙为
发生酯化反应生成丙,则丙为 ,故答案为:
,故答案为: .
.


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、单质的熔、沸点逐渐降低 |
| B、卤素离子的还原性逐渐增强 |
| C、单质的氧化性逐渐增强 |
| D、气态氢化物的稳定性逐渐增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
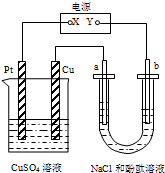 如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色,则
如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色,则查看答案和解析>>
科目:高中化学 来源: 题型:
| 13 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙醇、乙烯和植物油都能使酸性高锰酸钾褪色 |
| B、乙醇、乙烷、乙酸都可以与钠反应生成氢气 |
C、聚丙烯的结构简式为: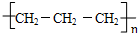 |
| D、用灼烧闻气味的方法可以区分纯棉织物和纯毛织物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 甘油的分离
甘油的分离查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com