
下列关于电解质溶液的叙述正确的是
A.常温下,pH=7的NH4Cl与氨水的混合溶液中离子浓度大小顺序为:
c (Cl-) > c (NH4+) > c (H+)> c (OH-)
B.将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低
C.中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同
D.常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大
科目:高中化学 来源: 题型:
1体积某气态烃和2体积氯化氢发生加成反应后,最多还能和6体积氯气发生取代反应。由此可以断定原气态烃是(气体体积均在相同条件下测定)( )
A.乙炔 B.丙炔 C.丁烯 D.丙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关Cl、N、S等非金属元素化合物的说法正确的是( )
A.漂白粉的成分为次氯酸钙
B.实验室可用浓硫酸干燥氨气
C.实验室可用NaOH溶液处理NO2和HCl废气
D.Al2(SO4)3可除去碱性废水及酸性废水中的悬浮颗粒
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实可用勒夏特列原理解释的是
A.使用催化剂有利于加快合成氨反应的反应速率
B.硫酸工业中,将黄铁矿粉碎后加入沸腾炉中
C.500℃左右比在室温时更有利于提高合成氨的转化率
D.配制氯化铁溶液时,将氯化铁加入盐酸中,然后加水稀释
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、M、N代表五种金属,有以下化学反应:
①水溶液中:X+Y2+===X2++Y;
②Z+2H2O(冷)===Z(OH)2+H2↑;
③M、N为电极与N盐溶液组成原电池,负极反应为:M-2e-===M2+;
④Y可以溶于稀H2SO4中,M不能被H2SO4氧化,则这五种金属的活动性由弱到强的顺序是
A.M<N<Y<X<Z B.N<M<Y<X<Z
C.N<M<X<Y<Z D.X<Z<N<M<Y
查看答案和解析>>
科目:高中化学 来源: 题型:
由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
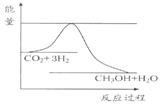 (1)关于该反应的下列说法中,其△H 0。(填“大于”、“小于”或“等于”), 且在 (填“较高”或“较低”)温度下有利于该反应自发进行。
(1)关于该反应的下列说法中,其△H 0。(填“大于”、“小于”或“等于”), 且在 (填“较高”或“较低”)温度下有利于该反应自发进行。
(2)该反应平衡常数K的表达式为 。
(3)温度降低,平衡常数K (填“增大”、“不变”或“减小”)。
(4)若为两个容积相同的密闭容器,现向甲容器中充入1 mol CO2(g)和3 molH2(g),乙容器中充入1mol CH3OH(g)和1 mol H2O(g),在相同的温度下进行反应,达到平衡时,甲容器内n(CH3OH) (填“大于”“小于”或“等于”)乙容器内n(CH3OH)。
(5)已知:CO(g)+2H2(g) = CH3OH (g) △H= -116 kJ•mol-1;CO(g)+1/2O2(g)=CO2(g)
△H=-283 kJ•mol-1 ;H2 (g)+1/2O2(g)=H2O(g) △H=-242 kJ•mol-1 ,写出CH3OH燃烧生成CO2和水蒸气的热化学方程式______________________________________。
(6)以甲醇和氧气为燃料,氢氧化钾溶液为电解质溶液构成电池。
①负极的电极反应式为 。
②若以石墨为电极,电解硫酸铜溶液,写出电解的总反应方程式 。若以此燃料电池电解200 mL 0.8mol/L的硫酸铜溶液,当消耗1.6甲醇时,在阴极会析出 g铜。
查看答案和解析>>
科目:高中化学 来源: 题型:
在强酸性溶液中,下列离子组能大量共存的是( )
A.Na+、Al3+、NO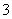 、Cl- B.K+、Na+、Cl-、AlO
、Cl- B.K+、Na+、Cl-、AlO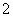
C.Fe2+、K+、NO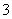 、Cl- D.Na+、HCO
、Cl- D.Na+、HCO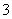 、K+、NO
、K+、NO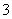
查看答案和解析>>
科目:高中化学 来源: 题型:
将一定量的晶体A,隔绝空气加热到200℃时,A全部分解为等物质的量的四种气体。这四种物质与其他的相互转化关系如下图所示。F和J是中学化学中常见的两种单质。H为红棕色气体。图中部分反应条件及生成物没有列出。请按要求填空:
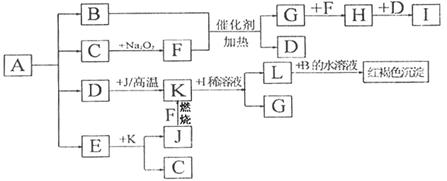
(1)单质F的化学式
(2)写出B和F反应的化学方程式 ,L和B的水溶液反应的离子方程式 ;
(3)写出K与I的稀溶液反应的离子方程式
(4)A的化学式为
(5)工业上以硫酸亚铁、稀硫酸和亚硝酸钠为原料来制备某高效净水剂Fe(OH)SO4,反应有G生成,该反应的化学方程式是
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是一些重要工业生产的转化关系(反应条件略去)。
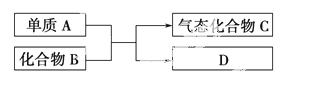
请完成下列问题:
(1)若D是单质,且与A属于同一主族,则:
①反应的化学方程式是_____________________________________________
_______________________________。
②D的原子结构示意图是________。
③D单质的一种重要用途是_________________________ _______________________________。
_______________________________。
(2)若B为黄色固体,D为固体化合物,则:
①该反应的化学方程式是 ___________________________________________________。
___________________________________________________。
②生产该工业品的工厂应建在离________较近的地方。
③实验室检验C的方法是______________________________________________________。
(3)若B是一种有刺激性气味的气体,则:
①B分子的空间构型为________。
②实验室进行此实验时,常看到有大量白烟 产生,产生大量白烟的原因是___________________________________________
产生,产生大量白烟的原因是___________________________________________ _________________。
_________________。
③化合物C在一定体积的容器中,在一定条件下发生反应,测得容器内气体的压强略小于原来的 。请写出该反应的化学方程式________________________________________________________。
。请写出该反应的化学方程式________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com