
| A. | 含氢量:苯>乙烯>甲烷 | |
| B. | 密度:H 2O>溴苯>苯 | |
| C. | 沸点:戊烷>2-甲基丁烷>2,2-二甲基丙烷 | |
| D. | 等质量的下列物质燃烧耗O 2量:乙炔>乙烯>乙烷 |
分析 A.根据C、H原子数目之比判断;
B.溴苯的密度大于水的;
C.烷烃同分异构体中,含有的支链越多,沸点越低;
D.等质量烃燃烧,H元素质量分数越大,耗氧量越大.
解答 解:A.苯、乙烯、甲烷中C、H原子数目之比分别为1:1、1:2、1:4,故含氢量:苯<乙烯<甲烷,故A错误;
B.密度为:溴苯>H 2O>苯,故B错误;
C.烷烃同分异构体中,含有的支链越多,沸点越低,则沸点:戊烷>2-甲基丁烷>2,2-二甲基丙烷,故C正确;
D.等质量烃燃烧,H元素质量分数越大,耗氧量越大,乙炔、乙烯、乙烷中C、H原子数目之比分别为1:1、1:2、1:3,含氢量为:乙炔<乙烯<乙烷,故耗氧量:乙炔<乙烯<乙烷,故D错误.
故选:C.
点评 本题考查化学式计算、有机物性质、熔沸点比较、烃燃烧有关计算等,比较基础,题目有利于基础知识的巩固.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
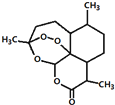
| A. | 用沸点只有35℃的乙醚作为溶剂来提取青蒿素的方法化学上叫萃取 | |
| B. | 能够发生水解反应 | |
| C. | 分子式为C15H23O5 | |
| D. | 青蒿素能够治疗疟疾可能与结构中存在过氧键或酯基等基团有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业上电解熔融的ZW制备Z单质 | |
| B. | 元素Y与Z形成的化合物中只能有一种化学键 | |
| C. | 离子半径大小顺序为W>X>Y>Z | |
| D. | 在一定条件下X的氢化物能与Y单质发生置换反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳碳键键长:乙烯>苯 | B. | 沸点:正戊烷>异戊烷 | ||
| C. | 相对密度: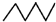 > >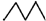 | D. | 水溶性:CH3CH2OH>CH3CH2Br |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
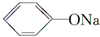 +CH3I→
+CH3I→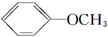 +NaI
+NaI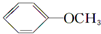 +HI→
+HI→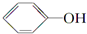 +CH3l
+CH3l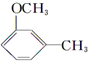 $\stackrel{KMnO_{4}(H+)}{→}$
$\stackrel{KMnO_{4}(H+)}{→}$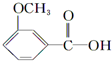
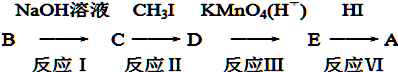
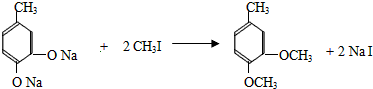 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
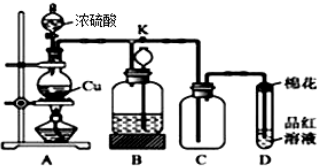
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol CH≡CH可以与Br2发生加成反应,消耗2 mol Br2 | |
| B. | 苯的邻位二元取代物只有一种可以说明苯分子不具有碳碳单键和碳碳双键的交替结构 | |
| C. | 2甲基戊烷的沸点高于己烷 | |
| D. | 用水可区分苯和溴苯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com