
”¾ĢāÄæ”æ»ÆŃ§Ę½ŗāŌĄķŹĒ֊ѧ»ÆѧѧĻ°µÄÖŲŅŖÄŚČŻ£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
¼×“¼ŹĒŅ»ÖÖæÉŌŁÉśÄÜŌ“£¬¾ßÓŠæŖ·¢ŗĶÓ¦ÓĆµÄ¹ćĄ«Ē°¾°£¬¹¤ŅµÉĻæÉÓĆŗĻ³ÉĘų£ØÖ÷ŅŖ³É·ÖCO”¢H2£©Öʱø¼×“¼”£
£Ø1£©¼ŗÖŖ£ŗCO”¢H2”¢CH3OH”¢µÄČ¼ÉÕČČ£Ø”÷H£©·Ö±šĪŖ-283.0kJ/mol”¢-241.8kJ/mol”¢-192.2 kJ/mol£¬ĒėŠ“³öŗĻ³ÉĘųÖʱø¼×“¼µÄČČ»Æѧ·½³ĢŹ½ ”£
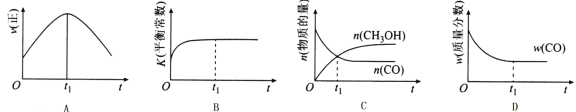
£Ø2£©ČōŌŚ¾ųČČ”¢ŗćČŻµÄĆܱÕČŻĘ÷ÖŠ³äČė1 mol CO”¢2 mol H2£¬·¢ÉśCO£Øg£©+2H2£Øg£©![]() CH3OH£Øg£©·“Ó¦£¬ĻĀĮŠŹ¾ŅāĶ¼ÕżČ·ĒŅÄÜĖµĆ÷·“Ó¦ŌŚ½ųŠŠµ½t1Ź±æĢĪŖĘ½ŗāדĢ¬µÄŹĒ______£ØĢīŃ”Ļī×ÖÄø£©”£
CH3OH£Øg£©·“Ó¦£¬ĻĀĮŠŹ¾ŅāĶ¼ÕżČ·ĒŅÄÜĖµĆ÷·“Ó¦ŌŚ½ųŠŠµ½t1Ź±æĢĪŖĘ½ŗāדĢ¬µÄŹĒ______£ØĢīŃ”Ļī×ÖÄø£©”£
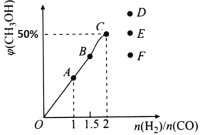
£Ø3£©ŌŚT1”ꏱ£¬ŌŚĢå»żĪŖ5 LµÄŗćČŻČŻĘ÷ÖŠ³äČė3 molµÄŗĻ³ÉĘų£¬·“Ó¦“ļµ½Ę½ŗāŹ±CH3OHµÄĢå»ż·ÖŹżÓėn£ØH2£©£Æn£ØCO£©µÄ¹ŲĻµČēĶ¼ĖłŹ¾”£H2ŗĶCO°“2:1Ķ¶ČėŹ±¾¹ż5 min“ļµ½Ę½ŗā£¬Ōņ5 minÄŚÓĆH2±ķŹ¾µÄ·“Ó¦ĖŁĀŹĪŖv£ØH2£©=_______”£ĪĀ¶Č²»±ä£¬µ±![]() Ź±£¬“ļµ½Ę½ŗāדĢ¬£¬CH3OHµÄĢå»ż·ÖŹżæÉÄÜŹĒĶ¼ĻóÖŠµÄ______µć”£
Ź±£¬“ļµ½Ę½ŗāדĢ¬£¬CH3OHµÄĢå»ż·ÖŹżæÉÄÜŹĒĶ¼ĻóÖŠµÄ______µć”£
£Ø4£©ŗ¬ÓŠ¼×“¼µÄ·ĻĖ®ĖęŅāÅÅ·Å»įŌģ³ÉĖ®ĪŪČ¾£¬æÉÓĆClO2½«ĘäŃõ»ÆĪŖCO2£¬Č»ŗóŌŁ¼Ó¼īÖŠŗĶ¼“æÉ”£Š“³ö“¦Ąķ¼×“¼ĖįŠŌ·ĻĖ®¹ż³ĢÖŠ£¬ClO2Óė¼×“¼·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ________________________”£
£Ø5£©Ė®µÄ×ŌżµēĄėæɱķŹ¾ĪŖH2O+H2O![]() H3O++OH-”£ÓėĖ®µēĄėĻąĖĘ£¬¼×“¼Ņ²ÄÜ·¢Éś×ŌżµēĄė£¬ĒėŠ“³ö¼×“¼µÄ×ŌżµēĄė·½³ĢŹ½_______________________________________£¬Ķł¼×“¼ÖŠ¼ÓČėÉŁĮ潚ŹōÄĘ·“Ӧɜ³É¼×“¼ÄĘ£¬Ōņ·“Ó¦ŗóµÄ»ģŗĻŅŗÖŠµÄµēŗÉŹŲŗćŹ½_____________________________”£
H3O++OH-”£ÓėĖ®µēĄėĻąĖĘ£¬¼×“¼Ņ²ÄÜ·¢Éś×ŌżµēĄė£¬ĒėŠ“³ö¼×“¼µÄ×ŌżµēĄė·½³ĢŹ½_______________________________________£¬Ķł¼×“¼ÖŠ¼ÓČėÉŁĮ潚ŹōÄĘ·“Ӧɜ³É¼×“¼ÄĘ£¬Ōņ·“Ó¦ŗóµÄ»ģŗĻŅŗÖŠµÄµēŗÉŹŲŗćŹ½_____________________________”£
”¾“š°ø”æ£Ø1£©CO£Øg£©+2H2£Øg£©![]() CH3OH£Øl£© ”÷H= -574.4kJ/mol £Ø3·Ö£© £Ø2£©D£Ø2·Ö£©
CH3OH£Øl£© ”÷H= -574.4kJ/mol £Ø3·Ö£© £Ø2£©D£Ø2·Ö£©
£Ø3£©0.06 molL-1min-1 £Ø2·Ö£©”¢F£Ø2·Ö£©
£Ø4£©6ClO2 +5CH3OH£½5CO2 +6Cl -+6H++7H2O£Ø2·Ö£©
£Ø5£©CH3OH+CH3OH![]() CH3OH2++CH3O -£Ø2·Ö£© c£ØCH3OH2+£©+ c£ØNa+£©£½c£ØCH3O -£©£Ø2·Ö£©
CH3OH2++CH3O -£Ø2·Ö£© c£ØCH3OH2+£©+ c£ØNa+£©£½c£ØCH3O -£©£Ø2·Ö£©
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗ£Ø1£©¼ŗÖŖ£ŗCO”¢H2”¢CH3OH”¢µÄČ¼ÉÕČČ£Ø”÷H£©·Ö±šĪŖ-283.0kJ/mol”¢-241.8kJ/mol”¢-192.2 kJ/mol£¬Ōņ¢ŁCO£Øg£©+1/2O2£Øg£©=CO2£Øg£©”÷H=-283.0kJmol-1
¢Ś2H2£Øg£© + O2£Øg£© = 2H2O£Øl£© ”÷H=£483.6kJ/mol
¢ŪCH3OH£Øl£©+3/2O2£Øg£©=CO2£Øg£©+2 H2O£Øl£©”÷H=-192.2kJmol-1
ÓÉøĒĖ¹¶ØĀÉæÉÖŖ¢Ł+¢Ś-¢ŪµĆ·“Ó¦CO£Øg£© + 2H2£Øg£©£½CH3OH£ØlµÄ”÷H£½£Ø-283-483.6+192.2£©kJmol-1£½£574.4kJ/mol”£
£Ø2£©A”¢µ½“ļĘ½ŗāŗóÕż”¢ÄęĖŁĀŹĻąµČ£¬²»ŌŁ±ä»Æ£¬¶ųt1Ź±æĢVÕż×ī“ó£¬Ö®ŗóĖŁĀŹ¼õŠ”£¬A“ķĪó£»B”¢øĆ·“Ó¦Õż·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬Ėę·“Ó¦½ųŠŠĪĀ¶ČÉżøߣ¬»ÆŃ§Ę½ŗā³£Źż¼õŠ”£¬µ½“ļĘ½ŗāŗó£¬ĪĀ¶ČĪŖ¶ØÖµ£¬“ļ×īøߣ¬Ę½ŗā³£Źż²»±ä£¬ĪŖ×īŠ”£¬Ķ¼ĻńÓėŹµ¼Ź·ūŗĻ£¬B“ķĪó£»C”¢t1Ź±æĢŗóŅ»Ńõ»ÆĢ¼”¢¼×“¼µÄĪļÖŹµÄĮæ·¢Éś±ä»Æ£¬t1Ź±æĢĪ“µ½“ļĘ½ŗāדĢ¬£¬C“ķĪó£»D”¢t1Ź±æĢ£¬COµÄÖŹĮæ·ÖŹżĪŖ¶ØÖµ£¬“¦ÓŚĘ½ŗāדĢ¬£¬Ķ¼ĻńÓėŹµ¼Ź·ūŗĻ£¬DÕżČ·£»“š°øŃ”D”£
£Ø3£©øł¾ŻĶ¼ĻńæÉÖŖH2ŗĶCO°“2:1Ķ¶ČėĘ½ŗāŹ±¼×“¼µÄŗ¬ĮæŹĒ0.5£¬Ōņøł¾Ż·½³ĢŹ½æÉÖŖ
CO£Øg£©+2H2£Øg£©![]() CH3OH£Øg£©
CH3OH£Øg£©
ĘšŹ¼Įæ£Ømol£© 1 2 0
Ę½ŗāĮæ£Ømol£© n 2n n
×Ŗ»ÆĮæ£Ømol£©1£n 2£2n n
Ņņ“ĖÓŠ![]()
½āµĆn£½0.75
ĖłŅŌ5 minÄŚÓĆH2±ķŹ¾µÄ·“Ó¦ĖŁĀŹĪŖ![]() £½0.06 molL-1min-1”£
£½0.06 molL-1min-1”£
ĪĀ¶Č²»±ä£¬µ±![]() Ź±ĒāĘųµÄĪļÖŹµÄĮæŌö¼Ó£¬COµÄ×Ŗ»ÆĀŹŌö“󣬵«ĒāĘųµÄ×Ŗ»ÆĀŹ¼õŠ”£¬Ņņ“Ė²śÉśµÄ¼×“¼µÄĪļÖŹµÄĮæ¼õŠ”£¬ĖłŅŌ“ļµ½Ę½ŗāדĢ¬Ź±CH3OHµÄĢå»ż·ÖŹż½µµĶ£¬Ņņ“ĖæÉÄÜŹĒĶ¼ĻóÖŠµÄFµć”£
Ź±ĒāĘųµÄĪļÖŹµÄĮæŌö¼Ó£¬COµÄ×Ŗ»ÆĀŹŌö“󣬵«ĒāĘųµÄ×Ŗ»ÆĀŹ¼õŠ”£¬Ņņ“Ė²śÉśµÄ¼×“¼µÄĪļÖŹµÄĮæ¼õŠ”£¬ĖłŅŌ“ļµ½Ę½ŗāדĢ¬Ź±CH3OHµÄĢå»ż·ÖŹż½µµĶ£¬Ņņ“ĖæÉÄÜŹĒĶ¼ĻóÖŠµÄFµć”£
£Ø4£©·“Ó¦ÖŠClŌŖĖŲ»ÆŗĻ¼Ū“Ó£«4¼Ū½µµĶµ½£1¼Ū£¬µĆµ½5øöµē×Ó”£Ģ¼ŌŖĖŲ»ÆŗĻ¼Ū“Ó£2¼ŪÉżøßµ½£«4¼Ū£¬Ź§Č„6øöµē×Ó£¬Ņņ“Ėøł¾Żµē×ӵƏ§ŹŲŗćæÉÖŖClO2Óė¼×“¼·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ6ClO2 +5CH3OH£½5CO2 +6Cl -+6H++7H2O”£
£Ø5£©øł¾ŻĖ®µÄ×ŌżµēĄėæɱķŹ¾ĪŖH2O+H2O![]() H3O++OH-æÉÖŖ¼×“¼µÄ×ŌżµēĄė·½³ĢŹ½ĪŖCH3OH£«CH3OH
H3O++OH-æÉÖŖ¼×“¼µÄ×ŌżµēĄė·½³ĢŹ½ĪŖCH3OH£«CH3OH![]() CH3OH2+£«CH3O -£¬Ķł¼×“¼ÖŠ¼ÓČėÉŁĮ潚ŹōÄĘ·“Ӧɜ³É¼×“¼ÄĘ£¬Ōņ·“Ó¦ŗóµÄ»ģŗĻŅŗÖŠµÄµēŗÉŹŲŗćŹ½ĪŖc£ØCH3OH2+£©+ c£ØNa+£©£½c£ØCH3O -£©”£
CH3OH2+£«CH3O -£¬Ķł¼×“¼ÖŠ¼ÓČėÉŁĮ潚ŹōÄĘ·“Ӧɜ³É¼×“¼ÄĘ£¬Ōņ·“Ó¦ŗóµÄ»ģŗĻŅŗÖŠµÄµēŗÉŹŲŗćŹ½ĪŖc£ØCH3OH2+£©+ c£ØNa+£©£½c£ØCH3O -£©”£


 »ĘøŌĢģĢģĮ·æŚĖćĢāæØĻµĮŠ“š°ø
»ĘøŌĢģĢģĮ·æŚĖćĢāæØĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æA”¢B”¢C”¢D”¢E”¢F”¢GĘßÖÖ¶ĢÖÜĘŚŌŖĖŲ£¬ĘäŌ×ÓŠņŹżŅĄ“ĪŌö“ó”£AµÄŌ×Ó֊ƻӊ³É¶Ōµē×Ó£»BµÄ»łĢ¬Ō×ÓÖŠµē×ÓÕ¼¾ŻČżÖÖÄÜĮæ²»Ķ¬µÄŌ×Ó¹ģµĄ£¬ĒŅĆæÖÖ¹ģµĄÖŠµÄµē×Ó×ÜŹżĻąĶ¬£»DŌ×Ó×īĶā²ćµē×ÓŹżŹĒÄŚ²ćµē×ÓŹżµÄ3±¶£»DÓėG“¦ŌŚĶ¬Ņ»×壻FŹĒµŲæĒÖŠŗ¬Įæ×īøߵĽšŹōŌŖĖŲ”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ŌŖĖŲFŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆ ”£
£Ø2£©B”¢C”¢DČżÖÖŌŖĖŲµÄµŚŅ»µēĄėÄÜÓɓ󵽊”µÄĖ³ŠņŹĒ £ØÓĆŌŖĖŲ·ūŗűķŹ¾£©”£
£Ø3£©ÅäŗĻĪļNi(BD)4³£ĪĀĻĀĪŖŅŗĢ¬£¬Ņ×ČÜÓŚCCl4”¢±½µČÓŠ»śČܼĮ£¬Ņņ“Ė¹ĢĢ¬Ni(BD)4ŹōÓŚ £ØĢī¾§ĢåĄąŠĶ£©”£
£Ø4£©CA3·Ö×ӵĵē×ÓŹ½ĪŖ ”£
£Ø5£©EDŹĒÓÅĮ¼µÄÄĶøßĪĀ²ÄĮĻ£¬Ę侧Ģå½į¹¹ÓėNaCl¾§ĢåĻąĖĘ”£EDµÄČŪµć±ČNaCløߣ¬ĘäŌŅņŹĒ ”£
£Ø6£©ÓÉA”¢D”¢GÖŠČĪĮ½ÖÖŌŖĖŲ¹¹³É¼×”¢ŅŅĮ½ÖÖ¾łŗ¬18øöµē×ӵķÖ×Ó£¬Ėłŗ¬Ō×ӵďżÄæŅĄ“ĪĪŖ3”¢4”£Ōņ¼×·Ö×ÓµÄÖŠŠÄŌ×Ó²ÉČ” Ōӻƣ»1 molŅŅ·Ö×Óŗ¬ÓŠ mol¦Ņ¼ü”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijŠ”×éŅŌCoCl2”¤6H2O”¢NH4Cl”¢H2O2”¢Ņŗ°±”¢ĀČ»Æļ§ĪŖŌĮĻ£¬ŌŚ»īŠŌĢæ“ß»ÆĻĀŗĻ³ÉĮĖ³Č»ĘÉ«¾§ĢåX”£ĪŖ²ā¶ØĘä×é³É£¬½ųŠŠČēĻĀŹµŃ锣
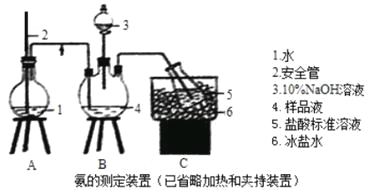
¢Ł°±µÄ²ā¶Ø£ŗ¾«Č·³ĘČ”wgX£¬¼ÓŹŹĮæĖ®Čܽā£¬×¢ČėČēĶ¼ĖłŹ¾µÄČż¾±ĘæÖŠ£¬Č»ŗóÖšµĪ¼ÓČė×ćĮæ10%NaOHČÜŅŗ£¬ĶØČėĖ®ÕōĘų£¬½«ŃłĘ·ČÜŅŗÖŠµÄ°±Č«²æÕō³ö£¬ÓĆV1mLc1mol”¤L”Ŗ1µÄŃĪĖįČÜŅŗĪüŹÕ”£Õō°±½įŹųŗóČ”ĻĀ½ÓŹÕĘ棬ÓĆc2mol”¤L”Ŗ1NaOH±ź×¼ČÜŅŗµĪ¶Ø¹żŹ£µÄHCl£¬µ½ÖÕµćŹ±ĻūŗÄV2mLNaOHČÜŅŗ”£
¢ŚĀČµÄ²ā¶Ø£ŗ×¼Č·³ĘȔѳʷX£¬Åä³ÉČÜŅŗŗóÓĆAgNO3±ź×¼ČÜŅŗµĪ¶Ø£¬K2CrO4ČÜŅŗĪŖÖøŹ¾¼Į£¬ÖĮ³öĻÖשŗģÉ«³Įµķ²»ŌŁĻūŹ§ĪŖÖÕµć£ØAg2CrO4ĪŖשŗģÉ«£©”£
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©×°ÖĆÖŠ°²Č«¹ÜµÄ×÷ÓĆŌĄķŹĒ ”£
£Ø2£©ÓĆNaOH±ź×¼ČÜŅŗµĪ¶Ø¹żŹ£µÄHClŹ±£¬Ó¦Ź¹ÓĆ Ź½µĪ¶Ø¹Ü£¬æÉŹ¹ÓƵÄÖøŹ¾¼ĮĪŖ ”£
£Ø3£©ŃłĘ·ÖŠ°±µÄÖŹĮæ·ÖŹż±ķ“ļŹ½ĪŖ ”£
£Ø4£©²ā¶Ø°±Ē°Ó¦øƶŌ×°ÖĆ½ųŠŠĘųĆÜŠŌ¼ģŃ飬ČōĘųĆÜŠŌ²»ŗĆ²ā¶Ø½į¹ū½« £ØĢī”°Ę«øß”±»ņ”°Ę«µĶ”±£©”£
£Ø5£©²ā¶ØĀČµÄ¹ż³ĢÖŠ£¬Ź¹ÓĆ×ŲÉ«µĪ¶Ø¹ÜµÄŌŅņŹĒ £»µĪ¶ØÖÕµćŹ±£¬ČōČÜŅŗÖŠc(Ag£«)=2.0”Į10”Ŗ5mol”¤L”Ŗ1£¬c(CrO42”Ŗ)ĪŖ mol”¤L”Ŗ1”££ØŅŃÖŖ£ŗKsp(Ag2CrO4)=1.12”Į10”Ŗ12£©
£Ø6£©¾²ā¶Ø£¬ŃłĘ·XÖŠīÜ”¢°±”¢ĀȵÄĪļÖŹµÄĮæÖ®±ČĪŖ1:6:3£¬īܵĻÆŗĻ¼ŪĪŖ £¬ÖʱøXµÄ»Æѧ·½³ĢŹ½ĪŖ £»XµÄÖʱø¹ż³ĢÖŠĪĀ¶Č²»ÄܹżøßµÄŌŅņŹĒ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀ±ķŹĒŌŖĖŲÖÜĘŚ±ķµÄŅ»²æ·Ö”£±ķÖŠĖłĮŠµÄ×ÖÄø·Ö±š“ś±ķijŅ»ÖÖ»ÆѧŌŖĖŲ”£
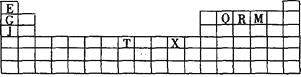

£Ø1£©Š“³ö»łĢ¬T3+µÄŗĖĶāµē×ÓÅŲ¼Ź½£ŗ £»TŌŚÖÜĘŚ±ķÖŠĖłŌŚ·ÖĒųĪŖ ”£
£Ø2£©Q”¢R”¢MµÄµŚŅ»µēĄėÄÜÓɓ󵽊”µÄĖ³ŠņŹĒ (ÓĆŌŖĖŲ·ūŗűķŹ¾)£¬ŌŅņ ”£
£Ø3£©ĻĀĮŠÓŠ¹ŲÉĻŹöŌŖĖŲµÄĖµ·ØÕżČ·µÄŹĒ ”£
A£®J±ČX»īĘĆ£¬ĖłŅŌJæÉŅŌŌŚČÜŅŗÖŠÖĆ»»³öX |
B£®½«J2M2ČÜÓŚĖ®£¬ŅŖĘĘ»µĄė×Ó¼üŗĶ¹²¼Ū¼ü |
C£®RE3·ŠµćøßÓŚQE4£¬Ö÷ŅŖŹĒŅņĪŖĒ°ÕßĻą¶Ō·Ö×ÓÖŹĮæ½Ļ“ó |
D£®Ņ»øöQ2E4·Ö×ÓÖŠŗ¬ÓŠĪåøö¦Ä¼üŗĶŅ»øö¦Š¼ü |
£Ø4£©G2OµÄČŪµć±ČJ2OµÄ £ØĢī”°øß”±»ņ”°µĶ”±£© £¬ĘäŌŅņŹĒ ”£
£Ø5£© GÓėRµ„ÖŹÖ±½Ó»ÆŗĻÉś³ÉŅ»ÖÖĄė×Ó»ÆŗĻĪļG3R”£øĆ¾§Ģå¾ßÓŠĄąĖĘŹÆÄ«µÄ²ćד½į¹¹”£Ćæ²ćÖŠ£¬GŌ×Ó¹¹³ÉĘ½ĆęĮł±ßŠĪ£¬ĆæøöĮł±ßŠĪµÄÖŠŠÄÓŠŅ»øöRŌ×Ó”£²ćÓė²ćÖ®¼ä»¹¼ŠŌÓŅ»¶ØŹżĮæµÄŌ×Ó”£ĒėĪŹÕāŠ©¼ŠŌÓµÄŌ×ÓÓ¦øĆŹĒ (ĢīG»ņRµÄŌŖĖŲ·ūŗÅ)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŠ»śĪļµÄ½į¹¹æÉÓĆ”°¼üĻߏ½”±¼ņ»Æ±ķŹ¾£¬ČēCH3-CH=CH-CH3æɼņŠ“ĪŖ![]() ”£ÓŠ»śĪļXµÄ¼üĻߏ½ĪŖ
”£ÓŠ»śĪļXµÄ¼üĻߏ½ĪŖ![]() £¬YŹĒXµÄĶ¬·ÖŅģ¹¹Ģ壬ĒŅŹōÓŚ·¼ĻćĢž”£ĻĀĮŠÓŠ¹ŲYµÄĖµ·ØÕżČ·µÄŹĒ( )
£¬YŹĒXµÄĶ¬·ÖŅģ¹¹Ģ壬ĒŅŹōÓŚ·¼ĻćĢž”£ĻĀĮŠÓŠ¹ŲYµÄĖµ·ØÕżČ·µÄŹĒ( )
A£®YÄÜŹ¹ĖįŠŌKMnO4ČÜŅŗĶŹÉ«£¬ĖłŅŌŹĒ±½µÄĶ¬ĻµĪļ
B£®YÄÜŹ¹äåĖ®ĶŹÉ«£¬ĒŅ¾²ÖĆŗó²»·Ö²ć
C£®Y²»ÄÜ·¢ÉśČ”“ś·“Ó¦
D£®YÄÜ·¢Éś¼Ó¾Ū·“Ӧɜ³É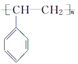
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潫ŹŹĮæAgBr¹ĢĢåČÜŌŚĖ®ÖŠ£¬ČÜŅŗÖŠ“ęŌŚAgBr(s)![]() Ag£«(aq)£«Br£(aq)”£ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
Ag£«(aq)£«Br£(aq)”£ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A£®Ļņ“ĖĢåĻµÖŠµĪ¼Ó×ćĮæÅØNaClČÜŅŗ£¬·¢ĻÖ³Įµķ×Ŗ»ÆĪŖ°×É«£¬ĖµĆ÷Ksp(AgCl)£¼Ksp(AgBr)
B£®Ä³ČÜŅŗÖŠc(Ag£«)”¤c(Br£)=Ksp(AgBr)£¬ĖµĆ÷“ĖŹ±c(Ag£«)=c(Br£)
C£®Ļņ“ĖĢåĻµÖŠ¼ÓČėÉŁĮæAgBr¹ĢĢå£¬Ę½ŗāÕżĻņŅĘ¶Æ£¬µ±ŌŁ“ĪĘ½ŗāŹ±c(Ag£«)”¢c(Br£)Ōö“ó
D£®“ĖĢåĻµÖŠŅ»¶Ø“ęŌŚc(Ag£«)=c(Br£)=[Ksp(AgBr)]1/2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
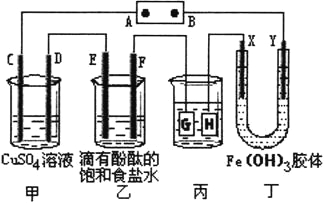
”¾ĢāÄæ”æČēĻĀĶ¼ĖłŹ¾£¬C”¢D”¢E”¢F”¢X”¢Y¶¼ŹĒ¶čŠŌµē¼«£¬¼×”¢ŅŅÖŠČÜŅŗµÄĢå»żŗĶÅØ¶Č¶¼ĻąĶ¬£Ø¼ŁÉčĶصēĒ°ŗóČÜŅŗĢå»ż²»±ä£©£¬A”¢BĪŖĶā½ÓÖ±Į÷µēŌ“µÄĮ½¼«”£½«Ö±Į÷µēŌ“½ÓĶØŗ󣬶”ÖŠX¼«ø½½üµÄŃÕÉ«Öš½„±äĒ³£¬Y¼«ø½½üµÄŃÕÉ«Öš½„±äÉī”£Ēė»Ų“š£ŗ
£Ø1£©Čō¼×”¢ŅŅ×°ÖĆÖŠµÄC”¢D”¢E”¢Fµē¼«¾łÖ»ÓŠŅ»ÖÖµ„ÖŹÉś³ÉŹ±£¬¶ŌÓ¦µ„ÖŹµÄĪļÖŹµÄĮæÖ®±ČĪŖ__________”£
£Ø2£©ĻÖÓƱū×°ÖĆøųĶ¼ž¶ĘŅų£¬µ±ŅŅÖŠČÜŅŗµÄpHŹĒ13Ź±£Ø“ĖŹ±ŅŅČÜŅŗĢå»żĪŖ500mL£©£¬±ūÖŠ¶Ę¼žÉĻĪö³öŅųµÄÖŹĮæĪŖ__________”£
£Ø3£©Fe(OH)3½ŗĢåµÄÖʱøÓŠŃĻøńµÄŅŖĒ󣬊”Ć÷ĻėĻņFeCl3ČÜŅŗÖŠµĪ¼ÓNaOHČÜŅŗĄ“ÖʱøFe(OH)3½ŗĢ壬½į¹ūŗÜæģ¾ĶÉś³ÉĮĖŗģŗÖÉ«µÄ³Įµķ”£Ėū²āµĆČÜŅŗµÄpH=5£¬Ōņ“ĖŹ±ČÜŅŗÖŠc(Fe3£«)=__________mol/L”££Ø¼ŗÖŖKsp[Fe(OH)3]=1”Į10£36£©”£
£Ø4£©ČōÓĆ¼×ĶéČ¼ĮĻµē³Ų£Øµē½āÖŹČÜŅŗĪŖ2L2mol/LKOHČÜŅŗ£©Ģį¹©µēŌ“£¬³ÖŠųĶØČė¼×Ķ飬ŌŚ±ź×¼×“æöĻĀ£¬Ļūŗļ×ĶéµÄĢå»żVL”£µ±ĻūŗÄCH4µÄĢå»żŌŚ44.8£¼V”Ü89.6Ź±£¬“ĖŹ±µēŌ“ÖŠB¼«·¢ÉśµÄµē¼«·“Ó¦ĪŖ£ŗ__________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøł¾ŻµāÓėĒāĘų·“Ó¦µÄČČ»Æѧ·½³ĢŹ½£ØµāĪŖĘųĢ¬»ņ¹ĢĢ¬£©£¬ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø £©
(¢”) I2(?)£«H2(g) ![]() 2HI(g) ”÷H£½-9.48 kJ/mol
2HI(g) ”÷H£½-9.48 kJ/mol
(¢¢) I2(?)£«H2(g) ![]() 2HI(g) ”÷H£½26.48 kJ/mol
2HI(g) ”÷H£½26.48 kJ/mol
A£®¢”ÖŠµāĪŖĘųĢ¬£¬¢¢ÖŠµāĪŖ¹ĢĢ¬
B£®·“Ó¦(¢”)µÄ²śĪļ±Č·“Ó¦(¢¢)µÄ²śĪļĪȶØ
C£®1 mol I2(g)ÖŠĶØČė1 mol H2(g)£¬·“Ó¦·ÅČČ9.48 kJ
D£®1 mol¹ĢĢ¬µāÓė1 molĘųĢ¬µāĖłŗ¬µÄÄÜĮæĻą²ī17.00 kJ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹµŃéŹŅÓĆĻĀĮŠŅĒĘ÷×é×°Ņ»Ģ×ÕōĮóŹÆÓĶµÄ×°ÖĆ£¬²¢½ųŠŠÕōĮóµĆµ½ĘūÓĶŗĶĆŗÓĶ”£
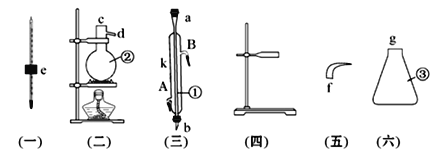
£Ø1£©Š“³öĻĀĮŠŅĒĘ÷µÄĆū³Ę£ŗ
¢Ł__________________£»¢Ś___________________£»¢Ū_________________”£
£Ø2£©½«ŅŌÉĻŅĒĘ÷°““Ó×óµ½ÓŅĖ³Šņ£¬ÓĆ×ÖÄøa”¢b”¢c””½ųŠŠĮ¬½Ó£ŗ
e½Ó__________£»_________½Ó_________£»_________½Ó_________
£Ø3£©¢ŁŅĒĘ÷µÄAæŚŹĒ__________£¬BæŚŹĒ__________”£
£Ø4£©ÕōĮóŹ±£¬ĪĀ¶Č¼ĘĖ®ŅųĒņÓ¦ŌŚ______________________£ØĪ»ÖĆ£©”£
£Ø5£©ŌŚ¢ŚÖŠ×¢ČėŌÓĶŗ󣬼ӼøʬĖé“ÉʬµÄÄæµÄŹĒ_________________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com