
| M��OH��n | Kap | pH | |
| ��ʼ���� | ������ȫ | ||
| Al��OH��3 | 1.9��10-23 | 3.43 | 4.19 |
| Fe��OH��3 | 3.8��10-38 | 2.53 | 2.94 |
| Ni��OH��2 | 1.6��10-14 | 7.60 | 9.75 |
| ||



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| M��OH��n | Ksp | ||
| pH | |||
| ��ʼ���� | ������ȫ | ||
| Al��OH��3 | 1.9��10-23 | 3.4 | 4.2 |
| Fe��OH��3 | 3.8��10-38 | 2.5 | 2.9 |
| Ni��OH��2 | 1.6��10-14 | 7.6 | 9.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013���Ĵ�ʡ�Ű���ѧ����1���¿���ѧ�Ծ����������� ���ͣ������
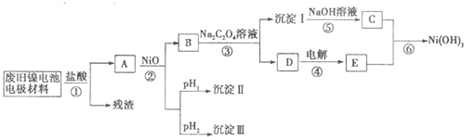
��12�֣�����ع㷺Ӧ���ڻ�϶�������ϵͳ���缫������Ni(OH)2��̼�ۡ���������Ϳ�����������Ƴɡ����ڵ��ʹ�ú�缫���϶Ի�����Σ����ij��ȤС��Ըõ�ص缫���Ͻ�����Դ�����о������ʵ���������£�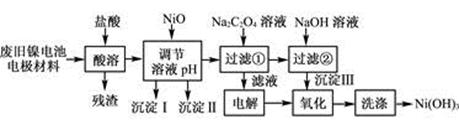
��֪����NiCl2������ˮ��Fe3����������Ni2����
����֪ʵ���¶�ʱ���ܽ�ȣ�NiC2O4��NiC2O4��H2O��NiC2O4��2H2O
��ij�¶���һЩ�������������Ksp����������������pH���±���ʾ��
| M(OH)n | Ksp | ��ʼ����pH | ������ȫpH |
| Al(OH)3 | 1.9��10��23 | 3.4 | 4.2 |
| Fe(OH)3 | 3.8��10��38 | 2.5 | 2.9 |
| Ni(OH)2 | 1.6��10��14 | 7.6 | 9.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ���Ĵ�ʡ����1���¿���ѧ�Ծ��������棩 ���ͣ������
��12�֣�����ع㷺Ӧ���ڻ�϶�������ϵͳ���缫������Ni(OH)2��̼�ۡ���������Ϳ�����������Ƴɡ����ڵ��ʹ�ú�缫���϶Ի�����Σ����ij��ȤС��Ըõ�ص缫���Ͻ�����Դ�����о������ʵ���������£�
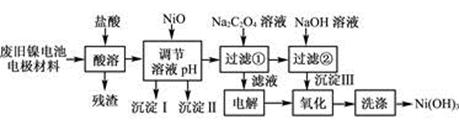
��֪����NiCl2������ˮ��Fe3����������Ni2����
����֪ʵ���¶�ʱ���ܽ�ȣ�NiC2O4��NiC2O4��H2O��NiC2O4��2H2O
��ij�¶���һЩ�������������Ksp����������������pH���±���ʾ��
|
M(OH)n |
Ksp |
��ʼ����pH |
������ȫpH |
|
Al(OH)3 |
1.9��10��23 |
3.4 |
4.2 |
|
Fe(OH)3 |
3.8��10��38 |
2.5 |
2.9 |
|
Ni(OH)2 |
1.6��10��14 |
7.6 |
9.8 |
�ش��������⣺
(1) ��NiO������Һ��pH����������������________�ͳ�����__________(�ѧʽ)��
(2) д������Na2C2O4��Һ�ķ�Ӧ�Ļ�ѧ����ʽ��
��
(3) ��������Һʱ��������������ķ�����
��
(4) д������������Ӧ�����ӷ���ʽ��
��
(5) ��μ���Ni(OH)3��ϴ�Ӹɾ���
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010-2011ѧ�꽭��ʡ�Ͼ��и������Ĵ�ģ�⿼�ԣ����ۣ���ѧ���� ���ͣ�ʵ����
����ع㷺Ӧ���ڻ�϶�������ϵͳ���缫������Ni(OH)2��̼�ۡ���������Ϳ�����������Ƴɡ����ڵ��ʹ�ú�缫���϶Ի�����Σ����ij��ȤС��Ըõ�ص缫���Ͻ�����Դ�����о������ʵ���������£�

��֪����NiCl2������ˮ��Fe3����������Ni2����
����֪ʵ���¶�ʱ���ܽ�ȣ�NiC2O4��NiC2O4��H2O��NiC2O4��2H2O
��ij�¶���һЩ�������������Ksp����������������pH���±���ʾ��
|
M(OH)n |
Ksp |
|
|
|
pH |
|
|
|
|
��ʼ���� |
������ȫ |
|
|
|
Al(OH)3 |
1.9��10��23 |
3.4 |
4.2 |
|
Fe(OH)3 |
3.8��10��38 |
2.5 |
2.9 |
|
Ni(OH)2 |
1.6��10��14 |
7.6 |
9.8 |
�ش��������⣺
(1) ��NiO������Һ��pH����������������________�ͳ�����__________(�ѧʽ)��
(2) д������Na2C2O4��Һ�ķ�Ӧ�Ļ�ѧ����ʽ������
(3) ��������Һʱ��������������ķ���������
(4) д������������Ӧ�����ӷ���ʽ������
(5) ��μ���Ni(OH)3��ϴ�Ӹɾ�������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com