
化合物G的合成路线如下:
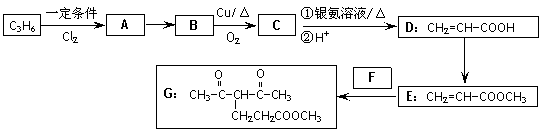 |
(1)D中含氧官能团的名称为 ,1 mol G发生加成反应最多消耗 mol H2
(2)除掉E中含有少量D的试剂和操作是 ;下列有关E的说法正确的是 (填字母序号)。
A.可发生氧化反应
B.催化条件下可发生缩聚反应
C.可发生取代反应
D.是CH2=CHCOOCH2CH3的同系物
E.易溶于水
(3)写出A→B的化学反应方程式 。
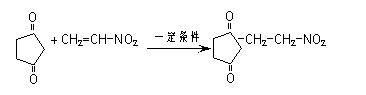 (4)反应E + F→ G属于下列麦克尔加成反应类型,则F的结构简式为 。
(4)反应E + F→ G属于下列麦克尔加成反应类型,则F的结构简式为 。
(5)比G少2个氢原子的物质具有下列性质:①遇FeCl3溶液显紫色;②苯环上的一氯取代物只有一种;③1mol物质最多可消耗2mol Na和1mol NaOH。任写一种该物质的结构简式 。
科目:高中化学 来源: 题型:
在一个固定容积的密闭容器中,可逆反应:mA(g)+nB(g)  pC(g)+qD(g)中,当m、n、p、q为任意正整数时,达到平衡的标志是( )
pC(g)+qD(g)中,当m、n、p、q为任意正整数时,达到平衡的标志是( )
A.体系压强不再发生变化
B.反应速率vA∶vB∶vC∶vD=m∶n∶p∶q
C容器内气体的密度不再改变
D. 各组分的物质的量浓度不再改变
查看答案和解析>>
科目:高中化学 来源: 题型:
美国科学家发现:普通盐水在无线电波照射下可燃烧,这一伟大的发现,有望解决用水作人类能源的重大问题。无线电频率可以降低盐水中所含元素之间的“结合力”,释放出氢原子,若点火,氢原子就会在该种频率下持续燃烧。上述中“结合力”实质是( )
A.分子间作用力 B.氢键 C.共价键 D.离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
在450℃并有催化剂存在下,在体积为1L的密闭恒温容器中,二氧化硫和氧气发生如下反应:2SO2+ O2 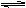
 2SO3
2SO3
(1)已知:64g SO2完全转化为SO3会放出85kJ热量。
SO2转化为SO3的热化学方程式是 。
 (2)该反应的化学平衡常数表达式K= 。
(2)该反应的化学平衡常数表达式K= 。
(3)降低温度,化学反应速度 。该反应K值将 。
压强将 。(填“增大”或“减小”或“不变”)
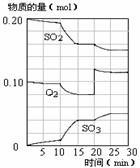
(4)450℃时,在一密闭容器中,将二氧化硫与氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态的时间段是 。
a.10-15min b.15-20min c.20-25min d.25-30min
(5)据图判断,10min到15min的曲线变化的原因可能是 (填写编号)。
a.增加SO3的物质的量 b.缩小容器体积 c.降低温度 d.催化剂
(6)在15分钟时,SO2的转化率是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
W、X、Y、Z是短周期元素,其部分性质如下表
| W | 单质是淡黄色固体 |
| X | 在地壳中的含量居第二位 |
| Y | 原子最外层电子数是电子总数的2/3 |
| Z | 第三周期原子半径最小的金属 |
下列说法正确的是
A.气态氢化物的热稳定性:X>W
B.最高价氧化物对应水化物的酸性:Y>X
C.离子半径:Z>W
D.Z的氧化物中含有非极性共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
碳酸钙和硫酸钙都是钙的重要化合物,它们在生产生活中都有着广泛的应用。甲、乙两组同学分别对碳酸钙的制备、硫酸钙的性质进行了以下探究,请你参与并完成对有关问题的解答。
(1)甲组使用大理石(含少量的Fe2O3杂质)等物质制备碳酸钙的实验流程如下:
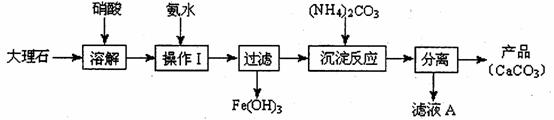
①溶解大理石时,用硝酸而不用硫酸的原因是 。
②上述流程中,“分离”得产品所包含的实验操作依次为:过滤、 、 。
③“滤液A”中除H+离子外,还含有的阳离子是 ;检验该阳离子的实验方法是:取少量滤液A与 在试管中混合、加热充分反应,将湿润的红色石蕊试纸(或pH试纸)靠近试管口,观察现象即可。
(2)乙组对某硫酸钙晶体(xCaS04·yH20)加热分解的有关反应进行探究。他们取6.52g该晶体进行加热,加热过程中,固体质量随时间的变化情况如下图所示。又知t5~t6时间段内固体质量减轻的原因是产生了两种气体,反应的化学方程式为:
 2CasO4 2CaO+2S02↑+O2↑。
2CasO4 2CaO+2S02↑+O2↑。
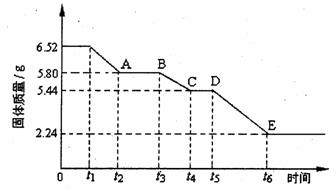
①加热时,该晶体开始发生化学变化的时间是 (填“t1”、“t3”或“t5”)。
②t4~t5时间段固体的化学式为 。
③tl~t2时间段固体发生反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学用语使用正确的是( )
A. 硫原子的原子结构示意图:
B.NH4Cl的电子式: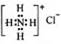
C.原子核内有10个中子的氧原子:
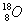
D.纯碱的化学式为NaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com