
儿茶素(其结构简式如图所示)是茶叶的主要活性成分,具有抗氧化、抗菌、除臭等作用。下列说法正确的是

A.常温下,儿茶素不溶于水,也不溶于有机溶剂
B.儿茶素能与FeCl3溶液发生显色反应
C.1mol儿茶素最多可与10mol NaOH反应
D.儿茶素一定不能发生水解反应
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
CaCO3广泛存在于自然界,是一种重要的化工原料。大理石主要成分为CaCO3,另外有少量的含硫化合物。实验室用大理石和稀盐酸反应制备CO2气体。下列装置可用于CO2气体的提纯和干燥。
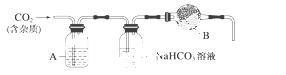
完成下列填空:
(1)用浓盐酸配制1∶1(体积比)的稀盐酸(约6 mol·L-1),应选用的仪器是_________。
a.烧杯 b.玻璃棒 c.量筒 d.容量瓶
(2)上述装置中,A是____________,NaHCO3溶液可以吸收________。
(3)上述装置中,B物质是__________。用这个实验得到的气体测定CO2的分子量,如果B物质失效,测定结果________(填“偏高”、“偏低”或“不受影响”)。
(4)一次性饭盒中石蜡(高级烷烃)和CaCO3在食物中的溶出量是评价饭盒质量的指标之一,测定溶出量的主要实验步骤设计如下:
剪碎、称重→浸泡溶解→过滤→残渣烘干→冷却、称重→恒重
为了将石蜡和碳酸钙溶出,应选用的试剂是__________。
a.氯化钠溶液 b.稀醋酸 c.稀硫酸 d.正己烷
(5)在溶出量测定实验中,为了获得石蜡和碳酸钙的最大溶出量,应先溶出________,后溶出_______。
(6)上述测定实验中,连续__________,说明样品已经恒重。
查看答案和解析>>
科目:高中化学 来源: 题型:
洪水过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。
(1)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为___________________。
(2)漂白粉的有效成分是(填名称)________。
(3)漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,反应的离子方程式为______________________________。
(4)反应(1)和反应(3)中,属于氧化还原反应的是(填编号)________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下图所示是验证氯气性质的 微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
已知:2KMnO4+16HCl—→2KCl+5Cl2↑+2MnCl2+8H2O

对实验现象的“解释或结论”正确的是 ( )
| 选项 | 实验现象 | 解释或结论 |
| A | a处变蓝,b处变红棕色 | 氧化性:Cl2>Br2>I2 |
| B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
| C | d处立即褪色 | 氯气与水生成了漂白性物质 |
| D | e处变红色 | 还原性:Fe2+>Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知: ,从A出发发生图示中的一系列反应,其中B和C按1:2反应生成Z,F和E按1:2反应生成W,W和Z互为同分异构体。
,从A出发发生图示中的一系列反应,其中B和C按1:2反应生成Z,F和E按1:2反应生成W,W和Z互为同分异构体。

回答下列问题:
(1)写出反应类型:①_____________________,②______________________________。
(2)写出下列反应的化学方程式:
③_____________________________________________________;
④_____________________________________________________。
(3)与B互为同分异构体,属于酚类且苯环上只有两个互为对位取代基的化合物有4种,其结构简式为_______________,_________________,_______________,______________。
(4)A的结构简式可能为_______________________________________(只写一种即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【化学卷·2015届浙江省嘉兴市高三上学期学科基础测试(201409)】8. 下列说法正确的是
A.石油裂解的目的是为了提高汽油等轻质油的产量和质量
B.等质量的葡萄糖和淀粉燃烧消耗的氧气量相等
C.用溴水可鉴别乙醇、环已烯和甲苯
D.分别用乙烷和乙烯制备氯乙烷的反应类型完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
研究下表信息可直接得出的结论是 ( )
| 元素 | F | Cl | Br | I |
| 氢化物组成 | HF | HCl | HBr | HI |
| 氢化物形成难 易程度 | H2、F2混合,冷暗处剧烈化合并发生爆炸 | H2、Cl2混合,光照或点燃时发生爆炸 |
| H2、I2混合,加热化合,同时又分解 |
| 氢化物热稳定性 | 很稳定 | 稳定 | 较稳定 | 较不稳定 |
A.元素性 质随原子序数的递增而呈周期性变化
质随原子序数的递增而呈周期性变化
B.同周期元素的非金属性随原子序数递增而增强
C.第ⅦA族元素的金属性随电子层数增加而减弱
D.第ⅦA族元素的非金属性随电子层数增加而减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
I、某实验小组同学为了探究铜与浓硫酸的反应,进行了如下系列实验,实验装置如图所示:
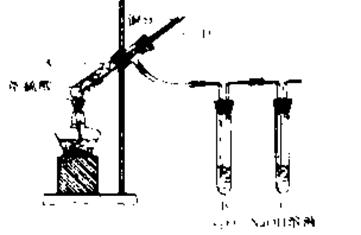
实验步骤:
①先连接好装置,检查气密性,加入试剂;
②加热A试管直到B中品红褪色,熄灭酒精灯;
③将Cu丝上提离开液面。
(1)装置A中发生反应的化学方程式为____________________.
(2)拆除装置前,不需打开胶塞,就可使装置中残留气体完全被吸收,应当采取的操作是_________________.
(3)若将B中品红溶液换成溴水,通入一段时间后溴水褪色,这说明了二氧化硫具有漂白性,你是否同意这个观点___________,(填“同意”或“不同意”),说明理由_________(用离子方程式表示)。
II、以浓硫酸、浓硝酸、粗铜、水和空气为原料可制得硫酸铜晶体。其过程如下图所示。

回答下列问题:
(4)配平在滤液(III)中发生反应的化学方程式:
_____NOx+____H2O+___O2=____HNO3
(5)写出制取硫酸铜的总反应方程式:_______________________.
(6)在上述生产过程中,被循环使用的物质是________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com