
”¾ĢāÄæ”æ×é³ÉÓńĆ×ŗĶČĖĢåĻø°ūÖŠ×ī»ł±¾µÄŌŖĖŲŹĒ
A.Ģ¼B.ĒāC.ŃõD.µŖ
”¾“š°ø”æA
”¾½āĪö”æ
×é³ÉĻø°ūµÄ“óĮæŌŖĖŲÓŠ£ŗC”¢H”¢O”¢N”¢P”¢S”¢K”¢Ca”¢Mg£¬ĘäÖŠC”¢H”¢O”¢NŹĒ×é³ÉĻø°ūµÄ»ł±¾ŌŖĖŲ£¬CŹĒ×é³ÉĻø°ūµÄ×ī»ł±¾ŌŖĖŲ£¬ŅņĪŖĢ¼Į“ŹĒ¹¹³ÉÉśĪļ“ó·Ö×ӵĻł±¾¹Ē¼Ü”£
“óĮæŌŖĖŲŹĒÖøŗ¬ĮæÕ¼ÉśĪļ×ÜÖŲĮæĶņ·ÖÖ®Ņ»ŅŌÉĻµÄŌŖĖŲ£¬°üĄØC”¢H”¢O”¢N”¢P”¢S”¢K”¢Ca”¢Mg£¬ĘäÖŠC”¢H”¢O”¢NĪŖ»ł±¾ŌŖĖŲ£¬CĪŖ×ī»ł±¾ŌŖĖŲ£¬OŹĒŗ¬Įæ×ī¶ąµÄŌŖĖŲ”£
¹ŹŃ”A”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚĀČĖ®ÖŠ“ęŌŚ¶ąÖÖ·Ö×ÓŗĶĄė×Ó£¬ĖüĆĒŌŚ²»Ķ¬µÄ·“Ó¦ÖŠ±ķĻÖ³öø÷×ŌµÄŠŌÖŹ”£ĻĀĮŠŹµŃéĻÖĻóŗĶ½įĀŪŅ»ÖĀĒŅÕżČ·µÄŹĒ£Ø £©
A. ¼ÓČėÓŠÉ«²¼Ģõ£¬Ņ»»į¶łÓŠÉ«²¼ĢõĶŹÉ«£¬ĖµĆ÷ČÜŅŗÖŠÓŠCl2“ęŌŚ
B. ČÜŅŗ³ŹĒ³»ĘĀĢÉ«£¬ĒŅÓŠ“Ģ¼¤ŠŌĘųĪ¶£¬ĖµĆ÷ÓŠCl2·Ö×Ó“ęŌŚ
C. ÓĆŃĪĖįĖį»Æŗ󣬵ĪČėAgNO3ČÜŅŗ²śÉś°×É«³Įµķ£¬ĖµĆ÷ĀČĖ®ÖŠÓŠCl-“ęŌŚ
D. ¼ÓČėNaOHČÜŅŗ£¬ĀČĖ®»ĘĀĢÉ«ĻūŹ§£¬ĖµĆ÷ÓŠHClO·Ö×Ó“ęŌŚ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æR2O82£Ąė×ÓŌŚŅ»¶ØĢõ¼žĻĀæÉŅŌ°ŃMn2+Ąė×ÓŃõ»Æ£¬Čō·“Ó¦ŗóR2O82£Ąė×Ó±äĪŖRO42£Ąė×Ó£¬ÓÖÖŖ·“Ó¦ÖŠŃõ»Æ¼ĮŗĶ»¹Ō¼ĮµÄĪļÖŹµÄĮæÖ®±ČĪŖ5©U2£¬Mn2+Ąė×Ó±»Ńõ»ÆŗóµÄ»ÆŗĻ¼ŪĪŖ
A. 4 B. 5 C. 6 D. 7
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻÖÓŠĪåÖÖĪļÖŹA”¢B”¢C”¢D”¢E,ĘäÖŠÓŠŅ»ÖÖŹĒ¼ī,ĖÄÖÖŹĒŃĪ,ČÜÓŚĖ®ŗóµēĄėæÉŅŌ²śÉśĻĀ±ķÖŠµÄĄė×Ó:
ŃōĄė×Ó | Na+””H+””Ba2+ |
ŅõĄė×Ó | OH-”” CO32-””SO42- |
ĪŖ¼ų±šĖüĆĒ,·Ö±šĶź³ÉŅŌĻĀŹµŃé,Ęä½į¹ūČēĻĀ:
¢ŁAČÜŅŗÓėBČÜŅŗ·“Ӧɜ³ÉĪŽÉ«ĘųĢåX,ĘųĢåXæÉŅŌÓėCČÜŅŗ·“Ӧɜ³É³ĮµķE,³ĮµķEæÉÓėBČÜŅŗ·“Ó¦;
¢ŚBČÜŅŗÓėCČÜŅŗ·“Ӧɜ³É°×É«³ĮµķD,³ĮµķD²»ČÜÓŚĻ”ĻõĖį”£
Ēėøł¾ŻÉĻŹöŹµŃé½į¹ū,ĢīæÕ:
(1)Š“³öĪļÖŹµÄ»ÆѧŹ½:A______ X______”£
(2) BČÜÓŚĖ®ŗóµÄµēĄė·½³ĢŹ½ĪŖ______________________”£
¼ų±šBÖŠŅõĄė×ӵďµŃé²Ł×÷·½·ØŹĒ_____________________”£
(3)Š“³ö AČÜŅŗÓėBČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½:
________________________________________________________________________ӣ
(4)DÓėEµÄ»ģŗĻĪļa g,¼ÓČė×ćĮæŃĪĖį,·“Ó¦Ķź±ĻÉś³É±ź×¼×“æöĻĀµÄĘųĢåb L,ŌņDŌŚ»ģŗĻĪļÖŠµÄÖŹĮæ·ÖŹżĪŖ________”££ØĮŠ³öĖćŹ½¼“æÉ£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻņĢå»ż¾łĪŖ10 mL”¢ĪļÖŹµÄĮæÅضČĻąĶ¬µÄĮ½·ŻNaOH ČÜŅŗÖŠ·Ö±šĶØČėŅ»¶ØĮæµÄCO2£¬µĆµ½ČÜŅŗ¼×ŗĶŅŅ”£Ļņ¼×”¢ŅŅĮ½ČÜŅŗÖŠ·Ö±šµĪ¼Ó0.1mol/LµÄŃĪĖį£¬“ĖŹ±·“Ӧɜ³ÉCO2Ģå»ż(±ź×¼×“æö)ÓėĖł¼ÓŃĪĖįĢå»żµÄ¹ŲĻµČēĶ¼ĖłŹ¾”£ŌņĻĀĮŠŠšŹöÖŠ²»ÕżČ·µÄŹĒ

A. ŌNaOHČÜŅŗµÄĪļÖŹµÄĮæÅضČĪŖ0.5 mol/L
B. µ±0ŃĪĖį)<10 mLŹ±£¬¼×ČÜŅŗÖŠ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖH++CO32-=HCO3-
C. ŅŅČÜŅŗÖŠŗ¬ÓŠµÄČÜÖŹŹĒNa2CO3”¢NaOH
D. ĻņŅŅČÜŅŗÖŠµĪ¼Ó¹żĮæŃĪĖįŗó²śÉśCO2Ģå»żµÄ×ī“óÖµĪŖ224 mL
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ·Ö×ÓŹ½ĪŖC5H12µÄĶéĢžŅ»¹²ÓŠ¶ąÉŁÖÖĶ¬·ÖŅģ¹¹Ģå£Ø””””£©
A.2
B.3
C.4
D.5
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æX”¢Y”¢Z”¢WŹĒŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄĖÄÖÖ¶ĢÖÜĘŚŌŖĖŲ£¬A”¢B”¢C”¢D”¢FŹĒÓÉĘäÖŠµÄĮ½ÖÖ»ņČżÖÖŌŖĖŲ×é³ÉµÄ»ÆŗĻĪļ£¬EŹĒÓÉZŌŖĖŲŠĪ³ÉµÄµ„ÖŹ£¬0.1molL-1 DČÜŅŗµÄpHĪŖ13£Ø25”ę£©”£ĖüĆĒĀś×ćČēĶ¼×Ŗ»Æ¹ŲĻµ£¬ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ

A. ÓÉX”¢Y”¢Z”¢WĖÄÖÖŌŖĖŲ×é³ÉµÄŃĪČÜŅŗpHŠ”ÓŚ7
B. »ÆŗĻĪļFÖŠŗ¬ÓŠ¹²¼Ū¼üŗĶĄė×Ó¼ü
C. 0.1molBÓė×ćĮæCĶźČ«·“Ó¦¹²×ŖŅʵē×ÓŹżĪŖ0.2NA
D. ZŌŖĖŲµÄ×īøßÕż¼ŪĪŖ£«6
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æNaClO2¹ć·ŗÓĆÓŚŌģÖ½¹¤Ņµ”¢ĪŪĖ®“¦ĄķµČ£¬ĘäĘÆ°×ÄÜĮ¦ŹĒĘÆ°×·ŪµÄ4”«5±¶£¬¹¤ŅµÉĻÓĆC1O2ĘųĢåÖĘNaClO2µÄ¹¤ŅÕĮ÷³ĢČēĻĀ£ŗ

¼ŗÖŖ£ŗNaClO2±„ŗĶČÜŅŗŌŚµĶÓŚ38”ꏱĪö³öNaC1O2”¤3H2O£¬øßÓŚ38”ꏱĪö³öNaClO2
ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A. ĪüŹÕĘ÷ÖŠÉś³ÉNaClO2µÄĄė×Ó·½³ĢŹ½£ŗ2ClO2+2OH-+H2O2=2ClO2-+O2+2H2O
B. Į÷³ĢÖŠµÄ½į¾§”¢¹żĀĖ²Ł×÷Ó¦øĆŹĒÕō·¢½į¾§”¢³ĆČČ¹żĀĖ
C. ĢįøßĪüŹÕĘ÷ÖŠµÄ·“Ó¦ĪĀ¶ČæÉŅŌĢįøß·“Ó¦ĖŁĀŹ£¬Ņ²Ģįøß·“Ó¦ĪļµÄĄūÓĆĀŹ
D. ·¢ÉśĘ÷ÖŠ·“Ó¦½įŹųŗó£¬ĻņĘäÖŠĶØČėŅ»¶ØĮææÕĘųµÄÄæµÄŹĒĒżøĻ³öClO2£¬Ź¹Ęä±»³ä·ÖĪüŹÕ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅĄ¾ŻĶ¼1ÖŠµŖŌŖĖŲ¼°Ęä»ÆŗĻĪļµÄ×Ŗ»Æ¹ŲĻµ£¬»Ų“šĪŹĢā£ŗ
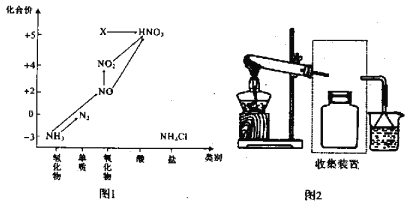
£Ø1£©ŹµŃéŹŅ³£ÓĆNH4ClÓėCa(OH)2ÖĘČ”°±Ęų£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ____________________”£
£Ø2£©ČōŅŖŹÕ¼ÆŅ»Ęæ°±Ęų£¬Ēė½«ĻĀĮŠ×°ÖĆ²¹³äĶźÕū£¬ŌŚĶ¼2ŠéæņÄŚ»³öĮ¬½ÓĶ¼”£____________
£Ø3£©ĻĀĮŠŹŌ¼ĮæÉÓĆÓŚøÉŌļNH3µÄŹĒ________________________________”£
A.ÅØĮņĖį B.¼īŹÆ»Ņ C.CuSO4¹ĢĢå D.P2O5
£Ø4£©¹¤ŅµÉĻŅŌNH3”¢æÕĘų”¢Ė®ĪŖŌĮĻÉś²śĻõĖį·ÖĪŖČż²½£ŗ
¢ŁNH3”śNO»Æѧ·½³ĢŹ½ĪŖ________________________________£»
¢ŚNO”śNO2ŹµŃéĻÖĻóŹĒ________________________________£»
¢Ū½«32.64gĶÓėl40mLŅ»¶ØÅØ¶ČµÄHNO3·“Ó¦£¬ĶĶźČ«Čܽā²śÉśµÄNOŗĶNO2»ģŗĻĘųĢåŌŚ±ź×¼×“æöĻĀµÄĢå»żĪŖ11.2L”£ŌņĘäÖŠNO”¢NO2µÄĪļÖŹµÄĮæ±ČĪŖ____________________”£
£Ø5£©Ķ¼1ÖŠŌŚ±ź×¼×“æöĻĀ½«NO2”¢NO”¢O2»ģŗĻ²¢³äĀśČŻĘ÷£¬½«øĆČŻĘ÷µ¹ÖĆÓŚĖ®ÖŠ£¬ĘųĢåĶźČ«Čܽā£¬ĪŽĘųĢåŹ£Óą£¬Čō²śĪļŅ²²»Ą©É¢£¬ŌņĖłµĆČÜŅŗµÄĪļÖŹµÄĮæÅضČM£¬Ę䏿ֵ“óŠ”·¶Ī§ĪŖ___________
A.0<M<l/22.4 B. 1/39.2<M<1/22.4 C.1/39.2<M<1/28 D.1/28<M<1/22.4
£Ø6£©Ķ¼1ÖŠX×Ŗ»ÆĪŖHNO3µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ________________________________”£
£Ø7£©ČōŅŖ½«NH3”śN2£¬“ÓŌĄķÉĻæ“£¬ĻĀĮŠŹŌ¼ĮæÉŠŠµÄŹĒ_______________”£
A.O2 B.Na C.NH4Cl D. NO2
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com