

| A、贝诺酯分子中所有碳原子一定共平面 |
| B、可用FeCl3 溶液区别乙酰水杨酸和对乙酰氨基酚 |
| C、贝诺酯与足量NaOH 溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠 |
| D、乙酰水杨酸和对乙酰氨基酚均可与NaHCO3 溶液反应 |


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将打磨过的铝箔在酒精灯上加热至熔化,熔化的铝不滴落,因为铝表面生成了氧化膜 |
| B、5mL淀粉溶剂和2滴碘水,1mL稀硫酸混合,加热颜色变浅,冷却后恢复原来颜色是因为淀粉水解以及水解产物重新结合生成淀粉 |
| C、某卤代弪与NaOH溶液共热,冷却后向其中滴加AgNO3溶液,产生白色沉淀,证明该卤代颈分子中一定含有氯原子 |
| D、将Fe(OH)3胶体和泥水混合物进行过滤,可以得到Fe(OH)3固体和泥土 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④ | B、②③④ |
| C、①②③ | D、②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有(1) |
| B、只有(2) |
| C、(2)(3) |
| D、(1)(2)(3) |
查看答案和解析>>
科目:高中化学 来源: 题型:
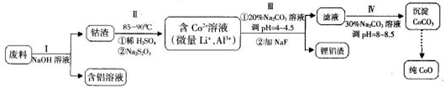
2- 3 |
2- 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、容量瓶使用前用1.0 mol?L-1的Na2CO3溶液润洗 |
| B、配制过程中,未用蒸馏水洗涤烧杯和玻璃棒 |
| C、仰视确定滴定终点 |
| D、用敞开容器称量Na2CO3且时间过长 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 组别 | 甲 | 乙 | 丙 |
| A | Al2O3 | HCl | NaOH |
| B | SiO2 | NaOH | HF |
| C | HCl | NaOH | NaHCO3 |
| D | NH3 | O2 | HNO3 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②④ | B、①③⑤ | C、③⑤ | D、⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com