
分析 (1)依据化学反应速率V=$\frac{△c}{△t}$计算,依据平衡移动原理分析;
(2)酸或碱抑制水电离,含有弱根离子的盐促进水电离;能形成原电池的装置能加快反应速率;
(3)加入的物质相当于氧化铜和水,根据转移电子相等计算;
(4)①2Zn(s)+O2(g)=2ZnO(s)△H=-701.0kJ•mol-1
②2Hg(l)+O2(g)=2HgO(s)△H=-181.6kJ•mol-1
根据盖斯定律,①-②计算;
(5)Cu2+沉淀较为完全浓度降至原来的千分之一,根据Ksp求出OH-离子的浓度,再求pH.
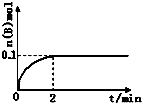
解答 解:(1)根据图象可知,0-2 min内,B的物质的量增加了0.1mol,则必然消耗A是0.2mol,使用平均反应速率v(A)=$\frac{0.2mol}{1L×2min}$=0.1 mol/(L•min);
平衡常数只与温度有关系,选项a不正确,由于反应前后体积不变,所以该反应是等效的,因此选项b、c正确,d不正确;
故答案为:0.1mol/(L•min); bc;
(2)水电离生成氢离子和氢氧根离子,所以酸能抑制水电离,锌和硫酸反应生成硫酸锌和氢气,硫酸锌是强酸弱碱盐,促进水电离,所以水的电离平衡向右移动;
a.向溶液中加入NaNO3,导致溶液中含有硝酸,硝酸和锌反应不产生氢气,故a错误;
b.CuSO4和锌发生置换反应生成铜,铜、锌和稀硫酸构成原电池,所以能加快反应速率,故b正确;
c.Na2SO4 不影响反应速率,故c错误;
d.NaHSO3和硫酸反应生成二氧化硫,氢离子浓度减小,所以生成氢气的速率减小,故d错误;
e.加入CH3COOH,醋酸是弱电解质,导致溶液中氢离子浓度减小,生成氢气速率减小,故e错误;
故答案为:向右;b;
(3)a mol 的Cu(OH)2相当于amolCuO和amoH2O,阳极上析出氧气,根据氧气和转移电子的关系式得转移电子数=amol×2×[0-(-2)]NA/mol=4aNA,故答案为:4aNA;
(4)已知:①2Zn(s)+O2(g)=2ZnO(s)△H=-701.0kJ•mol-1
②2Hg(l)+O2(g)=2HgO(s)△H=-181.6kJ•mol-1
根据盖斯定律,①-②得2Zn(s)+2HgO(s)=2ZnO(s)+2Hg(l),△H=(-701.0kJ•mol-1 )-(-181.6kJ•mol-1 )=-519.4kJ•mol-1,
即Zn(s)+HgO(s)=ZnO(s)+Hg(l),△H=-259.7kJ•mol-1;故答案为:-259.7 kJ•mol-1;
(5)Cu2+沉淀较为完全是的浓度为$\frac{0.2mol/L}{1000}$=2×10-4mol/L,
则c(OH-)=$\sqrt{\frac{2×10{\;}^{-20}}{2×10{\;}^{-4}}}$mol/L═10-8mol/L,
则c(H+)=$\frac{1×10{\;}^{-14}}{10{\;}^{-8}}$mol/L=10-6mol/L,
所以pH=-lg(10-6)=6,
故答案为:6.
点评 本题考查了化学反应速率的计算、平衡移动原理、影响反应速率的因素、盖斯定律以及溶度积常数的计算等知识点,明确弱电解质电离特点是解本题关键,注意(2)中硝酸和锌反应不产生氢气,为易错点.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.24 L CO2中含有的原子数为0.3×6.02×1023 | |
| B. | 0.1 L 3 mol•L-1的NH4NO3溶液中含有的NH4+数目为0.3×6.02×1023 | |
| C. | 5.6 g铁粉与硝酸反应失去的电子数一定为0.3×6.02×1023 | |
| D. | 4.5 g SiO2晶体中含有的硅氧键数目为0.3×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用酒精萃取溴水中的溴单质的操作可选用分液漏斗,而后静置分液 | |
| B. | 进行分液时,分液漏斗中的下层液体,从下端流出,上层液体则从上口倒出 | |
| C. | 萃取、分液前需对分液漏斗进行检漏 | |
| D. | 将上面的塞子拿下,可以保证分液漏斗内的液体顺利流出 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
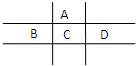 有A、B、C、D、E五种短周期元素,且相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的氢氧化物是两性氢氧化物,E的阳离子与A的阴离子核外电子层结构相同.
有A、B、C、D、E五种短周期元素,且相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的氢氧化物是两性氢氧化物,E的阳离子与A的阴离子核外电子层结构相同.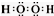 ,分子中所含共价键的类型为极性键、非金属性键.
,分子中所含共价键的类型为极性键、非金属性键.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  如图表示改变某化学平衡体系的温度时,反应速率随时间的变化情况 | |
| B. |  如图表示向稀盐酸中滴加氢氧化钠溶液时,溶液pH的变化情况 | |
| C. | 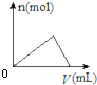 如图向氯化铝溶液中滴加氨水时,生成沉淀的物质的量变化情况 | |
| D. |  如图表示△H<0的可逆反应,化学平衡常数随温度的变化情况 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl | B. | H2SO4 | C. | AgNO3 | D. | Na2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
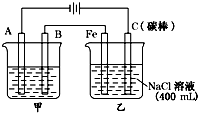 如图为相互串联的甲乙两电解池.试回答:
如图为相互串联的甲乙两电解池.试回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1个N≡N键断裂的同时,有6个N-H键形成 | |
| B. | 混合气体的密度不再改变 | |
| C. | v正(H2)=$\frac{3}{2}$ v逆(NH3) | |
| D. | N2、H2、NH3的体积比为1:3:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com