

| ĪļÖŹ | CaCO3 | MgCO3 | Ca£ØOH£©2 | Mg£ØOH£©2 | Fe £ØOH£©3 |
| Ksp | 4.96”Į10-9 | 6.82”Į10-6 | 4.68”Į10-6 | 5.61”Į10-12 | 2.64”Į10-39 |
| Ksp |
| [OH-]2 |
| 5.61”Į10-12 |
| 10-12 |
| Ksp |
| [OH-]3 |
| 2.64”Į10-39 |
| 10-18 |



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
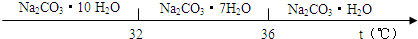
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ


| ĪļÖŹ | CaCO3 | MgCO3 | Ca£ØOH£©2 | Mg£ØOH£©2 | Fe £ØOH£©3 |
| Ksp | 4.96”Į10-9 | 6.82”Į10-6 | 4.68”Į10-6 | 5.61”Į10-12 | 2.64”Į10-39 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
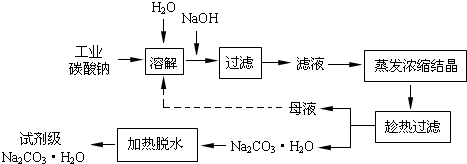
£Ø10·Ö£©¹¤ŅµĢ¼ĖįÄĘ£Ø“æ¶ČŌ¼ĪŖ98£„£©ÖŠ³£ŗ¬ÓŠCa2+”¢Mg2+”¢Fe3+”¢Cl”„ŗĶSO42”„µČŌÓÖŹ£¬ĪŖĮĖĢį“湤ŅµĢ¼ĖįÄĘ£¬²¢»ńµĆŹŌ¼Į¼¶Ģ¼ĖįÄĘµÄ¹¤ŅÕĮ÷³ĢĶ¼ČēĻĀ£ŗ
ŅŃÖŖ£ŗĢ¼ĖįÄʵı„ŗĶČÜŅŗŌŚ²»Ķ¬ĪĀ¶ČĻĀĪö³öµÄČÜÖŹČēĻĀĶ¼ĖłŹ¾£ŗ
£Ø1£©¼ÓČėNaOHČÜŅŗŹ±·¢ÉśµÄĄė×Ó·“Ó¦·½³ĢŹ½ĪŖ ”ų ”¢ ”ų ”£
£Ø2£©ČȵÄNa2CO3ČÜŅŗÓŠ½ĻĒæµÄČ„ÓĶĪŪÄÜĮ¦£¬ĘäŌŅņŹĒ£ØÓĆĄė×Ó·½³ĢŹ½¼°±ŲŅŖµÄĪÄ×Ö¼ÓŅŌ½āŹĶ£© ”ų ”£
£Ø3£©”°³ĆČČ¹żĀĖ”±Ź±µÄĪĀ¶ČÓ¦æŲÖĘŌŚ ”ų ”£
£Ø4£©ŅŃÖŖ£ŗNa2CO3”¤10H2O(s)£½Na2CO3(s)£«10 H2O(g) ”÷H£½+532.36kJ”¤mol”Ŗ1
””Na2CO3”¤10H2O(s)£½Na2CO3”¤H2O(s)£«9 H2O(g) ”÷H£½+473.63kJ”¤mol”Ŗ1
Š“³öNa2CO3”¤H2OĶŃĖ®·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ ”ų ”£
£Ø5£©ÓŠČĖ“Ó”°ĀĢÉ«»Æѧ”±½Ē¶ČÉčĻė½«”°ÄøŅŗ”±ŃŲĮ÷³ĢĶ¼ÖŠŠéĻßĖłŹ¾½ųŠŠŃ»·Ź¹ÓĆ”£ĒėÄć·ÖĪöŹµ¼ŹÉś²śÖŠŹĒ·ńæÉŠŠ ”ų £¬ĘäĄķÓÉŹĒ ”ų ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2012-2013ѧğĮÉÄžŹ”Ī劣Š×÷ĢåøßČż³å“Ģ×īŗóŅ»Ä£»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗ¼ĘĖćĢā
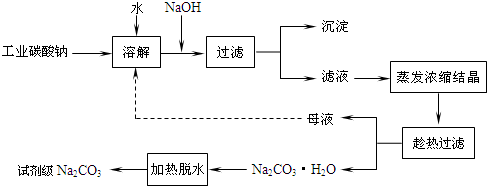
¹¤ŅµĢ¼ĖįÄĘ£Ø“æ¶ČŌ¼ĪŖ98£„£©ÖŠŗ¬ÓŠCa2+”¢Mg2+”¢Fe3+”¢Cl£ŗĶSO42”ŖµČŌÓÖŹ£¬Ģį“湤ŅÕĻßĀ·ČēĶ¼ĖłŹ¾£ŗ

¢ń£®Ģ¼ĖįÄʵı„ŗĶČÜŅŗŌŚ²»Ķ¬ĪĀ¶ČĻĀĪö³öµÄČÜÖŹČēĶ¼ĖłŹ¾£ŗ

¢ņ£®ÓŠ¹ŲĪļÖŹµÄČܶȻżČēĻĀ
|
ĪļÖŹ |
CaCO3 |
MgCO3 |
Ca£Ø0H£©2 |
Mg£ØOH£©2 |
Fe£ØOH£©3 |
|
Ksp |
4.96”Į10£9 |
6.82”Į10£6 |
4.68”Į10£6 |
5.61”Į10£12 |
2.64”Į10£39 |
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©¼ÓČėNaOHČÜŅŗŹ±£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ ”£Ļņŗ¬ÓŠMg2+”¢Fe3+µÄČÜŅŗÖŠµĪ¼ÓNaOHČÜŅŗ£¬µ±Į½ÖÖ³Įµķ¹²“ęĒŅČÜŅŗµÄpH=8Ź±£¬c£ØMg2+£©£ŗc£ØFe3+£©= ”£
£Ø2£©”°ÄøŅŗ”±ÖŠ³żĮĖŗ¬ÓŠNa+”¢CO32”ŖĶā£¬»¹ŗ¬ÓŠ µČĄė×Ó”£
£Ø3£©ÓŠČĖ“Ó”°ĀĢÉ«»Æѧ”±½Ē¶ČÉčĻė½«”°ÄøŅŗ”±ŃŲĮ÷³ĢÖŠŠéĻß½ųŠŠŃ»·Ź¹ÓĆ”£ĒėÄć·ÖĪöŌŚŹµ¼Ź¹¤ŅµÉś²śÖŠŹĒ·ńæÉŠŠ£ŗ £ØĢī”°æÉŠŠ”±»ņ”°²»æÉŠŠ”±£©£¬²¢ĖµĆ÷ĄķÓÉ£ŗ ”£
£Ø4£©ŅŃÖŖ£ŗNa2CO3”¤10H2O£Øs£©=Na2CO3£Øs£©+10H2O£Øg£© =+532.36 kJ”¤mol£1
=+532.36 kJ”¤mol£1
Na2CO3”¤10H2O£Øs£©=Na2CO3”¤H2O£Øs£©+9H2O£Øg£©  =+473.63
kJ”¤mol£1
=+473.63
kJ”¤mol£1
Š“³öNa2CO3”¤H2OĶŃĖ®·“Ó¦µÄČČ»Æѧ·½³ĢŹ½£ŗ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ½ĖÕŹ”ÄĻĶØŹŠĶØÖŻĒų2010½ģøßČż²éĀ©²¹Č±×ØĻīĮ·Ļ°»ÆѧŹŌĢā ĢāŠĶ£ŗĢīæÕĢā
£Ø10·Ö£©¹¤ŅµĢ¼ĖįÄĘ£Ø“æ¶ČŌ¼ĪŖ98£„£©ÖŠ³£ŗ¬ÓŠCa2+”¢Mg2+”¢Fe3+”¢Cl”„ŗĶSO42”„µČŌÓÖŹ£¬ĪŖĮĖĢį“湤ŅµĢ¼ĖįÄĘ£¬²¢»ńµĆŹŌ¼Į¼¶Ģ¼ĖįÄĘµÄ¹¤ŅÕĮ÷³ĢĶ¼ČēĻĀ£ŗ

ŅŃÖŖ£ŗĢ¼ĖįÄʵı„ŗĶČÜŅŗŌŚ²»Ķ¬ĪĀ¶ČĻĀĪö³öµÄČÜÖŹČēĻĀĶ¼ĖłŹ¾£ŗ

£Ø1£©¼ÓČėNaOHČÜŅŗŹ±·¢ÉśµÄĄė×Ó·“Ó¦·½³ĢŹ½ĪŖ ”ų ”¢ ”ų ”£
£Ø2£©ČȵÄNa2CO3ČÜŅŗÓŠ½ĻĒæµÄČ„ÓĶĪŪÄÜĮ¦£¬ĘäŌŅņŹĒ£ØÓĆĄė×Ó·½³ĢŹ½¼°±ŲŅŖµÄĪÄ×Ö¼ÓŅŌ½āŹĶ£© ”ų ”£
£Ø3£©”°³ĆČČ¹żĀĖ”±Ź±µÄĪĀ¶ČÓ¦æŲÖĘŌŚ ”ų ”£
£Ø4£©ŅŃÖŖ£ŗNa2CO3”¤10 H2O(s)£½Na2CO3(s)£«10 H2O(g) ”÷H£½+532.36kJ”¤mol”Ŗ1
””Na2CO3”¤10 H2O(s)£½Na2CO3”¤H2O(s)£«9 H2O(g) ”÷H£½+473.63kJ”¤mol”Ŗ1
Š“³öNa2CO3”¤H2OĶŃĖ®·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ ”ų ”£
£Ø5£©ÓŠČĖ“Ó”°ĀĢÉ«»Æѧ”±½Ē¶ČÉčĻė½«”°ÄøŅŗ”±ŃŲĮ÷³ĢĶ¼ÖŠŠéĻßĖłŹ¾½ųŠŠŃ»·Ź¹ÓĆ”£ĒėÄć·ÖĪöŹµ¼ŹÉś²śÖŠŹĒ·ńæÉŠŠ ”ų £¬ĘäĄķÓÉŹĒ ”ų ”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com