
【题目】现有25℃时0.1molL﹣1的氨水.请回答以下问题:
(1)若向氨水中加入少量硫酸铵固体,此时溶液中 ![]() (填“增大”、“减小”或“不变”).
(填“增大”、“减小”或“不变”).
(2)若向氨水中加入稀硫酸,使其恰好完全中和,写出反应的离子方程式:;所得溶液的pH7(填“<”、“=”或“>”),用离子方程式表示其原因 .
(3)若向氨水中加入稀硫酸至溶液的pH=7,此时 ![]() =a molL﹣1 ,
=a molL﹣1 , ![]() 则= .
则= .
【答案】
(1)减小
(2)NH3?H2O+H+=NH4++H2O;<; NH4++H2O?NH3?H2O+H+
(3)0.5amol/l
【解析】解:(1)由于(NH4)2SO4=2NH4++SO42﹣,溶液中NH4+浓度增大,抑制氨水电离,导致溶液中氢氧根离子浓度减小,氨水分子浓度增大,所以此时溶液中液中 ![]() 减小;
减小;
所以答案是:减小;(2)硫酸和氨水反应生成硫酸铵和水,离子反应方程式为NH3.H2O+H+=NH4++H2O,硫酸铵是强酸弱碱盐水解而使其溶液呈酸性,水解方程式为:NH4++H2ONH3.H2O+H+;
所以答案是:NH3H2O+H+=NH4++H2O,<,NH4++H2ONH3H2O+H+;(3)溶液呈中性,则溶液中c(H+)=c(OH﹣),溶液呈电中性,溶液中存在电荷守恒c(NH4+)+c(H+)=2c(SO42﹣ )+c(OH﹣),所以c(SO42﹣ )=0.5c(NH4+)=0.5amol/l;
所以答案是:0.5amol/l.
【考点精析】关于本题考查的弱电解质在水溶液中的电离平衡,需要了解当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理才能得出正确答案.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】有机物H (结构简式为 )是合成高分子化合物M的单体,H可以通过有机物A (分子式为C7H8O) 和丙酮为原料来进行合成,E为中间产物(结构简式为
)是合成高分子化合物M的单体,H可以通过有机物A (分子式为C7H8O) 和丙酮为原料来进行合成,E为中间产物(结构简式为 )其合成路线如图:
)其合成路线如图:

己知:![]()
请回答下列问题:
(1)A的名称为_________,G 中含氧官能团的名称是________________;①的反应类型是__________。
(2)检验有机物A中官能团的方法为______________________________。
(3)高分子化合物M 的结构简式为____________________。
(4)反应③的化学反应方程式为______________________________。
(5)有机物C有多种同分异构体,其中苯环上只有两个侧链的芳香酯的同分异构体有__________种
(6)已知: ,以2-溴丙烷和乙烯为原料,选用必要的无机试剂合成
,以2-溴丙烷和乙烯为原料,选用必要的无机试剂合成![]() ,此合成路线为
,此合成路线为 ,请完成接下来的合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上下注明试剂和反应条件)。____________
,请完成接下来的合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上下注明试剂和反应条件)。____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从樟科植物枝叶提取的精油中含有甲、乙两种成分: ![]()
(1)①用酸性高锰酸钾溶液检验甲和乙中含有碳碳双键,方案是否可行(填“可 行”或“不可行”).
②请写出甲的一种能同时满足下列3个条件的同分异构体的结构简式 .
a.苯环上有两个不同的取代基
b.能与Br2的CCl4溶液发生加成反应
c.遇FeCl3溶液呈现紫色
(2)由甲转化为乙的过程为(已略去无关产物): 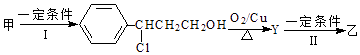
步骤Ⅰ的反应类型为 , Y的结构简式 , 设计步骤Ⅰ的目的是 .
(3)1mol乙最多可与 mol H2发生加成反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的定容密闭容器中,当下列物理量不再变化时,可表明反应:A(g)+B(g)![]() C(g)+D(g) 已达化学平衡状态的是( )
C(g)+D(g) 已达化学平衡状态的是( )
A. 混合气体的压强 B. B的物质的量浓度 C. 混合气体的密度 D. v(A)正 = v(D)正
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项中的两种物质不论以何种比例混合,只要混合物的总物质的量一定,则完全燃烧消耗O2的物质的量保持不变的是( )
A. C2H6、C2H6O B. C3H6、C2H4 C. C3H4、C2H6O D. C2H4、C2H6O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. FeCl3溶液可用于铜质印刷线路板的制作,该反应是置换反应
B. 用惰性电极电解含有H218O的普通水时,阳极可能产生两种相对分子质量不同的氧分子
C. 反应A(g) ![]() B(g) △H,若正反应的活化能为EakJ/mol,逆反应的活化能为EbkJ/mol,则△H=-(Ea-Eb)kJ/mol
B(g) △H,若正反应的活化能为EakJ/mol,逆反应的活化能为EbkJ/mol,则△H=-(Ea-Eb)kJ/mol
D. 3x%的A物质的溶液与x%的A物质的溶液等体积混合后,溶液的质量分数小于2x%,则A物质可能为乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过石油裂解可以获得乙烯,再以乙烯为原料还可以合成很多的化工产品,试根据图回答有关问题: 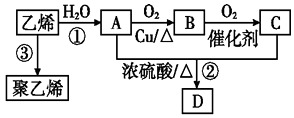
已知:有机物D是一种有水果香味的油状液体.
(1)有机物B的名称为 , 结构简式为 . 决定有机物A、C的化学特性的原子团的名称分别是 .
(2)写出图示反应②、③的化学方程式,并指明反应类型: ②; 反应类型: .
③; 反应类型: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用酸式滴定管准确移取25.00mL某未知浓度的盐酸溶于一洁净的锥形瓶中,然后用0.2000molL ﹣1的氢氧化钠溶液(指示剂为酚酞),滴定结果如下:
NaOH起始读数 | NaOH终点读数 | |
第一次 | 0.10mL | 18.60mL |
第二次 | 0.30mL | 18.00mL |
(1)根据以上数据可以计算出盐酸的物质的量浓度为molL﹣1 .
(2)达到滴定终点的标志是 .
(3)以下操作造成测定结果偏高的原因可能是 .
A.配制标准溶液的氢氧化钠中混有Na2CO3杂质
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
E.未用标准液润洗碱式滴定管.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com