
【题目】表为元素周期表的一部分:
IA | IIA | IIIA | IVA | VA | VIA | VIIA | ||
二 | C | N | ① | |||||
三 | ② | ③ | ④ | P | ⑤ | ⑥ |
请填写下列空白:
(1)表中元素,原子半径最大的是(填写元素符号);①的核外电子排布式;③和⑥两元素形成化合物的电子式为 .
(2)②③④三种元素最高价氧化物对应的水化物中,碱性最强的是(填化学式).
(3)比较④、⑤两种元素的简单离子半径:>(填离子符号);元素④最高价氧化物对应的水化物与硝酸反应的离子方程式为 .
(4)列举一个事实来证明元素①比元素⑤的非金属性强 .
(5)若8g甲烷气体完全燃烧生成液态水时放出445.15kJ的热量,请写出其热化学方程式 .
【答案】
(1)Na;1s22s22p4; ![]()
(2)NaOH
(3)S2﹣; Al3+; Al(OH)3+3H+=Al3++3H2O
(4)H2O的稳定性大于H2S
(5)CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=﹣890.3KJ?mol﹣1
【解析】解:(1)由元素在周期表中位置,可知①为O、②为Na、③为Mg、④为Al、⑤为S、⑥为Cl,电子层越多原子半径越大,所以第三周期的元素半径大于第二周期的元素,
同周期自左而右原子半径减小,表中元素,原子半径最大的是Na,①为O为8号元素,原子核外有8个电子,核外电子排布式为1s22s22p4,③和⑥两元素形成化合物为氯化镁,氯化镁是离子化合物,由镁离子与氯离子构成,电子式为 ![]() ,
,
所以答案是:Na;1s22s22p4; ![]() ;(2)②为Na、③为Mg、④为Al,三者位于同一周期,金属性Na>Mg>Al,则最高价氧化物对应水合物的碱性最强的为NaOH,
;(2)②为Na、③为Mg、④为Al,三者位于同一周期,金属性Na>Mg>Al,则最高价氧化物对应水合物的碱性最强的为NaOH,
所以答案是:NaOH; (3)S2﹣核外有三层电子,结构示意图为 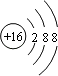 ,Al3+核外有两层电子,结构示意图为:
,Al3+核外有两层电子,结构示意图为: 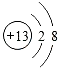 .离子电子层数越多,离子半径越大,则离子半径S2﹣>Al3+,元素④最高价氧化物对应的水化物为氢氧化铝,与硝酸生成硝酸铝和水,硝酸、硝酸铝拆成离子,离子方程式为:Al(OH)3+3H+=Al3++3H2O,
.离子电子层数越多,离子半径越大,则离子半径S2﹣>Al3+,元素④最高价氧化物对应的水化物为氢氧化铝,与硝酸生成硝酸铝和水,硝酸、硝酸铝拆成离子,离子方程式为:Al(OH)3+3H+=Al3++3H2O,
所以答案是:S2﹣;Al3+;Al(OH)3+3H+=Al3++3H2O;(4)元素的非金属性越强,对应氢化物的稳定性越强,H2O的稳定性大于H2S,则O的非金属性比S的强,
所以答案是:H2O的稳定性大于H2S;(5)8g甲烷n(CH4)= ![]() =0.5mol,完全燃烧生成液态水时放出的热量是445.15kJ,则1mol计算完全燃烧放出890.3KJ的能量,所以热化学方程式为CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=﹣890.3KJmol﹣1,
=0.5mol,完全燃烧生成液态水时放出的热量是445.15kJ,则1mol计算完全燃烧放出890.3KJ的能量,所以热化学方程式为CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=﹣890.3KJmol﹣1,
所以答案是:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=﹣890.3KJmol﹣1.


科目:高中化学 来源: 题型:
【题目】如图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略)。
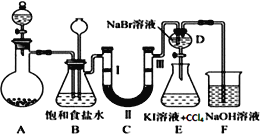
(1)装置 A 中反应的化学反应方程式为:________________________________。装置 B 中饱和食盐水的作用是___________________;同时装置 B 亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时 B 中的现象________________________________。
(2)装置 C 的实验目的是验证氯气是否具有漂白性,为此 C 中Ⅰ、Ⅱ、Ⅲ依次放入_____________。(填序号)
a | b | c | d | |
Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(3)设计装置 D、 E 的目的是验证氯、溴、碘单质的氧化性强弱(Cl2> Br2>I2),当向D中缓缓通入少量氯气时,可以看到无色溶液逐渐变为橙黄色,说明Cl2氧化性>Br2,打开活塞,将装置D中少量溶液加入装置 E中,振荡,观察到的现象是________________________________。
(4)工业上将氯气通入石灰乳制取漂白粉, 化学反应方程式为_____________________________,漂白粉敞放于空气中会失效,请写出失效所发生反应的化学方程式_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,用0.1000mol/L NaOH溶液滴定25.00mL 0.1000mol/L某一元酸HX溶液,滴定过程中pH变化曲线如图所示.下列说法不正确的是( ) 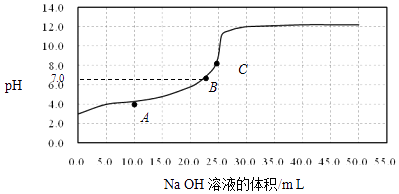
A.在A点:c(HX)>c(Na+)>c(X﹣)
B.在B点,溶液中c(H+)=c(OH﹣)
C.C点溶液中存在的主要平衡是X﹣+H2OHX+OH﹣
D.0.05mol/L NaX溶液的pH≈9
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究电化学腐蚀及防护的装置如图所示.下列有关说法正确的是( ) 
A.锌片发生氧化反应作阴极
B.电子从铁片经过导线流向锌片
C.铁片上电极反应为:O2+2H2O+4e→4OH﹣
D.该装置可用于研究外加电流阴极保护法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组欲测定某已部分变质的小苏打样品中Na2CO3的质量分数,设计如下实验方案。
【方案一】称取一定质量样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算。
(1)坩埚中发生反应的化学方程式为_______________。
(2)实验中,需加热至恒重的目的是_______________。
【方案二】称取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量Ba(OH)2溶液,过滤,洗涤、干燥沉淀,称量固体质量,计算。(已知:Ba2++OH-+HCO3-==BaCO3↓+H2O)
(1)过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为_______________。
(3)实验中判断沉淀是否完全的方法是_______________。
【方案三】按如下图所示装置进行实验:
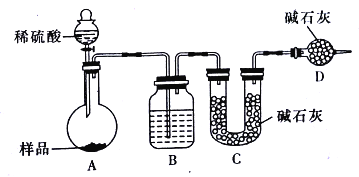
(1)D装置的作用是_______________。分液漏斗中_________(填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(2)实验前称取17.90g样品,实验后测得C装置增重8.80g,则样品中Na2CO3的质量分数为________________(保留三位有效数字)
(3)根据此实验测得的数据,测定结果有误差,因为实验装置还存的在一个明显缺陷是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烯烃A在一定条件下可以按下面的框图进行反应. 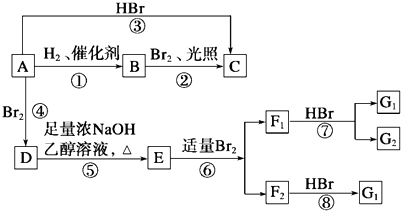
已知:D是 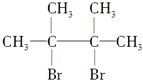 .
.
请填空:
(1)A的结构简式是 , 其名称为 .
(2)框图中属于取代反应的是(填数字代号).
(3)框图中①、③、⑥属于反应.
(4)G1的结构简式是
(5)写出由D→E的化学方程式:;写出由E→F2的化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量的NaOH溶液中逐滴加入AlCl3溶液,生成沉淀Al(OH)3的量随AlCl3加入量的变化关系如图所示。则下列离子组在对应的溶液中一定能大量共存的是
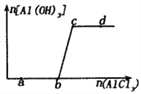
A. a点对应的溶液中: Na+、K+、SO42-、HCO3-
B. b点对应的溶液中:Na+、ClO-、SO42-、Cl-
C. c点对应的溶液中: Ag+、H+、Ca2+、NO3-
D. d 点对应的溶液中: K+、NH4+、OH-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,2﹣二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度是2.18克/厘米3 , 沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验中可以用如图所示装置制备1,2﹣二溴乙烷.其中分液漏斗和仪器a中装有乙醇和浓硫酸的混合液,试管d中装有浓溴(表面覆盖少量水).请填写下列空白: 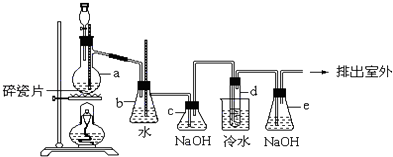
(1)图中a仪器的名称 , 实验中加入沸石的作用是 . 若加热后发现未加沸石,应采取的正确方法是 .
(2)仪器a中发生的是乙醇的消去反应,反应温度是170℃,且该反应要求温度迅速升高到170℃,请你写出乙醇的这个消去反应方程式: .
(3)写出装置d中反应的化学方程式: .
(4)装置b的作用: .
(5)e装置内NaOH溶液的作用是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com