
【题目】利用下图所示的有机物X可生产S诱抗素Y。下列说法正确的是
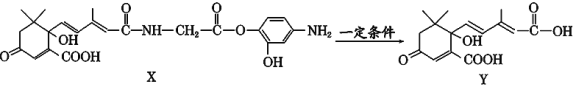
A. X结构中有2个手性碳原子
B. X可以发生氧化、取代、酯化、加聚、缩聚反应
C. Y既可以与FeCl3溶液发生显色反应,又可使酸性KMnO4溶液褪色
D. 1 mol X与足量NaOH溶液反应,最多消耗4 mol NaOH,1 mol Y最多能加成4 molH2
【答案】B
【解析】
A.连有4个不同原子或原子团的碳原子为手性碳原子,则X中只有与-OH相连的C为手性碳原子,A错误;
B. X中含有-OH、-COOH、碳碳双键、-CONH-、-COOC-,可以发生氧化、取代、酯化、加聚、缩聚反应,含-NH2则能与盐酸反应生成有机盐,B正确;
C.Y中不含酚羟基,则不具有酚的性质,所以不与FeCl3溶液发生显色反应,但含有-OH、C=C,能使酸性KMnO4溶液褪色,C错误;
D.-OH、-COOH、-CONH-、-COOC-均能与碱反应,则1molX与足量NaOH溶液反应,最多消耗5molNaOH,Y中含3个碳碳双键和1个![]() ,则1molY最多能加成消耗4molH2,D错误;
,则1molY最多能加成消耗4molH2,D错误;
故合理选项是B。


 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:
【题目】常温下,向25 mL 0.1 mol·L-1NaOH溶液中逐滴滴加0.2 mol·L-1的HN3(叠氮酸)溶液,pH的变化曲线如图所示(溶液混合时体积的变化忽略不计,叠氮酸的是一元弱酸)。下列说法正确的是

A. 在C点,滴加的V(HN3)=12.5 mL
B. 在B点,离子浓度大小为 c(OH-)>c(H+)>c (Na+)>c(N3-)
C. 水电离出的c(H+):A点小于B点
D. 在D点,c(Na+)=2c(HN3)+2 c(N3-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两烧杯中各盛有100 mL 3 mol·L-1的盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后生成的气体的体积比为甲∶乙=1∶2,则加入铝粉的质量为( )
A.5.4 gB.3.6 gC.2.7 gD.1.8 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】泄盐(MgSO4·7H2O)是一种中药药剂,还可用于制革、肥料、瓷器、印染料等工业。一种利用氯碱工业的废渣(主要成分是Mg(OH)2,杂质为MnCO3、FeCO3、Al(OH)3、SiO2等)生产泄盐的流程如下:
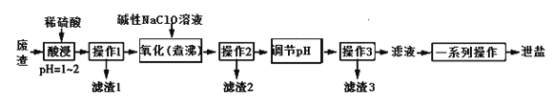
已知部分氢氧化物沉淀pH如下表:
氢氧化物 | Fe(OH)3 | Mg(OH)2 | Al(OH)3 | Al(OH)3在pH=7.8时开始溶解,pH=10.0完全溶解 |
开始沉淀的pH | 2.3 | 10.8 | 3.7 | |
完全沉淀的pH | 4.3 | 12.4 | 5.2 |
回答下列问题:
(1) “酸浸”是工业对矿物利用的一种方法,该操作关键是提供浸取率和浸取速率,写出提高该工艺流程中“酸浸”速率的2种方法:___________________。
(2) “操作1” “操作2”和“操作3”相同,实验室在进行该操作时,用到的玻璃仪器有________,“滤渣1”的成分是________(写化学式)。
(3) “氧化(煮沸)”操作的目的是使溶液中的锰元素转化为MnO2,写出该反应的离子方程式:____________________。
(4)“调节pH”时最好选用__________, pH范围应控制为____________,高温加热“滤渣3”可得到_________(写化学式)。
(5) “一系列操作”是指_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、Q、R的原子序数依次增大,X的简单阴离子与锂离子具有相同的电子层结构,Y原子最外层电子数等于内层电子数的2倍,Q的单质与稀硫酸剧烈反应生成X的单质。向100mL X2R的水溶液中缓缓通入RZ2气体,溶液pH与RZ2体积关系如图。下列说法错误的是
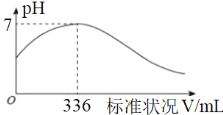
A.单质的沸点:Q>Z>XB.X2R溶液的浓度为0.3 molL-1
C.简单气态氢化物稳定性Z>R>YD.将RZ2分别通入BaCl2、Ba(NO3)2溶液中,均无明显现象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如何降低大气中CO2的含量及有效地开发利用CO2是当前科学家研究的重要课题。
(1)利用H2和CO2生产甲醇燃料。为探究该反应原理,进行如下实验:某温度下,在容积为2 L的密闭容器中充入1 mol CO2和3.25 molH2,在一定条件下反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间的变化关系如图所示。
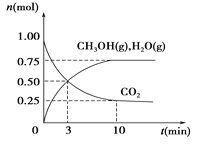
①从反应开始到3min时,氢气的平均反应速率v(H2)=_________。
②下列措施中一定能使CO2的转化率增大的是____________。
A.在原容器中再充入1 molCO2 B.在原容器中再充入1molH2
C.在原容器中充入1 molHe D.使用更有效的催化剂
E.缩小容器的容积 F.将水蒸气从体系中分离出
(2)利用氢气在一定条件下与二氧化碳反应生成乙醇燃料,其热化学反应方程式为2CO2(g)+6H2(g)![]() CH3CH2OH(g)+3H2O(g) ΔH=akJ/mol,在一定条件下,测得该反应达到平衡状态时的实验数据如表所示。请根据表中数据回答下列问题。
CH3CH2OH(g)+3H2O(g) ΔH=akJ/mol,在一定条件下,测得该反应达到平衡状态时的实验数据如表所示。请根据表中数据回答下列问题。
温度(K) CO 2转化率/ (%)
| 500 | 600 | 700 | 800 |
1.5 | 45 | 33 | 20 | 12 |
2 | 60 | 43 | 28 | 15 |
3 | 80 | 61 | 35 | 21 |
①上述反应的a________0(填“大于”或“小于”)。该反应自发的条件是__________(填“高温”,“低温”,或“任意温度”)。
②恒温下,向反应体系中加入固体催化剂,则反应产生的热量________(填“增大”、“减小”或“不变”)。
③在2L密闭容器中充入1molCO2,在![]() =3,500K的温度下达到化学平衡时,则反应的平衡常数是_______________。
=3,500K的温度下达到化学平衡时,则反应的平衡常数是_______________。
(3)锂空气电池是前景很广的新颖电池,但锂和空气中的氮气、二氧化碳、水蒸气等发生副反应是锂-空气电池的致命缺陷。所以应在锂金属电极上加一个保护层。该技术的核心是锂表面增加了一层由碳酸锂/碳(Li2CO3/C)组成的致密的保护性涂层。涂层的过程:利用熔融碳酸盐作电解质,直接由锂金属电极与二氧化碳通过 10 次充放电循环,在电极的表面进行化学反应来完成。写出锂电极生成致密保护涂层的电极反应式___________________。利用一种钾盐水溶液作电解质,CO2电催化还原为乙烯,如图所示。在阴极上产生乙烯的电极反应式为_________________。
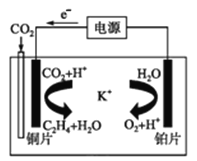
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组对某无色水样进行检验,已知水样中只可能含有K+、Mg2+、Cu2+、Al3+、CO32-、SO42-、C1-中的若干种离子。该小组取100mL水样进行实验,先滴加硝酸钡溶液,再滴加1mol·L-1的硝酸,实验过程中沉淀质量变化情况如图所示,下列分析错误的是

A. 一定含有的离子是:K+、SO42-、CO32-
B. BC段反应的离子方程式:BaCO3+2H+=Ba2++CO2↑+H2O
C. K+物质的量浓度的范围是: c(K+)≥0.6mol/L
D. 取少量水样置于试管中,滴加硝酸银溶液,可检验水样中是否含有C1-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铅酸蓄电池的工作原理如图所示,其总反应式为Pb+PbO2+2H2SO4=2PbSO4+2H2O。下列判断不正确的是( )
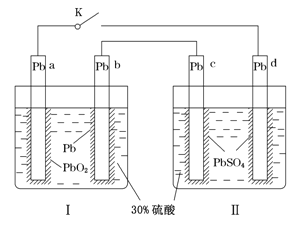
A. 闭合K时,d电极的反应式为PbSO4+2H2O-2e-=PbO2+4H++SO42—
B. 当电路中转移0.2 mol电子时,Ⅰ中消耗的H2SO4为0.2 mol
C. 闭合K时,Ⅱ中SO42—向c电极迁移
D. 闭合K一段时间后,Ⅱ可单独作为原电池,d电极为正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
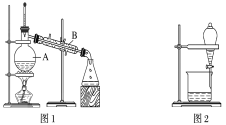
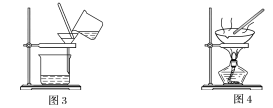
(1)装置图1中B的名称是________________,图2中漏斗的名称是________________。A中一般要加入碎瓷片,其作用是__________________________。下列关于以上实验操作说法一定正确的是_。
A.图1实验中,加热一段时间后发现未加入碎瓷片,应马上添加,以防发生危险
B.图2实验中,应打开活塞,将有机溶剂从下端导管中放出
C.图3实验中,可以用玻璃棒在漏斗中搅拌,以加快过滤速度
D.图4实验中,当加热至有较多固体析出时,即停止加热
(2)现有一瓶A和B的混合液,已知它们的性质如下表。
物质 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 | 溶解性 |
A | -11.5 | 198 | 1.11 | A、B互溶,且均易溶于水和酒精 |
B | 17.9 | 290 | 1.26 |
据此分析,将A和B相互分离可选用上图中的图________________所示仪器。
(3)在图2所示实验中,静置分层后,如果不知道哪一层液体是“水层”,试设计一种简便的判断方法。____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com