
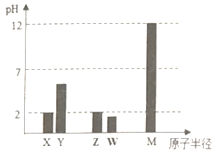
����Ŀ��X��Y��Z��W��MΪ����������Ԫ�أ�25��Cʱ��������������Ӧ��ˮ���Ũ�Ⱦ�Ϊ 0.01mol.L-1)��Һ��pH��ԭ�Ӱ뾶�Ĺ�ϵ��ͼ��ʾ�������й�˵������ȷ����
A. Y�����������ĵ���ʽΪ��![]()
B. �����̬�⻯������ȶ��ԣ�Z>W
C. X��M����Ԫ���γɵļ����Ӱ뾶��С˳��X<M
D. X���⻯����Z���⻯�ﷴӦ�����ɵĻ������мȺ����Ӽ��ֺ����ۼ�
���𰸡�C
��������X��Y��Z��W��MΪ����������Ԫ�أ�25��Cʱ��������������Ӧ��ˮ���Ũ�Ⱦ�Ϊ 0.01mol.L-1)��Һ��pH��ԭ�Ӱ뾶�Ĺ�ϵ:NaOH��Һ��pHΪ12��MΪNa�������pH=2��XΪNԪ�أ�Y��ӦpH��2��Ϊ̼�ᣬ��YΪC��W��ӦpH��2��Ϊ���ᣬ����WΪS��Z��ӦpH=2����ԭ�������������Z��Cl��
A��YΪ̼Ԫ�أ�Y�����������ΪCO2������ʽΪ��![]() ����A��ȷ��B����Ԫ�صķǽ����Ա���ǿ�������̬�⻯������ȶ��ԣ�Z>W����B��ȷ��C��X��M����Ԫ���γɵļ����Ӱ뾶��С˳��X>M��N3����Na����������Ų���ͬ�����Ӳ�ṹ��ͬ���˵����Խ�����Ӱ뾶ԽС����C����D��X���⻯��NH3��Z���⻯��HCl��Ӧ�����ɵĻ�����NH4Cl��笠��������������γ����Ӽ�����ԭ������ԭ���Թ��õ��Ӷ��γɹ��ۼ�����D��ȷ����ѡC��
����A��ȷ��B����Ԫ�صķǽ����Ա���ǿ�������̬�⻯������ȶ��ԣ�Z>W����B��ȷ��C��X��M����Ԫ���γɵļ����Ӱ뾶��С˳��X>M��N3����Na����������Ų���ͬ�����Ӳ�ṹ��ͬ���˵����Խ�����Ӱ뾶ԽС����C����D��X���⻯��NH3��Z���⻯��HCl��Ӧ�����ɵĻ�����NH4Cl��笠��������������γ����Ӽ�����ԭ������ԭ���Թ��õ��Ӷ��γɹ��ۼ�����D��ȷ����ѡC��


 ����ѵ�����⿼ϵ�д�
����ѵ�����⿼ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����84������Һ���ճ�������ʹ�ù㷺��������Һ��ɫ����Ư�����á�������Ч�ɷ������������е�һ�֣�����������
A.KMnO4B.Na2O2C.NH3��H2OD.NaClO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȡ����Ӧ���л���ѧ��һ����Ҫ�ķ�Ӧ����������ȡ����Ӧ����
A. �����������ڹ��յ������������ȱ���ķ�Ӧ
B. ��ϩ��������Ȼ�̼��Һ����1��2-��������ķ�Ӧ
C. ��ϩ��ˮ�����Ҵ��ķ�Ӧ
D. ��ϩ�������ɾ���ϩ�ķ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO��CO2�ǻ������糧�ͷų�����Ҫβ�����������Ի�����ɸ���Ӱ�죬��Ҳ����Ҫ�Ļ���ԭ�ϣ�����������ǻ��������о����ȵ���⡣
��1��CO ��Cl2�ڴ����������ºϳɹ���(COCl2)��ij�¶��£���2L ���ܱ�������Ͷ��һ������CO��Cl2���ڴ����������·�����Ӧ��CO(g)+Cl2(g)![]() COCl2(g) ��H=a kJ/ mol��
COCl2(g) ��H=a kJ/ mol��
��Ӧ�����вⶨ�IJ����������±���
t/ min | n (CO) /mol | n (Cl2) /mol |
0 | 1.20 | 0.60 |
1 | 0.90 | |
2 | 0.80 | |
4 | 0.20 |
�ٷ�Ӧ�ӿ�ʼ��2min ĩ��һ��ʱ���ڵ�ƽ������v(COCl2)=_____mol/(L��min)��
����2min~4min �䣬v (Cl2) ��______v (Cl2)�������������������=���������¶���K=_______��
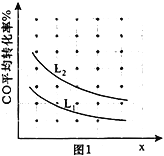
����֪X��L�ɷֱ�����¶Ȼ�ѹǿ��ͼ1��ʾL��ͬʱ��CO��ת������X�ı仯��ϵ��L��������������_____________��a_________0�����������������=������
��2���ڴ���������NO��CO ��ת��Ϊ�����壺
2CO(g)+2NO(g)![]() 2CO2(g)+N2(g) ��H
2CO2(g)+N2(g) ��H
����֪�� N2(g)+O2 (g)=2NO(g) ��H1= +180.0kJ/mol
2C(s)+O2 (g)=2CO (g) ��H2= -221.0 kJ/mol
2C(s)+2O2 (g)=2CO2 (g) ��H3= -787.0 kJ/mol
��H=____________��
���о���������ʹ�õ���������ʱ����������ȱ���������ѧ��Ӧ���ʡ�ijͬѧ���������ʵ�飨ʵ�������Ѿ����������ʵ����Ʊ��У���ʵ������Ŀ����___________________________��
ʵ���� | T���棩 | NO��ʼŨ�� (mol L-1) | CO��ʼŨ�� (mol L-1) | �����ıȱ����(m2 g-1) |
�� | 280 | 1.20��10-3 | 5.80��10-3 | 82 |
�� | 280 | 1.20��10-3 | 5.80��10-3 | 124 |
�� | 350 | 1.20��10-3 | 5.80��10-3 | 124 |
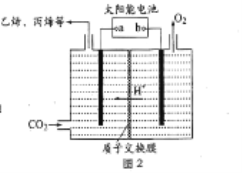
��3����ǿ���Եĵ����ˮ��Һ�У����Բ������缫�����CO2�ɵõ�����ȼ�ϣ���ԭ����ͼ2 ��ʾ��
��b Ϊ��Դ��_______��������������������ʱ�����ɱ�ϩ�ĵ缫��Ӧʽ��_________��
�ں����Ƽ�п�����CO2��NH3��NaCl��Ϊԭ�����Ƶ�NaHCO3�����������������֪H2CO3 ��Ka1=4.3��10-7 molL-1��Ka2=5.6��10-11 molL-1��NaHCO3��Һ�и�����Ũ���ɴ�С��˳��Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���� 100 mL 0.1 mol L-1 FeCl3 ��Һ�� 200 mL 0.3 mol L-1 NaCl ��Һ��Ϻ�(�����ǻ�Ϻ���Һ������ı仯��������Һ��Cl-��Ũ����
A.0.1 molL-1B.0.3 mol L-1C.0.6 mol L-1D.0.4mol L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪BaCO3��BaSO4�ܶȻ������ֱ�ΪKsp��5.1��10��9 mol2��L��2��Ksp��1.1��10��10 mol2��L��2����BaSO4�������ͣ�BaCO3���������͵���Ҫ�����ǣ� ��
A. BaSO4���ܶȻ�������BaCO3��С
B. SO![]() û�ж��ԣ�CO
û�ж��ԣ�CO![]() �ж���
���
C. BaSO4���ܶȴ�
D. θ������CO![]() ��ϣ�����CO2��H2O��ʹBaCO3���ܽ�ƽ�������ƶ���Ba2��Ũ�������������Ba2���ж�
��ϣ�����CO2��H2O��ʹBaCO3���ܽ�ƽ�������ƶ���Ba2��Ũ�������������Ba2���ж�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
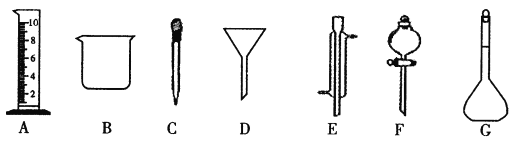
��1��д���������ƣ�E_____________��F_____________��
��2������ʵ��������õ�����D����_________(ѡ������ѡ��ı����ĸ )��
A������ˮ��CC14�Ļ���� B������ˮ�;ƾ��Ļ���� C������ˮ����ɰ�Ļ����
��.ij������ȤС����Ҫ200mL1mol/L��Na2CO3��Һ,��ش��������⣺
��1��������Һ����������ҩƷ��
Ӧ��ȡNa2CO3������ | Ӧѡ������ƿ�Ĺ�� | ������ƿ���Ҫ������������������ͼ�е�______��_____�������� |
��2������ʱ������ȷ�IJ���˳����(����ĸ��ʾ��ÿ������ֻ����һ��)______________��
A��������ȴ����Һ�ز�����ע������ƿ��
B����������ƽȷ��������Na2CO3�������������ձ��У��ټ�������ˮ���ò���������������ʹ���ܽ�(��Ҫʱ�ɼ���)
C��������ˮϴ���ձ�2-3�Σ�ϴ��Һ��ע������ƿ�У���
D�����ý�ͷ�ιܼ�ˮ��ʹ��Һ��Һ��ǡ����̶�������
E.������ƿ�ǽ�����ҡ��
F.����������ƿ��С�ļ�ˮ��ֱ��Һ��ӽ��̶�1��2cm��
��3�������������������������ҺŨ�Ƚ��к�Ӱ��(����ƫ��������ƫ����������Ӱ����)?
û�н���C����________��������Һʱ������ƿδ����_________������ʱ���ӿ̶���_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�����о�������Ļ�ѧ�ɷ�ʱ����������������Ԫ���ڷ�����綼����,��һ��ʵ˵�� �� ��
A. �����ͷ������û������ B. ��������������Դ�ڷ�����
C. �����ͷ���������ͳһ�� D. �����ͷ��������в�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��TiO2��TiCl4��Ϊ��Ҫ�Ĺ�ҵԭ�ϡ���֪��
��.TiCl4(g)+O2(g)![]() TiO2(s)+2Cl2(g) ��H1=-175.4kJ��mol-1
TiO2(s)+2Cl2(g) ��H1=-175.4kJ��mol-1
��.2C(s)+O2(g)![]() 2CO(g) ��H2= -220.9kJ��mol-1
2CO(g) ��H2= -220.9kJ��mol-1
��ش��������⣺
��1��TiCl4(g)��CO(g)��Ӧ����TiO2(s)��C(s)���������Ȼ�ѧ����ʽΪ_____________________�������¶ȣ��Ը÷�Ӧ��Ӱ��Ϊ___________________________________��
��2������Ӧ����淴Ӧ��ܱ�ʾΪEkJ��mol-1����E________220.9(�>����<����=��)��
��3��t��ʱ����10 L�����ܱ������г���1molTiCl4��2 molO2��������Ӧ��5min�ﵽƽ��ʱ���TiO2�����ʵ���Ϊ0.2 mol��
��0~5 min �ڣ���Cl2��ʾ�ķ�Ӧ����v(Cl2)=__________��
��TiCl4��ƽ��ת����a=__________________��
�����д�ʩ�����ܼӿ��淴Ӧ������������TiCl4��ƽ��ת���ʵ���__________����ѡ����ĸ����
A����С�����ݻ� B��������� C�����������TiO2 D������O2Ũ��
��t��ʱ����10 L�����ܱ������г���3 mol TiCl4��һ����O2�Ļ�����壬������Ӧ�����������ƽ��ת����(a)����ʼ�����ʵ���֮��(![]() )�Ĺ�ϵ��ͼ��ʾ��
)�Ĺ�ϵ��ͼ��ʾ��
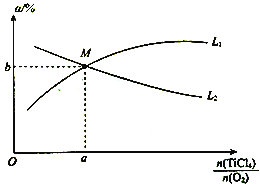
�ܱ�ʾTiCl4ƽ��ת���ʵ�����Ϊ__________(�L1����L2��)��M�������Ϊ___________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com