
| A. | CH3COOH | B. | CuSO4 | C. | K2SO4 | D. | NaHCO3 |
分析 根据反应的实质为Zn+2H+═Zn2++H2↑,为了减缓反应速率,但又不影响生成氢气的总量,则减小氢离子的浓度但不能改变氢离子的物质的量即可,注意Zn过量,以此来解答.
解答 解:A.加入CH3COOH溶液,溶液被稀释,溶液中氢离子降低,反应速率减小,但电离出氢离子物质的量增大,所以生成氢气总量增大,故A错误;
B、Zn可以置换出Cu,构成原电池,加快反应速率,故B错误;
C.加入硫酸钾溶液,氢离子浓度降低,反应速率减小,但氢离子总量不变,所以生成氢气总量不变,故C正确;
D.加入碳酸氢钠溶液,与盐酸反应是二氧化碳,氢离子总量较小,生成氢气的量减少,故D错误,
故选C.
点评 本题考查化学反应速率影响因素,比较基础,需注意生成氢气的量不变,注意B选项构成原电池,加快反应速率.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 427℃时该反应的平衡常数为9.4,则该反应的△H>0 | |
| B. | 800℃下,该反应的化学平衡常数为0.25 | |
| C. | 同温下,若继续向该平衡体系中通入1.0mol的H2O(g),则平衡时H2O(g)转化率为66.7% | |
| D. | 同温下,若继续向该平衡体系中通入1.0mol的CO(g),则平衡时H2O(g)物质的量分数为11.1% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3OH的燃烧热为192.9kJ/mol | |
| B. | 反应①中的能量变化如图所示: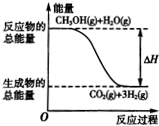 | |
| C. | 根据②推知反应CH3OH(l)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)的△H>-192.9kJ/mol | |
| D. | CH3OH转变成H2的过程一定要吸收能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,10mL0.02 mol•L-1 HCl溶液与10mL0.02 mol•L-1 Ba(OH)2溶液充分混合,若混合后溶液的体积为20mL,则溶液的pH=11 | |
| B. | 在0.1 mol•L-1CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+) | |
| C. | 中和物质的量浓度与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 | |
| D. | 配制三氯化铁溶液时应将三氯化铁溶于浓盐酸,再加水稀释至所需浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、OH一、HCO3- Cu2+ | B. | NH4+、NO3-、OH-、K+ | ||
| C. | H+、K+、CO32-、SO42- | D. | Ba2+、OH一、C1-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所得溶液的质量分数:w=36.5c/1000 | |
| B. | 36.5 gHCl气体在标准状况下占有的体积约为22.4L | |
| C. | 所得溶液的物质的量浓度:c=1 mol•L-1 | |
| D. | 所得溶液中含有NA个HCl分子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com