
在10L容器中,加入2mol的SO2(g)和2mol的NO2(g),保持温度恒定,发生反应:SO2(g)+ NO2(g) SO3(g)+NO(g)。当达到平衡状态时,测得容器中SO2(g)的转化率为50%。
SO3(g)+NO(g)。当达到平衡状态时,测得容器中SO2(g)的转化率为50%。
试求:该温度下、该容器中,再继续加入1mol的SO2(g),则:
(1)化学平衡将向________方向移动,NO2的转化率将____________(填“增大” 、“不变”或“减小”);
(2)经计算,当达到新的平衡状态时,容器中SO2(g)的浓度是___________mol/L;
(3)整个过程中,SO2的转化率由50%变为___________%,NO2的转化率由__________%变为___________%。
(4)计算结果给我们的启示是:增大一种反应物物的用量,其转化率将_______________(填“增大” 、“不变”或“减小”)另一反应物的转化率将____________(填“增大” 、“不变”或“减小”)。现实生产中的意义是:可以通过增大________的用量,来提高成本高的反应物的利用率。
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源:2016-2017学年浙江省嘉兴市七校高一上期中化学试卷(解析版) 题型:选择题
某位同学配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )
A. 向容量瓶中加水未到刻度线
B. 所用NaOH已经潮解
C. 有少量NaOH溶液残留在烧杯里
D. 用带游码的托盘天平称2.4 g NaOH时误用了“左码右物”方法
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市红桥区高一上学期期中化学试卷(解析版) 题型:推断题
某固体混合物可能由KCl、NaNO3、K2SO4、CuCl2、CaCl2、K2CO3中的一种或几种混合而成,为鉴定其组成,依次进行如下实验:
(1)混合物中加入足量水得一无色透明溶液,
(2)上述溶液中滴加 BaCl 2有白色沉淀产生,
2有白色沉淀产生,
(3)过滤,然后向上述白色沉淀加盐酸时,沉淀全部溶解,
(4)往滤液中加AgNO3溶液时有白色沉淀产生且白色沉淀不溶于稀硝酸.
①试判断:肯定存在的物质有__________;肯定不存在的物质有_________;可能存在的物质有__________.
②写出第(3)步反应的离子方程式_____________________
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市红桥区高一上学期期中化学试卷(解析版) 题型:选择题
某溶液中含有较大量的Cl-、CO32-、OH-等3种阴离子,如果只取一次该溶液就能够分别将 3 种阴离子依次检验出来,下列实验操作顺序正确的是( )
3 种阴离子依次检验出来,下列实验操作顺序正确的是( )
①滴加Mg(NO3)2溶液;②过滤;③滴加AgNO3溶液;④滴加Ba(NO3)2溶液
A. ①②④②③ B. ④②①②③ C. ①②③②④ D. ④②③②①
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市河东区高二上学期期中质检化学试卷(解析版) 题型:选择题
25 ℃和1.01×105 Pa时,反应2N2O5(g)=4NO2(g)+O2(g) ΔH=+56.76 kJ/mol自发进行的原因是
A.是吸热反应 B.是放热反应
C.是熵减小的反应 D.熵增大效应大于能量效应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市河东区高二上学期期中质检化学试卷(解析版) 题型:选择题
反应4CO(g)+2NO2(g) N2(g)+4CO2(g)开始进行时,CO的浓度为4 mol/L,N2的浓度为0,2 min后测得N2的浓度为0.6 mol/L,则此段时间内,下列反应速率表示正确的是
N2(g)+4CO2(g)开始进行时,CO的浓度为4 mol/L,N2的浓度为0,2 min后测得N2的浓度为0.6 mol/L,则此段时间内,下列反应速率表示正确的是
A.v(CO)=1.2 mol/(L·s) B.v(NO2)=0.3 mol/(L·min)
C.v(N2)=0.6 mol/(L·min) D.v(CO2)=1.2 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源:2017届贵州省高三上月考三化学试卷(解析版) 题型:填空题
Ⅰ.请回答:
(1)Na2O2的电子式 。
(2)除去FeCl3中少量FeCl2,除杂过程涉及的化学反应方程式 。
(3)往饱和Na2CO3溶液中通入CO2气体,溶液中出现白色浑浊,写出该反应的离子方程式 。
(4)双氧水能使酸性高锰酸钾溶液褪色,请完成以下相关反应的离子方程式:
( )MnO4-+( )H2O2+ =( )Mn2++( )H2O+ 。
Ⅱ.无机化合物A 和NaH都是重要的还原剂,遇水都强烈反应。一定条件下,2.40g NaH与气体B反应生成3.90g化合物A和 2.24L(已折算成标准状况)的H2。已知气体B可使湿润红色石蕊试纸变蓝。已知:NH3+ NH3=NH4++NH2-
请回答下列问题:
(1)A的化学式是 。
(2)A与足量盐酸发生非氧化还原反应的化学方程式 。
(3)在高温下氢化钠(NaH)可将四氯化钛(TiC14)还原成金属钛,该反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高二上期中化学卷(解析版) 题型:选择题
已知化学反应A2(g)+ B2(g) = 2AB(g)的能量变化如图所示,判断下列叙述中正确的是
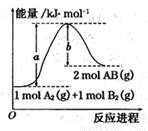
A.每生成2分子AB吸收bkJ热量
B.断裂1molA—A和1molB—B键,放出akJ能量
C.该反应中反应物的总能量高于生成物的总能量
D.该反应热△H=+(a-b)kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com