
| A. | 该反应中氧化性:Co2O3>Cl2 | |
| B. | 参加反应的HCl全部被Co2O3氧化 | |
| C. | 每生成1摩尔氯气,消耗1摩尔Co2O3 | |
| D. | 制备相同量的氯气,所需Co2O3质量比MnO2多 |
分析 用Co2O3代替MnO2制备Cl2,反应后Co元素以 Co2+的形式存在,则反应方程式为Co2O3+6HCl(浓)═2CoCl2+Cl2↑+3H2O中,Co元素的化合价由+3价降低为+2价,Cl元素的化合价由-1价升高到0价,以此来解答.
解答 解:A.Co元素的化合价由+3价降低为+2,则氧化剂为Co2O3,Cl元素被氧化,则Cl2为氧化产物,所以氧化性:Co2O3>Cl2,故A正确;
B.由方程式Co2O3+6HCl(浓)═2CoCl2+Cl2↑+3H2O可知,参加反应的HCl部分被Co2O3氧化,故B错误;
C.由方程式Co2O3+6HCl(浓)═2CoCl2+Cl2↑+3H2O可知,每生成1摩尔氯气,消耗1摩尔Co2O3,故C正确;
D.由方程式Co2O3+6HCl(浓)═2CoCl2+Cl2↑+3H2O和MnO2+4HCl(浓)═MnCl2+Cl2↑+2H2O,可知,制备相同量的氯气,所需Co2O3和MnO2的物质的量相同,所以Co2O3质量比MnO2多,故D正确;
故选B.
点评 本题考查氧化还原反应,明确元素的化合价变化及氧化还原反应中的概念即可解答,题目难度不大.


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:填空题
 、
、 、
、 ;属于芳香醚类的是C6H5OCH3.
;属于芳香醚类的是C6H5OCH3. 、
、 或
或 (写两种);
(写两种);查看答案和解析>>
科目:高中化学 来源: 题型:实验题
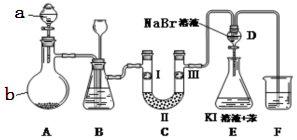
| 实验现象 | 原因 |
| 溶液最初从紫色逐渐变为红色 | 氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | 氯气与水反应生成HClO具有漂白性 |
| 然后溶液从无色逐渐变为浅黄绿色 | 过量氯气溶解于水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当a=1时,发生的离子反应为:OH-+H+═H2O | |
| B. | 当a=2时,发生的离子反应为:OH-+CO32-+2H+═HCO3-+H2O | |
| C. | 当1<a<2,反应后的溶液中CO32-和HCO3-的物质的量之比为:(a×10-2-0.01):(0.02-a×10-2) | |
| D. | 当a≥3时,发生的离子反应:3H++OHˉ+CO32-═2H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
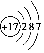 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由于铜盐能杀死某些细菌,并能抑制藻类生长,因此游泳场馆常用硫酸铜作池水消毒剂 | |
| B. | 高炉炼铁得到纯度高的铁,加入其他金属炼制得到钢 | |
| C. | 焙制糕点的发酵粉主要成分之一是碳酸氢钠,它也是治疗胃酸过多的一种药剂 | |
| D. | 分子筛常用于分离、提纯气体或液体混合物,还可作干燥剂、离子交换剂、催化剂及催化剂载体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com