
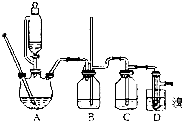
 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/0C | 78.5 | 132 | 34.6 |
| 熔点/0C | -130 | 9 | -116 |
| 溶解性 | 易溶水 | 难溶水 | 微溶于水 |
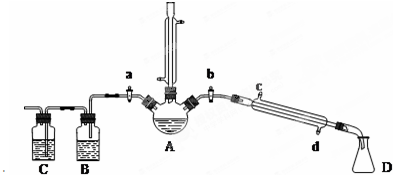
分析 实验室制备1,2-二溴乙烷的反应原理为:A装置中乙醇发生消去反应生成乙烯:CH3CH2OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2↑+H2O,B装置可以作安全瓶,要以防倒吸,由于有副反应的发生,生成的乙烯中有酸性气体,所以C装置用氢氧化钠吸收乙烯中的酸性杂质气体,然后乙烯与溴发生加成反应生成1,2-二溴乙烷:CH2=CH2+Br2→BrCH2CH2Br,产物中混有的溴单质可以用氢氧化钠溶液除去,
(1)乙醇在浓硫酸140℃的作用下发生分子间脱水;
(2)浓硫酸具有强氧化性,可能氧化乙醇中的碳;
(3)乙烯和溴水发生了加成反应;
(4)根据1,2-二溴乙烷和水的密度相对大小解答;
(5)1,2-二溴乙烷熔点为9℃,冷却容易析出晶体,堵塞玻璃导管,B为安全瓶,可以防止倒吸,根据长导管中内外液面高低变化,可以判断是否发生堵塞;
(6)溴易挥发,该反应放热;
(7)根据反应方程式CH2=CH2+Br2→BrCH2CH2Br可知,16.0g的溴和足量的乙醇制备1,2-二溴乙烷的质量为18.8g,根据产率=$\frac{实际产量}{理论产量}$×100%计算.
解答 解:实验室制备1,2-二溴乙烷的反应原理为:A装置中乙醇发生消去反应生成乙烯:CH3CH2OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2↑+H2O,B装置可以作安全瓶,要以防倒吸,由于有副反应的发生,生成的乙烯中有酸性气体,所以C装置用氢氧化钠吸收乙烯中的酸性杂质气体,然后乙烯与溴发生加成反应生成1,2-二溴乙烷:CH2=CH2+Br2→BrCH2CH2Br,产物中混有的溴单质可以用氢氧化钠溶液除去,
(1)乙醇在浓硫酸140℃的条件下,发生分子内脱水,生成乙醚,
故答案为:d;
(2)浓硫酸具有强氧化性,将乙醇氧化成二氧化碳,自身被还原成二氧化硫,二氧化碳、二氧化硫能和氢氧化钠溶液反应,
故答案为:c;
(3)乙烯和溴水发生加成反应生成1,2-二溴乙烷,1,2-二溴乙烷为无色,
故答案为:溴的颜色完全褪去;
(4)1,2-二溴乙烷和水不互溶,1,2-二溴乙烷密度比水大,
故答案为:下;
(5)1,2-二溴乙烷熔点为9℃,冷却容易析出晶体,堵塞玻璃导管,B为安全瓶,可以防止倒吸,根据B中长导管内外液面高低变化,可以判断是否发生堵塞,
故答案为:防止倒吸、判断装置是否堵塞;
(6)溴在常温下,易挥发,乙烯与溴反应时放热,溴更易挥发,冷却可避免溴的大量挥发,但1,2-二溴乙烷的凝固点9℃较低,不能过度冷却,
故答案为:乙烯与溴反应时放热,冷却可避免溴的大量挥发;1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使气路堵塞;
(7)根据反应方程式CH2=CH2+Br2→BrCH2CH2Br可知,16.0g的溴和足量的乙醇制备1,2-二溴乙烷的质量为18.8g,所以产率=$\frac{实际产量}{理论产量}$×100%=$\frac{9.4g}{18.8g}$×100%=50%,
故答案为:50%.
点评 该题较为综合,主要考查了乙醇制备1,2-二溴乙烷,掌握相关物质的基本化学性质,是解答本题的关键,平时须注意积累相关反应知识,难度中等.


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等浓度的溶液中滴入稀盐酸.放出气体的快慢Na2C03<NaC03 | |
| B. | 热稳定性Na2C03<NaHC03 | |
| C. | 常温时水溶性Na2C03<NaHC03 | |
| D. | 相对分子质量Na2C03<NaHC03 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | 熔点/0C | 沸点/0C |
| 1-丁醇 | -89.5 | 117.3 |
| 1-溴丁烷 | -112.4 | 101.6 |
| 丁醚 | -95.3 | 142.4 |
| 1-丁烯 | -185.3 | -6.5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com