
| A | B | D | E | |
| »ÆŗĻ¼Ū | -4 | -2 | -3 | -2 |
| µēøŗŠŌ | 2.5 | 2.5 | 3.0 | 3.5 |
 ×12=4£¬
×12=4£¬ ×6+8×
×6+8× =4£¬¶žÕß±ČÖµĪŖ1£ŗ1£¬Ōņ»ÆѧŹ½ĪŖCoO£¬
=4£¬¶žÕß±ČÖµĪŖ1£ŗ1£¬Ōņ»ÆѧŹ½ĪŖCoO£¬ 2[Co£ØCN£©6]3-+H2”ü+2OH-£¬¹Ź“š°øĪŖ£ŗ2[Co£ØCN£©6]4-+2H2O
2[Co£ØCN£©6]3-+H2”ü+2OH-£¬¹Ź“š°øĪŖ£ŗ2[Co£ØCN£©6]4-+2H2O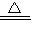 2[Co£ØCN£©6]3-+H2”ü+2OH-£®
2[Co£ØCN£©6]3-+H2”ü+2OH-£®

 ŌĘÄĻŹ¦“óø½Š”Ņ»ĻßĆūŹ¦ĢįÓÅ×÷ŅµĻµĮŠ“š°ø
ŌĘÄĻŹ¦“óø½Š”Ņ»ĻßĆūŹ¦ĢįÓÅ×÷ŅµĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ




²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ




²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ


| ||
| ||
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ


²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
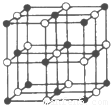
ŅŃÖŖA”¢B”¢C”¢D”¢EŹĒ¶ĢÖÜĘŚÖŠµÄ5ÖÖ·Ē½šŹōŌŖĖŲ£¬ĖüĆĒµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó”£AŌŖĖŲŌ×ÓŠĪ³ÉµÄĄė×ÓŗĖĶāµē×ÓŹżĪŖĮć£¬C”¢DŌŚŌŖĖŲÖÜĘŚ±ķÖŠ“¦ÓŚĻąĮŚµÄĪ»ÖĆ£¬BŌ×ÓµÄ×īĶā²ćµē×ÓŹżŹĒÄŚ²ćµē×ÓŹżµÄ2±¶”£EŌŖĖŲÓėDŌŖĖŲĶ¬Ö÷×壻EµÄµ„ÖŹĪŖ»ĘÉ«¾§Ģ壬Ņ×ČÜÓŚ¶žĮņ»ÆĢ¼”£
£Ø1£©ĒėŠ“³öĻĀĮŠŌŖĖŲµÄŌŖĖŲ·ūŗÅ
A£ŗ C£ŗ E£ŗ £Øø÷1·Ö£©
£Ø2£©»³öEµÄŅõĄė×Ó½į¹¹Ź¾ŅāĶ¼£ŗ (1·Ö)
£Ø3£©AµÄµ„ÖŹŗĶCµÄµ„ÖŹŌŚŅ»¶ØĢõ¼žĻĀÉś³É»ÆŗĻĪļX£¬ÓƵē×ÓŹ½±ķŹ¾XµÄŠĪ³É¹ż³Ģ £Ø2·Ö£©£»ĻņXµÄĖ®ČÜŅŗÖŠµĪČė·ÓĢŖČÜŅŗ£¬»į¹Ū²ģµ½ £Ø1·Ö£©
£Ø4£©½«9æĖBµÄµ„ÖŹŌŚ×ćĮæµÄDµÄµ„ÖŹÖŠČ¼ÉÕ£¬ĖłµĆĘųĢåĶØČė1L 1mol”¤L-1
NaOHČÜŅŗÖŠ£¬ĶźČ«ĪüŹÕŗó£¬ČÜŅŗÖŠ“óĮæ“ęŌŚµÄČÜÖŹŹĒ £¬
ĒŅĪļÖŹµÄĮæĪŖ £Øø÷2·Ö£©
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com