
| ������� | �¶�/�� | ��ʼʱ���ʵ���/mol | ƽ��ʱ���ʵ���/mol | ||
| N2 | H2 | NH3 | NH3 | ||
| �� | 500 | 1 | 3 | 0 | 0.5 |
| �� | 500 | 0.6 | 1.8 | 0 | |
| �� | 550 | 0 | 0 | 2 | a |
| A�� | �����١����з�Ӧ��ƽ�ⳣ������� | |
| B�� | ��ƽ��ʱ����������H2��ת���ʴ���25% | |
| C�� | a��0.5 | |
| D�� | ��ʼʱ���������г���1 mol N2��2 mol H2��0.5 mol NH3����Ӧ�����淴Ӧ������� |
���� A��ƽ�ⳣ����Ӱ���������¶ȣ��¶�һ����ƽ�ⳣ�����䣻
B�������١�������ں�ѹ�����½��У��������з�Ӧ���ת������ȣ���Ϊ�����������൱��ƽ��ʱ�������������ƽ����ƶ����жϷ�Ӧ���ת���ʱ仯��
C���ٺ͢۵���ʼ��������ȫת��������¶���ͬ�γɵ�ƽ��Ϊ��Чƽ�⣬�����¶Ȳ�ͬ�����ڵ�Чƽ��Ļ����ϣ��ı��¶ȣ������¶ȱ仯���ж�ƽ���ƶ��������ж�ƽ��״̬�ı仯��
D���ȼ������ƽ�ⳣ��������Qc��ƽ�ⳣ���Ĺ�ϵ���жϷ�Ӧ���еķ��ɣ�
��� �⣺A�������١����з�Ӧ�¶���ͬ���ﵽƽ��ʱ��ƽ�ⳣ����ȣ���A����
B���������дﵽƽ��ʱH2��ת����=$\frac{0.5mol��\frac{3}{2}}{3}$��100%=25%�������١��ڵ���ʼ״̬�뻯ѧ�����������ȣ�����ں�ѹ�����½��У��������з�Ӧ���ת������ȣ�H2��ת���ʾ�Ϊ25%����Ϊ�����������൱�ڽ��������н��е�ƽ��״̬�����������ʱƽ�������ƶ�����Ӧ���ת���ʽ��ͣ���H2��ת����С��25%����B����
C���ٺ͢۵���ʼ��������ȫת��������¶Ⱦ�Ϊ500�棬��ʱ�γɵ�ƽ��Ϊ��Чƽ�⣬NH3��ƽ�����ʵ���Ϊ0.5mol�����¶�Ϊ550�棬�൱�ڴ�ƽ�����£�ƽ�������ƶ���NH3�����ʵ�����С����a��0.5����C��ȷ��
D����������N2��g��+3H2��g��?2NH3��g���ﵽƽ��ʱ��NH3��ƽ�����ʵ���Ϊ0.5mol����N2�����ʵ���Ϊ1mol-0.25mol=0.75mol��H2�����ʵ���Ϊ3mol-0.25mol��3=2.25mol����ʱƽ�ⳣ��K=$\frac{{c}^{2}��N{H}_{3}��}{{c}^{3}��{H}_{2}����c��{N}_{2}��}$=$\frac{��\frac{0.5mol}{0.25L}��^{2}}{��\frac{2.25mol}{0.25L}��^{3}����\frac{0.75mol}{0.25L}��}$=$\frac{4}{2187}$����ʼʱ���������г���1 mol N2��2 mol H2��0.5 mol NH3����ʱQc=$\frac{{c}^{2}��N{H}_{3}��}{{c}^{3}��{H}_{2}����c��{N}_{2}��}$=$\frac{��{\frac{0.5mol}{0.25L}��}^{2}}{��\frac{2mol}{0.25L}��^{3}��\frac{1mol}{0.25L}��}$=$\frac{4}{2048}$��$\frac{4}{2187}$����Ӧ�����淴Ӧ������У���D��ȷ��
��ѡCD��
���� ����Ϊ��ѧƽ��Ŀ��飬�漰��Чƽ����ۺ�Ӧ�á���ѧƽ��ļ��㼰��ѧƽ�ⳣ����Ӧ�ã��ѵ�Ϊ��Чƽ��Ľ�����Dѡ��ѵ��еȣ����ӻ���ѧϰ�ǽ���֮����


 �����������Ů��ͯ������ϵ�д�
�����������Ů��ͯ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��SO2ͨ��Ʒ����Һ�У���Һ�ĺ�ɫ��ȥ | |
| B�� | ��5���Ȼ���������Һ����25mL��е�����ˮ�м������ȣ�Һ�����ɫ | |
| C�� | ��Fe2��SO4��3��Һ�еμ�NaOH��Һ�����ɺ��ɫ���� | |
| D�� | ����������Һ��������Cu��OH��2����Һ���������ڣ�����ש��ɫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �϶�����I- | B�� | �϶�����Na+ | ||
| C�� | �϶�����SO42-�϶�����SO32- | D�� | ���ܿ϶��Ƿ���SO42 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
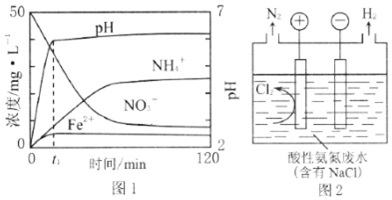
 ij��ѧС�����������ȼ�ϵ�ؽ���ˮ�е��Ҷ���[H2N��CH2��2NH2]�����ɻ����Ѻõ����ʣ�����ԭ����ͼ��ʾ��a��b��Ϊʯī�缫�������з�����ȷ���ǣ�������
ij��ѧС�����������ȼ�ϵ�ؽ���ˮ�е��Ҷ���[H2N��CH2��2NH2]�����ɻ����Ѻõ����ʣ�����ԭ����ͼ��ʾ��a��b��Ϊʯī�缫�������з�����ȷ���ǣ�������| A�� | a �缫������Ӧ��H2NCH2CH2NH2+16e-+4H2O�T2CO2��+N2��+16H+ | |
| B�� | ���ӽ���Ĥ��H+���������ƶ� | |
| C�� | �õ�������������½���ѧ��ת��Ϊ���� | |
| D�� | ��ʼ�ŵ�ʱb������pH���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������������ԣ�����������ʴ�̼� | |
| B�� | �ɱ�����ʱ���ȣ������������ | |
| C�� | ����ˮ��Ӧ�������ڳ�ȥ�Ҵ���������ˮ | |
| D�� | ������������ˮ��������ľ�ķ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������̾���ǿ�����ԣ��ܽ�˫��ˮ����Ϊ���� | |
| B�� | ͭ�Ľ�����Ա�����������ͭ������������Ũ���� | |
| C�� | ̿���л�ԭ�ԣ�����̿�ڸ����½��������軹ԭΪ�� | |
| D�� | �����dz������л��ܼ����������ѻ���������ȡ��ˮ�е��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com