
【题目】有A、B、C、D、E、F六种主族元素,已知:(a)A原子有四个电子层,其K、L层电子数分别与N、M层电子数相等;(b)B、C原子核外电子层数比A原子少1,B的最高正价和最低负价的代数和等于零,C的简单气态氢化物的化学式是H2C;(c)D、E的阴离子都带有一个单位的负电荷,D的阴离子的电子层结构与氩原子相同,E元素没有对应的含氧酸;(d)F与A位于同一周期且是六种元素中原子半径最大的元素。
(1)写出六种元素的名称:A___;B___;C___;D___;E___;F___。
(2)A、C、D、F四种元素的简单离子的半径由大到小的顺序为____(用离子符号表示)。
(3)B、C、D三种元素的简单气态氢化物的稳定性由强到弱的顺序为___(用化学式表示)。
【答案】钙 硅 硫 氯 氟 钾 S2->Cl->K+>Ca2+ HCl>H2S>SiH4
【解析】
A原子有四个电子层,其K、L层电子数分别与N、M层电子数相等,则A为钙元素;B、C原子核外电子层数比A原子少1,两种元素处于第三周期,B的最高正价和最低负价的代数和等于零,则B为硅元素,C的简单气态氢化物的化学式是![]() ,则C为硫元素;D、E的阴离子都带有一个单位的负电荷,D的阴离子的电子层结构与氩原子相同,则D为氯元素,E元素没有对应的含氧酸,则E为氟元素;F与A位于同一周期且是六种元素中原子半径最大的元素,则F为钾元素。
,则C为硫元素;D、E的阴离子都带有一个单位的负电荷,D的阴离子的电子层结构与氩原子相同,则D为氯元素,E元素没有对应的含氧酸,则E为氟元素;F与A位于同一周期且是六种元素中原子半径最大的元素,则F为钾元素。
(1)分析可知,A~F分别为钙、硅、硫、氯、氟、钾;
(2)A、C、D、F四种元素的简单离子分别为Ca2+、S2-、Cl-、K+,四种离子的电子层结构相同,则核电荷数越大,离子半径越小,故离子半径:S2->Cl->K+>Ca2+;
(3)金属性:Cl>S>Si,故简单气态氢化物的稳定性:HCl>H2S>SiH4。


 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源: 题型:
【题目】现有a~g7种短周期主族元素,它们在元素周期表中的相对位置如图所示,请回答下列问题:
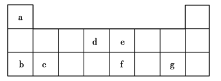
(1)下列选项中,元素的原子间最容易形成离子键的是______(填序号,下同),元素的原子间最容易形成共价键的是______。
A.![]() 和
和![]() B.
B.![]() 和
和![]() C.
C.![]() 和
和![]() D.
D.![]() 和
和![]()
(2)下列由a~g7种元素原子形成的各种分子中,所有原子最外层都满足8电子稳定结构的是______(填序号)。
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
(3)由题述元素中的3种非金属元素形成的AB型离子化合物的电子式为______。
(4)![]() 与
与![]() 可形成一种化合物
可形成一种化合物![]() ,其含有的化学键类型为______,其与过量稀盐酸反应的化学方程式为______。
,其含有的化学键类型为______,其与过量稀盐酸反应的化学方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为原子序数依次增大的短周期主族元素。X分别与Y、Z、W结合形成质子数相同的甲、乙、丙三种分子。丁为无色气体,遇空气变红棕色;丙的水溶液可刻蚀玻璃。
上述物质有如图转化关系:

下列说法错误的是
A. 四种元素形成的单质中W的氧化性最强
B. 甲、乙、丙中沸点最高的是丙
C. 甲常用作致冷剂
D. 甲、乙分子均只含极性共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】晶体的性质与晶体类型和结构紧密相关。
(1)氯酸钾熔化时克服的作用力是______;二氧化硅熔化时克服的作用力是______;碘升华时克服的作用力是______。三种晶体的熔点由高到低的顺序是______(填化学式)。
(2)下列六种晶体:①![]() ,②
,②![]() ,③
,③![]() ,④
,④![]() ,⑤
,⑤![]() ,⑥金刚石,它们的熔点从低到高的顺序为______(填序号)。
,⑥金刚石,它们的熔点从低到高的顺序为______(填序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应2NO2N2O4(g) H<0。将一定量的NO2充入注射器中并密封,改变活塞位置的过程中,气体透光率随时间的变化如图所示(气体颜色越深,透光率越小)。下列说法不正确的是
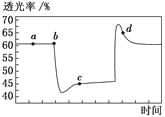
A.b 点的操作是压缩注射器
B.c 点与a点相比,c(NO2)增大、c(N2O4)减小
C.d 点:υ(正)<υ(逆)
D.若在c点将温度降低,其透光率将增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化碱法是工业上制备Na2S2O3的方法之一,反应原理为:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2(该反应△>0)某研究小组在实验室用硫化碱法制备Na2S2O3·5H2O流程如下。

(1)吸硫装置如图所示。

①装置B的作用是检验装置中SO2的吸收效率,B中试剂是________,表明SO2吸收效率低的实验现象是B中溶液________________。
②为了使SO2尽可能吸收完全,在不改变A中溶液浓度、体积的条件下,除了及时搅拌反应物外,还可采取的合理措施是_______、_______。(写出两条)
(2)假设本实验所用的Na2CO3含少量NaCl、NaOH,设计实验方案进行检验。(室温时CaCO3饱和溶液的pH=12), 限用试剂及仪器:稀硝酸、AgNO3溶液、CaCl2溶液、Ca(NO3)2溶液、酚酞溶液、蒸馏水、pH计、烧杯、试管、滴管、
序号 | 实验操作 | 预期现象 | 结论 |
① | 取少量样品于试管中,加入适量蒸馏水,充分振荡溶解,_________。 | 有白色沉淀生成 | 样品含NaCl |
② | 另取少量样品于烧杯中,加入适量蒸馏水,充分振荡溶解,_________。 | 有白色沉淀生成,上层清液pH>10.2 | 样品含NaOH |
(3)Na2S2O3溶液是定量实验中的常用试剂,测定其浓度的过程如下:
第一步:准确称取ag KIO3(相对分子质量:214)固体配成溶液,
第二步:加入过量KI固体和H2SO4溶液,滴加指示剂,
第三步:用Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液溶液的体积为vmL 则c(Na2S2O3溶液)=_______mol·L-1。(只列出算式,不作运算)
已知:IO3-+I-+6H+=3I2+3H2O ,2S2O32-+I2=S4O62-+2I- 某同学第一步和第二步的操作都很规范,第三步滴速太慢,这样测得的Na2S2O3的浓度可能_____(填“不受影响”、“偏低”或“偏高”) ,原因是________(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答:
(1)室温下,使用pH计测定0.1mol/LNH4Cl溶液的pH=5.12(如图1)由此可以得到的结论是___(填字母)。

a.NH3·H2O是弱碱
b.溶液中c(H+)>c(OH-)
c.NH4+水解是吸热反应
d.由H2O电离出的c(H+)<10-7mol/L
e.物质的量浓度相等的氨水和盐酸等体积混合,溶液pH=7
(2)室温下,用0.10mol/LNaOH溶液分别滴定20.00mL0.10mol/L的盐酸和醋酸,滴定曲线如图2所示。
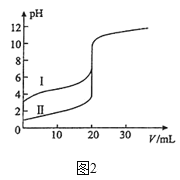
①表示滴定盐酸的曲线是____(填序号)。若此实验选用酚酞为指示剂,则滴定到达终点的现象是____。若用标准NaOH溶液测定未知盐酸溶液的浓度,下列实验操作会使实验结果偏低的是____。
a.锥形瓶用待测液润洗后再注入待测液
b.碱式滴定管滴定前有气泡,滴定后无气泡
c.碱式滴定管滴定前仰视读数,滴定后平视读数
②在滴定醋酸溶液的过程中:
V(NaOH)=10.00mL时,溶液中离子浓度由大到小的顺序为____。当c(Na+)=c(CH3COO-)+c(CH3COOH)时,溶液pH____7(填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铷(![]() )是37号元素,其相对原子质量是85.5,与钠位于同一主族,回答下列问题:
)是37号元素,其相对原子质量是85.5,与钠位于同一主族,回答下列问题:
(1)铷位于第______周期,其原子半径比钠元素的原子半径______(填“大”或“小”)。
(2)铷单质性质活泼,写出在点燃条件下它与氯气反应的化学方程式:________________________;铷单质易与水反应,反应的离子方程式为________________________,实验表明铷与水反应比钠与水反应______(填“剧烈”或“缓慢”);反应过程中铷在水______(填“面”或“底”)与水反应,原因是__________________。
(3)同主族元素的同类化合物的化学性质相似,写出过氧化铷与![]() 反应的化学方程式:________________。
反应的化学方程式:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业甲醇的质量分数可以用下列方法测定:
①在稀H2SO4中甲醇被Cr2O72-氧化成CO2和H2O,反应式为:CH3OH+Cr2O72-+8H+=CO2↑+2Cr3++6H2O;
②过量的Cr2O72-可用Fe2+与之完全反应:
Cr2O72﹣+ Fe2++ H+- Cr3++ Fe3++ H2O
现有0.12g工业甲醇,在H2SO4溶液中与25mL0.2molL-1K2Cr2O7溶液反应,多余的K2Cr2O7再用1molL-1FeSO4与其反应,结果用去FeSO4溶液9.6mL。
(1)配平第②步中离子方程式___。
(2)计算工业甲醇的质量分数___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com