
【题目】苯佐卡因可用于粘膜溃疡、创面等的镇痛,是一种常用的局部麻醉剂,其合成路线如下图所示![]() 已知:
已知:![]() 当苯环上连有甲基时,再引入的其他基团主要进入甲基的邻位或对位;当苯环上连有羧基时,再引入的其他基团主要进入羧基的间位。
当苯环上连有甲基时,再引入的其他基团主要进入甲基的邻位或对位;当苯环上连有羧基时,再引入的其他基团主要进入羧基的间位。

②![]()
![]()
![]()
③![]()
![]()
![]() (有若碱性,易被氧化)
(有若碱性,易被氧化)
![]() 上述合成路线中属于取代反应的是 ____________。
上述合成路线中属于取代反应的是 ____________。![]() 填代号
填代号![]() 。化合物C中含有的含氧官能团的名称为 _____________。
。化合物C中含有的含氧官能团的名称为 _____________。
![]() 合成路线中反应
合成路线中反应![]() 的化学方程式为 _______________________________________。
的化学方程式为 _______________________________________。
![]() 下列关于上述合成路线的说法中正确的是 ____________。
下列关于上述合成路线的说法中正确的是 ____________。![]() 填字母
填字母![]()
![]() 反应
反应![]() 除主要生成物质A外,还可能生成
除主要生成物质A外,还可能生成![]() 、
、 等
等
![]() 步骤
步骤![]() 和
和![]() 可以互换
可以互换
![]() 反应
反应![]() 是还原反应
是还原反应
![]() 苯佐卡因有多种同分异构体,请写出其中任意一种满足下列条件的同分异构体的结构简式: _______________。
苯佐卡因有多种同分异构体,请写出其中任意一种满足下列条件的同分异构体的结构简式: _______________。
![]() 有两个对位取代基;
有两个对位取代基;![]() 直接连在苯环上;
直接连在苯环上;![]() 分子结构中含有酯基。
分子结构中含有酯基。
![]() 化合物
化合物 有较好的阻燃性,请写出以甲苯为主要原料制备该阻燃剂的合成路线流程图______。提示:
有较好的阻燃性,请写出以甲苯为主要原料制备该阻燃剂的合成路线流程图______。提示:![]() 合成过程中无机试剂任选;
合成过程中无机试剂任选;![]() 合成路线流程图示例如下:
合成路线流程图示例如下: ![]()
![]()
【答案】![]() 羧基
羧基 ![]()
![]()


【解析】
本题考查了有机物的合成,涉及反应类型、官能团名称、同分异构体书写、设计合成路线等,侧重考查了学生理解运用能力,平时学习时要注意基础知识的积累掌握。
在反应④中,C与乙醇发生酯化反应生成苯佐卡因,则C应为![]() ,根据题给B的分子式为
,根据题给B的分子式为![]() 可知B为
可知B为![]() ,由题给信息:①当苯环上连有甲基时,再引入的其他基团主要进入甲基的邻位或对位;当苯环上连有羧基时,再引入的其他基团主要进入羧基的间位,所以A为
,由题给信息:①当苯环上连有甲基时,再引入的其他基团主要进入甲基的邻位或对位;当苯环上连有羧基时,再引入的其他基团主要进入羧基的间位,所以A为![]() ,据此分析。
,据此分析。
![]() 根据以上分析,反应①为甲苯在浓硫酸作用下与浓硝酸发生硝化反应生成
根据以上分析,反应①为甲苯在浓硫酸作用下与浓硝酸发生硝化反应生成![]() ,为取代反应,反应②为
,为取代反应,反应②为![]() 在酸性高锰酸钾条件下被氧化生成
在酸性高锰酸钾条件下被氧化生成![]() ,为氧化反应,反应③为
,为氧化反应,反应③为![]() 在铁、HCl作用下发生还原反应生成
在铁、HCl作用下发生还原反应生成![]() ,为还原反应,反应④为
,为还原反应,反应④为![]() 与乙醇发生酯化反应生成苯佐卡因,则为取代反应;C为
与乙醇发生酯化反应生成苯佐卡因,则为取代反应;C为![]() 含有的含氧官能团的名称为羧基;
含有的含氧官能团的名称为羧基;
![]() 反应①为甲苯在浓硫酸作用下与浓硝酸发生硝化反应生成
反应①为甲苯在浓硫酸作用下与浓硝酸发生硝化反应生成![]() ,反应的化学方程式为
,反应的化学方程式为![]() ;
;
![]() 、根据题给信息,甲苯和与浓硝酸发生邻位取代或生成三硝基甲苯,故a正确;
、根据题给信息,甲苯和与浓硝酸发生邻位取代或生成三硝基甲苯,故a正确;
b、因为当苯环上连有甲基时,再引入的其他基团主要进入甲基的邻位或对位;当苯环上连有羧基时,再引入的其他基团主要进入羧基的间位,所以当步骤①和②互换时,先氧化成羧基,再取代则就不是对位而是间位,故b错误;
c、反应③为![]() 在铁、HCl作用下发生还原反应生成
在铁、HCl作用下发生还原反应生成![]() ,为还原反应,故c正确;
,为还原反应,故c正确;
答案选ac;
(4)①有两个对位取代基;②![]() 直接连在苯环上; ③分子结构中含有酯基,则符合条件的同分异构体为
直接连在苯环上; ③分子结构中含有酯基,则符合条件的同分异构体为 ;
;
![]() 采用逆推法,要合成
采用逆推法,要合成 ,则要得到
,则要得到 ,模仿流程中用甲苯到C的反应,不同的是在邻位取代,则流程图为:
,模仿流程中用甲苯到C的反应,不同的是在邻位取代,则流程图为: 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】甲硅烷广泛用于电子工业、汽车领域,三氯氢硅(SiHCl3)是制备甲硅烷的重要原料。回答下列问题:
(1)工业上以硅粉和氯化氢气体为原料生产SiHCl3时伴随发生的反应有:
Si(s)+4HCl(g)= SiCl4(g)+2H2(g) H=-241kJ/mol
SiHCl3(g)+HCl(g)=SiCl4(g)+H2(g) H=-31kJ/mol
以硅粉和氯化氢气体生产SiHCl3的热化学方程式是____________________________。
(2)工业上可用四氯化硅和氢化铝锂(LiAlH4)制甲硅烷,反应后得甲硅烷及两种盐。该反应的化学方程式为_________________。
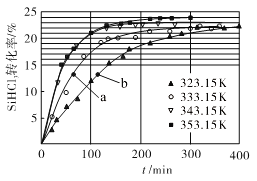
(3)三氯氢硅歧化也可制得甲硅烷。反应2SiHCl3(g) ![]() SiH2Cl2(g)+SiCl4(g)为歧化制甲硅烷过程的关键步骤,此反应采用一定量的PA100催化剂,在不同反应温度下测得SiHCl3的转化率随时间的变化关系如图所示。
SiH2Cl2(g)+SiCl4(g)为歧化制甲硅烷过程的关键步骤,此反应采用一定量的PA100催化剂,在不同反应温度下测得SiHCl3的转化率随时间的变化关系如图所示。
①353.15K时,平衡转化率为_________,反应的平衡常数K=________(保留3位小数)。该反应是________反应(填“放热”“吸热”)。
②323.15K时,要缩短反应达到平衡的时间,可采取的措施有_________、__________。
③比较a、b处反应速率的大小:va_____vb (填“>”“<”或“=”)。已知反应速率v正=![]() ,v逆=
,v逆=![]() ,k1、k2分别是正、逆反应的速率常数,与反应温度有关,x为物质的量分数,则在353.15K时
,k1、k2分别是正、逆反应的速率常数,与反应温度有关,x为物质的量分数,则在353.15K时![]() =________(保留3位小数)。
=________(保留3位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】干燥管 A 中为块状白色固体,烧杯中为稀盐酸,B 中为淡黄色粉末,C 中与 B含有相同阳离子的为白色半透明结晶状的固体碱,C 的火焰反应呈黄色。并将 A、B、C 按如图所示装置连接,当打开活塞(I)(II),关闭(III)时,D 中蜡烛火焰明亮;打开活塞(I)(III)时, D 中蜡烛火焰没有明显变化;关闭活塞(I)时,A 中反应自行停止。
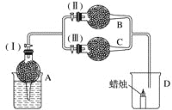
试根据上述实验事实,回答以下各问题:
(1)在装置B 中发生的化学反应是_______。
(2)在干燥管C 中的白色固体的俗名_____。写出 C 中发生化学反应的方程式:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为 A、B、C、D、E 五种含同一元素物质之间的相互转化关系。其中A、B、C、D 在常温下都是气体,且 B 为红棕色气体。

(1)①A、D、E三种物质中从相同元素化合价的角度分析既具有氧化性又具有还原性是(填化学式)____________;
②写出B的化学式:_______________, D的一种常见用途 _____________;
(2)按要求写出下列化学方程式或离子方程式
①写出 E 的稀溶液与 Cu 反应的离子方程式:_______________________;
②写出 D 的实验室制法的化学方程式___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物G是一种药物合成中间体,其合成路线如图:
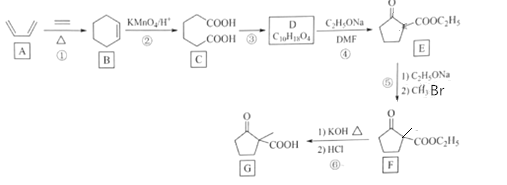
已知:R1CH2COOCH2CH3+R2COOCH2CH3![]() +CH3CH2OH
+CH3CH2OH
(1)化合物A的名称是__。
(2)反应②和⑤的反应类型分别是__、__。
(3)写出C到D的反应方程式__。
(4)E的分子式__。
(5)F中官能团的名称是__。
(6)X是G的同分异构体,X具有五元碳环结构,其核磁共振氢谱显示四组峰,且峰面积之比为6:2:1:1。写出两种符合要求的X的结构简式___。
(7)设计由乙酸乙酯和1,4-二溴丁烷制备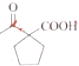 的合成路线___(无机试剂任选)。
的合成路线___(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W、M 均为短周期元素。25℃时,其最高价氧化物对应的水化物(浓度均为0.01mol/L)溶液的pH和原子半径的关系如图所示。下列说法不正确的是
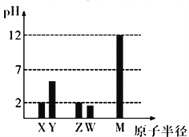
A. X、M 简单离子半径大小顺序:X>M
B. X、Y、Z、W、M 五种元素中只有一种是金属元素
C. Z 的最高价氧化物的化学式为ZO3
D. X、Z的最简单气态氢化物反应现象:有白烟生成XY ZW
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知四种物质A、B、C、D在一定条件下的相互转化关系如下图所示:
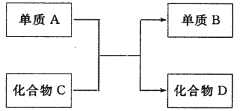
(1)若A是一种活泼金属单质,化合物D是烧碱。该反应的化学方程式为______;标准状况下,生成3.36L单质B,消耗单质A的物质的量为__。
(2)若A是国防金属,B是黑色固体单质。化合物C的化学式为_____;该反应中化合物C为___(填“氧化剂”或“还原剂”)。
(3)若A是一种黄绿色气体单质,单质B能使淀粉溶液变蓝。用四氯化碳将单质B从它的水溶液中提取出来,这种实验操作的名称叫做___。检验化合物D中阴离子的试剂为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2是一种重要的清洁能源。
(1)已知:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH2=-49.0kJmol-1
CH3OH(g)+H2O(g) ΔH2=-49.0kJmol-1
CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH3=-41.1kJmol-1
CO2(g)+H2(g) ΔH3=-41.1kJmol-1
H2还原 CO反应合成甲醇的热化学方程式为:CO(g)+2H2(g)![]() CH3OH(g) ΔH1,则ΔH1=___kJmol-1,该反应自发进行的条件为___
CH3OH(g) ΔH1,则ΔH1=___kJmol-1,该反应自发进行的条件为___
A.高温 B.低温 C.任何温度条件下
(2)恒温恒压下,在容积可变的密闭容器中加入 1molCO和2.2mol H2,发生反应CO(g)+2H2(g)![]() CH3OH(g),实验测得平衡时CO的转化率随温度、压强的变化如图所示。则P1__P2,判断的理由是_____。
CH3OH(g),实验测得平衡时CO的转化率随温度、压强的变化如图所示。则P1__P2,判断的理由是_____。

(3)若反应 CO(g)+2H2(g)![]() CH3OH(g)在温度不变且体积恒定为1的密闭容器中发生,反应过程中各物质的物质的量随时间变化如表所示:
CH3OH(g)在温度不变且体积恒定为1的密闭容器中发生,反应过程中各物质的物质的量随时间变化如表所示:
时间/min | 0 | 5 | 10 | 15 |
H2 | 4 | 2 | ||
CO | 2 | 1 | ||
CH3OH(g) | 0 | 0.7 |
①下列各项能作为判断该反应达到平衡标志的是____(填字母);
C.混合气体的相对分子质量保持不变 D.混合气体的密度保持不变
②若起始压强为P0 kPa,则在该温度下反应的平衡常数Kp=___(kPa)-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③反应速率若用单位时间内分压的变化表示,则10min内H2的反应速率v(H2)=___kPamin-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:①101kPa时,C(s)+1/2O2(g)=CO(g) △H1=-110.5kJ/mol②稀溶液中,H+(aq)+OH-(aq)=H2O(l) △H2=-57.3kJ/mol。下列结论中正确的是
A.若碳的燃烧热用△H3来表示,则△H3<△H1
B.若碳的燃烧热用△H3来表示,则△H3>△H1
C.稀硫酸与稀Ba(OH)2溶液反应生成2mol水,放出2×57.3kJ的热量
D.稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ的热量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com