
| A£® | ĶłČÜŅŗÖŠµĪČė0.2 mol•L-1µÄ°±Ė® | B£® | ĶłČÜŅŗÖŠ¼ÓČėNH4Cl¾§Ģå | ||
| C£® | ĶłČÜŅŗÖŠ¼ÓČėCH3COONa¹ĢĢå | D£® | ĶłČÜŅŗÖŠ¼ÓČėNaOH¹ĢĢå |
·ÖĪö °±Ė®ÖŠ“ęŌŚNH3•H2O?NH4++OH-£¬ČÜŅŗ³ŹČõ¼īŠŌ£¬Čē²ÉČ”Ä³Š©“ėŹ©£¬µĪÓŠ·ÓĢŖµÄ°±Ė®ČÜŅŗŃÕÉ«²»»į±äĒ³£¬ĖµĆ÷OH-Ąė×ÓÅØ¶Č²»¼õŠ”£¬ŅŌ“Ė½ā“šøĆĢā£®
½ā“š ½ā£ŗNH3•H2O?NH4++OH-£¬µĪČė·ÓĢŖ³ŹĻÖ·ŪŗģÉ«£¬ĖµĆ÷°±Ė®µÄpHŌŚ8”«10Ö®¼ä£®
A£®¼ÓČė0.2 mol•L-1µÄ°±Ė®£¬°±Ė®ÅضČŌö“ó£¬c£ØOH-£©Ōö“ó£¬ŗģÉ«±äÉī£¬¹ŹA“ķĪó£»
B£®¼ÓČėNH4Cl£¬c£ØNH4+£©Ōö“óŅÖÖĘĮĖ°±Ė®µÄµēĄė£¬c£ØOH-£©¼õŠ”ŃÕÉ«±äĒ³£¬¹ŹBÕżČ·£»
C£®¼ÓČėCH3COONa¹ĢĢ壬CH3COO-Ė®½ā²śÉśOH-£¬c£ØOH-£©Ōö“ó£¬ŗģÉ«±äÉī£¬¹ŹC“ķĪó£»
D£®¼ÓČėNaOH¹ĢĢ壬¶Ō°±Ė®µÄµēĄėĘ½ŗā²śÉśŅÖÖĘ×÷ÓĆ£¬µ«c£ØOH-£©±ä“ó£¬ŗģÉ«±äÉī£¬¹ŹD“ķĪó£®
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éĮĖČõµē½āÖŹŌŚČÜŅŗÖŠµÄµēĄė£¬ĪŖøßæ¼øßĘµæ¼µć£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦ŗĶ»ł±¾ĄķĀŪÖŖŹ¶µÄ×ŪŗĻĄķ½āŗĶŌĖÓƵÄ漲飬ĢāÄæ¶ą½Ē¶Čæ¼²éµēĄėĘ½ŗā£¬×¢Ņā°ŃĪÕĻą¹Ų»ł“”ÖŖŹ¶£¬ÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
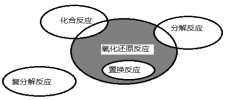 Ńõ»Æ»¹Ō·“Ó¦ÓėĖÄÖÖ»ł±¾ĄąŠĶ·“Ó¦µÄ¹ŲĻµČēĶ¼ĖłŹ¾£¬ŌņĻĀĮŠ»Æѧ·“Ó¦ŹōÓŚŅõÓ°²æ·ÖµÄŹĒ£Ø””””£©
Ńõ»Æ»¹Ō·“Ó¦ÓėĖÄÖÖ»ł±¾ĄąŠĶ·“Ó¦µÄ¹ŲĻµČēĶ¼ĖłŹ¾£¬ŌņĻĀĮŠ»Æѧ·“Ó¦ŹōÓŚŅõÓ°²æ·ÖµÄŹĒ£Ø””””£©| A£® | CuSO4+Mg=Cu+MgSO4 | B£® | 2NaHCO3$\frac{\underline{\;\;”÷\;\;}}{\;}$Na2CO3+H2O+CO2”ü | ||
| C£® | 2Na2O2+2CO2ØT2Na2CO3+O2 | D£® | 4Fe£ØOH£©2+O2+2H2OØT4Fe£ØOH£©3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£®ĢśµÄŅ±Į¶ | B£®µē³Ų·Åµē | C£®Ģ¼ĖįĒāÄĘ×÷·¢½Ķ·Ū | D£®ĢģČ»ĘųČ¼ÉÕ |
 |  |  |  |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2 mol•L-1 µÄNa2SO4ČÜŅŗÖŠŗ¬ÓŠ4 NAøöNa+ | |
| B£® | ½«ŗ¬ÓŠ0.1 mol FeCl3µÄ±„ŗĶČÜŅŗÖšµĪµĪČė×ćĮæ·ŠĖ®ÖŠ£¬µĆµ½Fe£ØOH£©3½ŗĢåŹżÄæĪŖ0.1 NA | |
| C£® | ŌŚ±ź×¼×“æöĻĀ£¬11.2 LÄŹĘųÖŠŗ¬ÓŠNAøöÄŹŌ×Ó1100”ę | |
| D£® | 7.8 g Na2O2ÖŠŅõĄė×ÓŹżÄæĪŖ0.1NA |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com