
分析 (1)Si的原子核外有14个电子分三层排布;
(2)同周期从左到右非金属性增强,同主族从上到下非金属性减弱;
(3)Si原子比C原子半径大,Si、O原子间距离较大.
解答 解:(1)Si的原子核外有14个电子分三层排布,则其电子排布式为1s22s22p63s23p2,故答案为:1s22s22p63s23p2;
(2)同周期从左到右非金属性增强,则非金属性:O>C,同主族从上到下非金属性减弱,则非金属性:C>Si,所以非金属性:O>C>Si,
故答案为:O>C>Si;
(3)CO2中C与O原子间形成σ键和π键,SiO2中Si与O原子间不形成上述π键,是因Si原子比C原子半径大,Si、O原子间距离较大,P-P轨道肩并肩重叠程度较小,不能形成上述稳定的π键,
故答案为:Si原子比C原子半径大,Si、O原子间距离较大,p-p轨道肩并肩重叠程度较小,不能形成上述稳定的π键.
点评 本题考查了核外电子排布、非金属性比较等,综合性较强,难度中等,注意把握非金属性的比较方法.


科目:高中化学 来源: 题型:选择题
| A. | 氢的同位素中重氢原子的符号:13H | |
| B. | Mg2+的结构示意图: | |
| C. | 氨气的电子式: | |
| D. | Ca(ClO)2的电离方程式:Ca(ClO)2=Ca2++2ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 研究有机物的组成、结构、性质、制备方法与应用的科学叫有机化学 | |
| B. | 有机物的反应与无机反应相比具有反应缓慢、产物复杂、常在水溶液中进行等特点 | |
| C. | 人们常利用有机物的性质,合成具有特定性质而自然界并不存在的有机物,满足人类的需要 | |
| D. | 高分子化合物与低分子有机物不仅在相对分子质量和结构上有差异,而且在物理性质、化学性质上也有较大差别 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CH-CH3+Cl2$\stackrel{高温}{→}$CH2=CHCH2Cl+HCl 加成反应 | |
| B. | 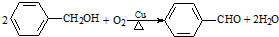 氧化反应 氧化反应 | |
| C. |  加成反应 加成反应 | |
| D. | 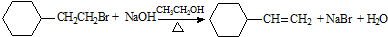 取代反应 取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 密闭容器中,9.6 g硫粉与11.2 g铁粉混合加热生成17.6 g硫化亚铁时,放出19.12 kJ热量.则Fe(s)+S(s)═FeS(s)△H=-95.6 kJ•mol-1 | |
| B. | 稀醋酸与0.1 mol•L-1 NaOH溶液反应:H+(aq)+OH-(aq)=H2O(l)△H=-57.3 kJ•mol-1 | |
| C. | 已知1 mol氢气完全燃烧生成液态水所放出的热量为285.5 kJ,则水分解的热化学方程式为2H2O(l)═2H2(g)+O2(g)△H=+285.5 kJ•mol-1 | |
| D. | 已知2C(s)+O2(g)=2CO(g)△H=-221 kJ•mol-1,则C的燃烧热△H=-110.5 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3-CH=CH-CHO | B. | CH3-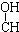 - -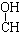 -CH3 -CH3 | ||
| C. | HOCH2-CH2-CH=CH-CHO | D. | HOCH2-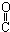 -CH2-CHO -CH2-CHO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com