
| A£® | CS2ĪŖÖ±ĻߊĪµÄ·Ē¼«ŠŌ·Ö×Ó | |
| B£® | ClO3-µÄæռ乹ŠĶĪŖĘ½ĆęČż½ĒŠĪ | |
| C£® | SF6ÖŠÓŠ6¶ŌĶźČ«ĻąĶ¬µÄ³É¼üµē×Ó¶Ō | |
| D£® | SiF4ŗĶSO32-µÄÖŠŠÄŌ×Ó¾łĪŖsp3ŌÓ»Æ |
·ÖĪö A£®CS2ÓėCO2·Ö×Ó¹¹ŠĶĻąĶ¬£¬øł¾Ż¶žŃõ»ÆĢ¼µÄ·Ö×Ó½į¹¹·ÖĪö£»
B£®ĻČĒó³öÖŠŠÄŌ×ӵļŪ²ćµē×Ó¶ŌŹż£¬ŌŁÅŠ¶Ļ·Ö×Ó¹¹ŠĶ£»
C£®SF6ÖŠS-Fŗ¬ÓŠŅ»øö³É¼üµē×Ó¶Ō£»
D£®ĻČĒó³öÖŠŠÄŌ×ӵļŪ²ćµē×Ó¶ŌŹż£¬ŌŁÅŠ¶ĻŌÓ»ÆĄąŠĶ£®
½ā“š ½ā£ŗA£®CS2ÓėCO2·Ö×Ó¹¹ŠĶĻąĶ¬£¬¶žŃõ»ÆĢ¼µÄ·Ö×Ó½į¹¹ĪŖO=C=O£¬ŌņCS2µÄ½į¹¹ĪŖS=C=S£¬ŹōÓŚÖ±ĻߊĪµÄ·Ē¼«ŠŌ·Ö×Ó£¬¹ŹAÕżČ·£»
B£®ClO3-ÖŠClµÄ¼Ū²ćµē×Ó¶ŌŹż=3+$\frac{1}{2}$£Ø7+1-2”Į3£©=4£¬ŗ¬ÓŠŅ»øö¹Āµē×Ó¶Ō£¬ŌņĄė×ÓµÄæռ乹ŠĶĪŖČż½Ē׶ŠĪ£¬¹ŹB“ķĪó£»
C£®SF6ÖŠS-Fŗ¬ÓŠŅ»øö³É¼üµē×Ó¶Ō£¬ĖłŅŌSF6ÖŠŗ¬ÓŠ6øöS-F¼ü£¬Ōņ·Ö×ÓÖŠÓŠ6¶ŌĶźČ«ĻąĶ¬µÄ³É¼üµē×Ó¶Ō£¬¹ŹCÕżČ·£»
D£®SiF4ÖŠSiµÄ¼Ū²ćµē×Ó¶ŌŹż=4+$\frac{1}{2}$£Ø4-1”Į4£©=4£¬SO32-ÖŠSiµÄ¼Ū²ćµē×Ó¶ŌŹż=3+$\frac{1}{2}$£Ø6+2-2”Į3£©=4£¬ĖłŅŌÖŠŠÄŌ×Ó¾łĪŖsp3Ōӻƣ¬¹ŹDÕżČ·£®
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²é·Ö×ӵĹ¹ŠĶ”¢Ō×ÓŌӻƷ½Ź½ÅŠ¶ĻµČÖŖŹ¶µć£¬²ąÖŲæ¼²é»ł±¾ĄķĀŪ£¬ÄѵćŹĒÅŠ¶ĻŌ×ÓŌӻƷ½Ź½£¬ÖŖµĄ¹Āµē×Ó¶ŌøöŹżµÄ¼ĘĖć·½·Ø£¬ĪŖŅדķµć£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
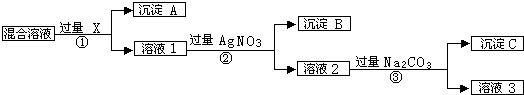
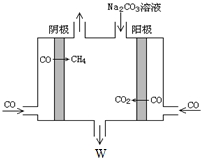
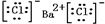 £¬³ĮµķAµÄ¾§ĢåĄąŠĶĄė×Ó¾§Ģ壬CO32-µÄæռ乹ŠĶŹĒĘ½ĆęČż½ĒŠĪ£®
£¬³ĮµķAµÄ¾§ĢåĄąŠĶĄė×Ó¾§Ģ壬CO32-µÄæռ乹ŠĶŹĒĘ½ĆęČż½ĒŠĪ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś | B£® | ¢Ś¢Ū | C£® | ¢Ś¢Ü | D£® | ¢Ū¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ź±¼ä£Øs£© | 0 | 20 | 40 | 60 | 80 |
| n£ØNO2£©/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n£ØN2O4£©/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
| A£® | ·“Ó¦æŖŹ¼20 sÄŚŅŌ¶žŃõ»ÆµŖ±ķŹ¾µÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ0.00125 mol/L•s | |
| B£® | 80 sŹ±ĻņČŻĘ÷ÖŠ¼ÓČė0.32 molŗ¤Ęų£¬Ķ¬Ź±½«ČŻĘ÷Ą©“óĪŖ 4 L£¬ŌņĘ½ŗā½«²»ŅĘ¶Æ | |
| C£® | µ±·“Ó¦“ļµ½Ę½ŗāŗó£¬ČōĖõŠ”ČŻĘ÷µÄĢå»ż£¬Ę½ŗāĻņÉś³ÉN2O4·½ĻņŅĘ¶Æ£¬ĘųĢåµÄŃÕÉ«±äÉī | |
| D£® | ČōĘäĖüĢõ¼ž²»±ä£¬ĘšŹ¼Ķ¶ĮĻøÄĪŖ0.40 mol N2O4£¬ĻąĶ¬Ģõ¼žĻĀ“ļĘ½ŗā£¬Ōņø÷×é·Öŗ¬ĮæÓėŌĘ½ŗāĢåĻµ¶ŌÓ¦ĻąµČ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£® £¬A2C2µÄ½į¹¹Ź½£ŗH-O-O-H£®
£¬A2C2µÄ½į¹¹Ź½£ŗH-O-O-H£® £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŗĖÄŚÓŠ2øöÖŹ×Ó | B£® | Óė4He»„ĪŖĶ¬Ī»ĖŲ | ||
| C£® | ŗĖÄŚÓŠ1øöÖŠ×Ó | D£® | ŹĒ4HeµÄĶ¬ĖŲŅģŠĪĢå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | AŌ×Ó×īĶā²ćµē×ÓŹż±ČBŌ×ÓµÄ×īĶā²ćµē×ÓŹżÉŁ | |
| B£® | ½«A”¢B×é³ÉŌµē³ŲŹ±£¬AĪŖÕż¼« | |
| C£® | 1molA“ÓĖįÖŠÖĆ»»Éś³ÉµÄH2±Č1mol B“ÓĖįÖŠÖĆ»»Éś³ÉµÄH2¶ą | |
| D£® | ½«AŗĶBÓƵ¼ĻßĻąĮ¬½Ó£¬Ņ»Ķ¬·ÅČėCuSO4ČÜŅŗÖŠ£¬BµÄ±ķĆęÓŠŗģÉ«µÄĶĪö³ö |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ·Ö×ÓŹ½/½į¹¹Ź½ | NO/N”ŌO | CO/C”ŌO | CO2/O=C=O | N2/N”ŌN |
| »Æѧ¼ü | N”ŌO | C”ŌO | C=O | N”ŌN |
| ¼üÄÜ£ØKJ/mol£© | 632 | 1072 | 750 | 946 |
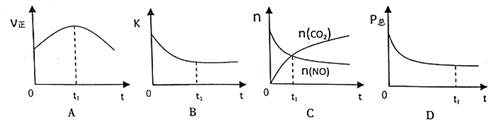
| Ź±¼ä/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n£ØNO£©/”Į10-2mol | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| n£ØCO£©/”Į10-1mol | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

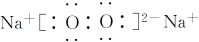
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com