
 TiCl4+2CO
TiCl4+2CO  2MgCl2+Ti 下列叙述正确的是
2MgCl2+Ti 下列叙述正确的是  阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:

(1)Ti的原子序数为22,Ti位于元素周期表中第_________周期,第_________族。
(2)步骤①加Fe的目的是___________________________;
步骤②冷却的目的________________________________。
(3)上述制备TiO2的过程中,可以利用的副产物是_________,考虑成本和废物综合利用因素,废液中应加入_________处理。
(4)由金红石(TiO2)制取单质Ti,涉及到的步骤为:
TiO2![]() TiCl4
TiCl4![]() Ti
Ti
已知:①C(s)+O2(g)====CO2(g);ΔH=-393.5 kJ·mol-1
②2CO(g)+O2(g)====2CO2(g);ΔH=-566 kJ·mol-1
③TiO2(s)+2Cl2(g)====TiCl4(s)+O2(g);ΔH=+141 kJ·mol-1
则TiO2(s)+2Cl2(g)+2C(s)====TiCl4(s)+2CO(g)的ΔH=__________。
反应TiCl4+2Mg====2MgCl2+Ti在Ar气氛中进行的理由是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
钛(Ti)被称为继铁、铝之后的第三金属。如下图所示,将钛厂、氯碱厂和甲醇厂组成产业链可以大大提高资源利用率,减少环境污染。请填写下列空白:
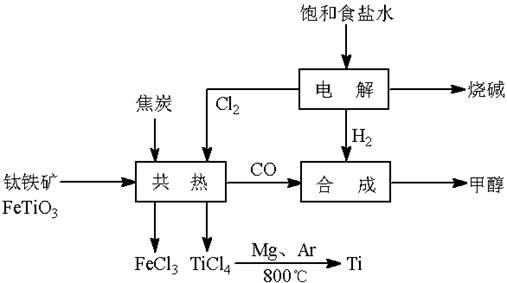
(1)电解饱和食盐水时,阳极的电极反应为 。
(2)写出钛铁矿与焦炭、Cl2共热制得四氯化钛的化学方程式________________________。
(3)已知:①Mg(s) + Cl2(g)=MgCl2(s);△H = – 641 kJ/mol
![]() ②Ti(s) + 2Cl2(g)=TiCl4(s);△H = –770 kJ/mol
②Ti(s) + 2Cl2(g)=TiCl4(s);△H = –770 kJ/mol
则2Mg(s) + TiCl4(s)=2MgCl2(s) + Ti(s);△H= 。
![]() 反应2Mg(s) + TiCl4(s)
反应2Mg(s) + TiCl4(s)![]() 2MgCl2(s) + Ti(s),在Ar气氛中进行的理由是 。
2MgCl2(s) + Ti(s),在Ar气氛中进行的理由是 。
(4)在上述产业链中,合成96 t 甲醇理论上消耗H2 t (不考虑生产过程中物质的任何损失)。
(5)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。已知该燃料电池的总反应式为:2CH3OH + 3O2 + 4OH-=2CO32- + 6H2O。该燃料电池发生反应时正极区溶液的pH (填“增大”、“减小”或“不变”),该电池中负极上的电极反应是________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年天津市十二校高三第二次模拟联考化学试卷(解析版) 题型:填空题
钛(Ti)被称为继铁、铝之后的第三金属,也有人说21世纪是钛的世纪。钛在地壳中的含量并不少,但钛的冶炼技术还未获得突破,目前钛只用于尖端领域。
如下图所示,将钛厂、氯碱厂和甲醇厂组成产业链可大大提高资源利用率,减少环境污染。

请填写下列空白:
(1)用惰性电极电解2 L食盐水时,总反应的离子方程式_______________________________,当阴极上产生224 mL气体(标准状况)时,所得溶液的pH= (假设电解前后溶液体积不变,食盐水足量)。
(2)写出高温下钛铁矿经氯化得到四氯化钛的化学方程式 。(提示:FeTiO3中Ti为+4价)
(3)反应2Mg+TiCl4 2MgCl4+Ti在Ar气氛中进行的理由是____________________。
2MgCl4+Ti在Ar气氛中进行的理由是____________________。
(4)二甲醚是一种重要的清洁燃料,可以通过甲醇分子间脱水制得:
2CH3OH(g) CH3OCH3(g)+H2O(g) ΔH=" -23.5" kJ/mol
CH3OCH3(g)+H2O(g) ΔH=" -23.5" kJ/mol
T1 ℃时,在恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如下图所示。

①T1 ℃时,该反应的平衡常数为 ;
②相同条件下,若改变起始浓度,某时刻各组分浓度依次为c(CH3OH)="0.4" mol/L、c(H2O)="0.6" mol/L、(CH3OCH3)="1.2" mol/L,此时正、逆反应速率的大小:v正 v逆(填“>”、“<”或“=”)。
(5)在上述产业链中,合成192吨甲醇理论上需额外补充H2__________吨 (不考虑生产过程中物质的任何损失)。
查看答案和解析>>
科目:高中化学 来源:西南师大附中2010届高三第五次月考(理综)试题化学部分 题型:填空题
(13分) 钛(Ti)被称为继铁、铝之后的第三金属。如下图所示,将钛厂、氯碱厂和甲醇厂组成产业链可以大大提高资源利用率,减少环境污染。请填写下列空白:
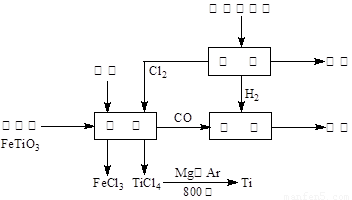
(1)电解饱和食盐水时,阳极的电极反应为 。
(2)写出钛铁矿与焦炭、Cl2共热制得四氯化钛的化学方程式________________________。
(3)已知:①Mg(s) + Cl2(g)=MgCl2(s);△H = – 641 kJ/mol
②Ti(s) + 2Cl2(g)=TiCl4(s);△H = –770 kJ/mol
则2Mg(s) + TiCl4(s)=2MgCl2(s) + Ti(s);△H= 。
反应2Mg(s) + TiCl4(s) 2MgCl2(s) + Ti(s),在Ar气氛中进行的理由是
。
2MgCl2(s) + Ti(s),在Ar气氛中进行的理由是
。
(4)在上述产业链中,合成96 t 甲醇理论上消耗H2 t (不考虑生产过程中物质的任何损失)。
(5)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。已知该燃料电池的总反应式为:2CH3OH + 3O2 + 4OH-=2CO32- + 6H2O。该燃料电池发生反应时正极区溶液的pH (填“增大”、“减小”或“不变”),该电池中负极上的电极反应是________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年广东省中山市高三化学模拟试卷(七) 题型:填空题
钛(Ti )被称为继铁、铝之后的第三金属。如下图所示,将钛厂、氯碱厂和甲醇厂组成产业链可以大大提高资源利用率,减少环境污染。请填写下列空白:


(l)电解饱和食盐水时,总反应的离子方程式是 。
 (2)写出钛铁矿经氯化法得到四氯化钛的化学方程
。
(2)写出钛铁矿经氯化法得到四氯化钛的化学方程
。
(3)已知:①Mg(s) + Cl2(g)=MgCl2(s) △H =-641kJ·mol-1
 ②Ti(s)
+ 2Cl2(g)=TiCl4(s) △H
= -770kJ·mol-1
②Ti(s)
+ 2Cl2(g)=TiCl4(s) △H
= -770kJ·mol-1
则2Mg(s) + TiCl4(s)=2MgCl2(s) + Ti(s) △H= 。
 反应2Mg(s)
+ TiCl4(s)
反应2Mg(s)
+ TiCl4(s) 2MgCl2(s)
+ Ti,在Ar气氛中进行的理由是:
______________________________________
。
2MgCl2(s)
+ Ti,在Ar气氛中进行的理由是:
______________________________________
。
 (4)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。该电池中负极上的电极反应式是
。
(4)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。该电池中负极上的电极反应式是
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com