
【题目】将氯碱工业与燃料电池联合能够有效降低能源消耗,如图是该工艺的图示(电源及电极未标出),请回答下列问题:
(1)电解饱和食盐水(氯碱工业)的化学方程式为 .
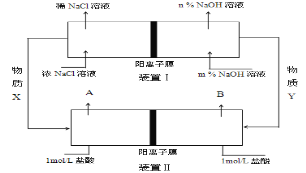
(2)物质X为 ,装置Ⅰ和Ⅱ中属于燃料电池的是 .
(3)装置Ⅰ中,NaOH溶液浓度m% n% (填“>”或“<”).
(4)利用装置Ⅱ可获得10mol/L盐酸,该产品出口为 (填“A”或“B”).
【答案】(1)2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑;(2)Cl2;Ⅱ;(3)<;(4)A。
2NaOH+H2↑+Cl2↑;(2)Cl2;Ⅱ;(3)<;(4)A。
【解析】
试题分析:(1)电解饱和食盐水得到氢氧化钠、氯气和氢气,因此化学反应方程式为:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑;(2)根据工艺图,装置I为电解池,装置Ⅱ为燃料电池,装置I的左端为阳极,电极反应式为2Cl--2e-=Cl2↑,右端为阴极,电极反应式2H++e-=H2↑,因此物质X为Cl2,物质Y为H2;(3)根据(2)中阳极反应式,右端产生OH-,因此m%<n%;(4)装置II左端是正极,反应式为Cl2+2e-=2Cl-,右端是负极,反应式为:H2-2e-=2H+,装置II中是阳离子交换膜,阳离子可以通过,即H+通过,根据原电池的工作原理,H+向正极移动,即10mol·L-1的盐酸从A口出。
2NaOH+H2↑+Cl2↑;(2)根据工艺图,装置I为电解池,装置Ⅱ为燃料电池,装置I的左端为阳极,电极反应式为2Cl--2e-=Cl2↑,右端为阴极,电极反应式2H++e-=H2↑,因此物质X为Cl2,物质Y为H2;(3)根据(2)中阳极反应式,右端产生OH-,因此m%<n%;(4)装置II左端是正极,反应式为Cl2+2e-=2Cl-,右端是负极,反应式为:H2-2e-=2H+,装置II中是阳离子交换膜,阳离子可以通过,即H+通过,根据原电池的工作原理,H+向正极移动,即10mol·L-1的盐酸从A口出。


科目:高中化学 来源: 题型:
【题目】常温时,向一定量的硫酸铜溶液中滴加pH="11" 的氨水,当Cu2+完全沉淀时,消耗氨水的体积为V,下列说法正确的是(已知Ksp[Cu(OH)2] = 2.2×10-20)( )
A. 若将氨水加水稀释,则稀释过程中,c(NH4+)/c(NH3H2O)始终保持增大
B. 滴加过程中,当溶液中c(Cu2+) = 2.2×10-2 mol/L 时,溶液的pH = 9
C. 滴加过程中,当溶液的pH =" 7" 时,溶液中2c(NH4+)= c(SO42-)
D. 若滴加pH =" 11" 的NaOH 溶液,Cu2+完全沉淀时消耗溶液的体积小于V
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z都是气体,反应前X、Y的物质的量之比是1:2,在一定条件下可逆反应X+2Y2Z达到平衡时,测得反应物总的物质的量等于生成物总的物质的量,则平衡时X的转化率是( )
A. 80% B. 20% C. 40% D. 60%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的熔点均按由高到低的排列,其原因是由于键能由大到小排列的是 ( )
A.铝、钠、干冰
B.金刚石、碳化硅、晶体硅
C.碘化氢、溴化氢、氯化氢
D.二氧化硅、二氧化碳、一氧化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于某些离子的检验及结论一定正确的是
A. 加入硝酸酸化的硝酸银溶液有白色沉淀生成,则溶液中一定含有Cl-
B. 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO![]()
C. 加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,则溶液中有CO![]()
D. 如透过蓝色的钴玻璃能够观察到紫色火焰,则一定有钾元素,一定不含有钠元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将碘水中的碘萃取出来的实验中,下列说法错误的是( )
A.分液漏斗使用前要检查它是否漏水
B.萃取剂要求不溶于水,且比水更容易使碘溶解
C. 注入碘水和萃取剂,倒转分液漏斗反复用力振荡后,不必静置,应立即分液
D. 分液时,下层液体应从下口流出,上层液体应从上口倒出
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com