
下列表述正确的是
A.H2O2的电子式:  B.Cl的原子结构示意图:
B.Cl的原子结构示意图: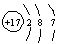
C.质子数是82,中子数是122的铅原子: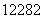 Pb D.CO2的比例模型:
Pb D.CO2的比例模型: 

 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案科目:高中化学 来源: 题型:
哈伯因发明了由氮气合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充入1molN2和3molH2,在一定条件下发生反应N2+3H2 2NH3 。下列有关说法正确的是:
2NH3 。下列有关说法正确的是:
A.达到化学平衡时,N2将完全转化为NH3
B.达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化
C.达到化学平衡时,反应则停止进行
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,碳钢腐蚀与溶液pH的关系如下:
| pH | 2 | 4 | 6 | 6.5 | 8 | 13.5 | 14 |
| 腐蚀快慢 | 较快 | 慢 | 较快 | ||||
| 主要产物 | Fe2+ | Fe3O4 | Fe2O3 | FeO2— |
下列说法不正确的是
A.在pH<4溶液中,碳钢主要发生析氢腐蚀
B.在pH>6溶液中,碳钢主要发生吸氧腐蚀
C.在pH>14溶液中,碳钢腐蚀的正极反应为O2+4H++4e—=2H2O
D.在煮沸除氧气后的碱性溶液中,碳钢腐蚀速率会减缓
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,在含CH3COOH和CH3COONa均为0.1mol/L的溶液中,测得pH<7,则下列说法中正确的是
A.c(CH3COO-)<c(Na+) B. c(CH3COOH) + c(CH3COO-)=0.2mol/L
C.c(CH3COOH) > c(CH3COO-) D.c(CH3COO-)>c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
某校化学兴趣小组的同学对一含有少量Na2SO4的NaOH样品中NaOH的含量进行测定,请回答下列问题
(1)甲同学运用沉淀法测定样品中NaOH的含量。甲同学选用的药品除样品外,还应有
▲ ,实验中应测定的数据有 ▲ 。
(2)乙同学运用滴定法测定样品中NaOH的含量。
①用分析天平准确称取该样品5.360g,全部溶于水配制成1000.0mL的溶液。用碱式滴定管取其中20.00mL放在锥形瓶中,滴加几滴甲基橙做指示剂。用标准的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视 ▲ 。滴定终点的现象是 ▲ 。
②下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是 ▲ (填写序号)
 A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,滴定结束时俯视读数
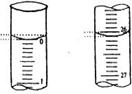
③若滴定开始和结束时,酸式滴定管中的液面如右图所示:
开始 结束
则起始读数为 ▲ mL,终点读数 ▲ mL;
(3)某学生根据三次实验分别记录有关数据如下:
| 滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.1000mol/L盐酸的体积(mL) | ||
| 滴定前刻度 | 滴定后刻度 | |||
| 第一次 | 20.00 | 0.00 | 26.01 | |
| 第二次 | 20.00 | 1.56 | 30.30 | |
| 第三次 | 20.00 | 0.22 | 26.21 |
请选用其中合理的数据列式计算出该样品中NaOH的质量百分含量。(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
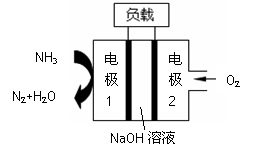
瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧
燃料电池示意图如右,有关说法正确的是
A.电池工作时,Na+ 向负极移动
B.通氨气的电极1作电池的正极
C.电子由电极2经外电路流向电极1
D.燃料电池的总反应为:4NH3+3O2=2N2+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
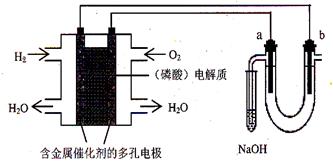
用酸性氢氧燃料电池电解饱和食盐水的装置如图所示 (a、b为石墨电极)。下列说法中,正确的是
A.电池工作时,正极反应式为:O2 +2 H2O + 4e-= 4OH-B.电解时,a 电极周围首先放电的是Cl—
C.电解时,电子流动路径是:负极→外电路→阴极→溶液→阳极→正极
D.忽略能量损耗,当电池中消耗0.2g H2 时,b极周围会产生2.24L H2
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列叙述正确的是 ( )。
A.标准状况下,2.24 L Cl2通入足量NaOH溶液中,反应转移电子的数目为
0.2NA
B.常温下,0.1 mol·L-1 NH4NO3溶液中NO3-数目为0.1NA
C.常温常压下,4.0 g CH4中含有共价键的数目为NA
D.标准状况下,22.4 L CHCl3含有分子的数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值。下列叙述正确的是(相对原子质量:D-2 O-16 Cu-64)
A.18 g的D216O中含有的中子数为9 NA
B.物质的量浓度均为1.0mol/L的硫酸与高氯酸(HClO4)溶液中含有的氧原子数均为4NA
C.33.6 L NO2溶于足量的水得到的溶液中含有的NO 数为NA
数为NA
D.32 g铜发生氧化还原反应,一定失去NA个电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com