
药物贝诺酯可由乙酰水杨酸和对-乙酰氨基酚在一定条件下反应制得:

有关上述反应物和产物的叙述不正确的是( )
A.上述三种有机物中共有四种含氧官能团
B.贝诺酯分子中有9种不同化学环境的氢原子
C.贝诺酯与足量NaOH(aq)共热,最多消耗NaOH 4mol
D.可用FeCl3(aq) 区别乙酰水杨酸和对-乙酰氨基酚
科目:高中化学 来源: 题型:
某兴趣小组为测定某工业纯碱(假设仅含NaHCO3杂质)中Na2CO3的质量分数,设计了下列四种实验方案:
方案一:纯碱样品 测定剩余固体质量
测定剩余固体质量
(1)称取mg样品放入坩埚中充分加热。坩埚中发生反应的化学方程式为:
(2)将坩埚置于干燥器中冷却后称量。实验时需要重复“加热、冷却、称量”操作多次,其目的是: 。
方案二:称取mg样品配成250mL溶液,从中取25mL溶液先用酚酞作指示剂用0.1mol/LHCl溶液滴定至终点,消耗0.1mol/LHCl溶液V1mL,继续用甲基橙作指示剂滴定至终点,消耗0.1mol/LHCl溶液V2mL。则该样品中碳酸钠的质量分数为: 。
方案三:纯碱样品溶液 测定沉淀质量
测定沉淀质量
(1)称取m1g样品,置于小烧杯中,加水溶解后滴加足量氯化钙溶液。将反应混和物过滤后的下一步操作是: ,沉淀经干燥后称量为m2g。
(2)如果用氢氧化钙溶液代替氯化钙溶液作沉淀剂,在其他操作正确的情况下,_______测定样品中的Na2CO3的质量分数。(填“能”或“不能”)
方案四:纯碱样品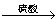 测定生成二氧化碳的质量
测定生成二氧化碳的质量
(1)本实验采用如图装置,C中盛放的物质是 。
(2)反应前后都要通入N2,反应后通入N2的目的是:
查看答案和解析>>
科目:高中化学 来源: 题型:
一定浓度l00mL的HNO3溶液中加入2.8gFe,全部溶解,得到标准状况下的NO气体1.12L, 测得反应后溶液中的c(H+)=0.1mol/L。若反应前后溶液体积变化忽略不计,则下列有关判断错误的是
A.反应后溶液中无硝酸亚铁 B.反应前HNO3溶液的浓度为2.0mol
C.反应后溶液中c(NO3-)=1.6mol D.反应后的溶液最多还能溶解1.6lgFe
D.反应后的溶液最多还能溶解1.6lgFe
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸亚锡(SnSO4)是一种重要的硫酸盐,主要用于电镀工业的镀锡、铝合金表面的氧化着色、印染工业的媒染剂、双氧水去除剂等。某研究小组设计SnSO4制备路线如下:
查阅资料:
Ⅰ.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
Ⅱ.SnCl2易水解生成难溶物Sn(OH)Cl(碱式氯化亚锡)。
请回答下列问题:
(1)锡原子的核电荷数为50,锡元素在周期表中的位置是 第五周期第ⅣA族
(2)SnCl2粉末需加浓盐酸进行溶解,请结合必要的方程式,用平衡移动原理来解释原因
。
(3)加入Sn粉的作用有两个:①调节溶液pH ② 。
(4)反应Ⅰ得到沉淀是SnO,得到该沉淀的离子反应方程式是
。
(5)操作Ⅰ包含的一系列具体实验步骤的名称分别为: 。
(6)酸性条件下,SnSO4还可以用作双氧水去除剂,发生反应的离子方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.糖类、油脂、蛋白质在一定条件都能发生水解反应
B.苯只能发生取代反应,不能发生加成反应
C.棉、麻、羊毛及合成纤维完全燃烧都只生成CO2和H2O
D.溴乙烷与NaOH的乙醇溶液共热生成乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
铝生产产业链由铝土矿开采、氧化铝制取、铝的冶炼和铝材加工等环节构成。请回答下列问题:
⑴工业上采用电解氧化铝-冰晶石(Na3AlF6)熔融体的方法冶炼得到金属铝:
2Al2O3  4Al+3O2↑加入冰晶石的作用:_______________________________。
4Al+3O2↑加入冰晶石的作用:_______________________________。
⑵上述工艺所得铝材中往往含有少量Fe和Si等杂质,可用电解方法进一步提纯,该电解池中阳极的电极反应式为 ,下列可作阴极材料的是________________。
A.铝材 B.石墨 C.铅板 D.纯铝

⑶阳极氧化能使金属表面生成致密的氧化膜。以稀硫酸为电解液,铝阳极发生的电极反应式为__________________________________。
⑷在铝阳极氧化过程中,需要不断地调整电压,理由是____________ 。
⑸下列说法正确的是 。
A. 阳极氧化是应用原电池原理进行金属材料表面处理的技术
B. 铝的阳极氧化可增强铝表面的绝缘性能
C. 铝的阳极氧化可提高金属铝及其合金的耐腐蚀性,但耐磨性下降
D. 铝的阳极氧化膜富有多孔性,具有很强的吸附性能,能吸附染料而呈各种颜色
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述I和II均正确且有因果关系的是
| 选项 | 叙述I | 叙述II |
| A | NH4Cl为强酸弱碱盐 | 用加热法除去NaCl中的NH4Cl |
| B | 溶解度:CaCO3<Ca(HCO3)2 | 溶解度:Na2CO3<NaHCO3 |
| C | SiO2与HF反应 | 氢氟酸不能保存在玻璃瓶中 |
| D | Fe3+具有氧化性 | 用KSCN溶液可以鉴别Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
对于3.4克氨气的有关说法,正确的是 ( )
A、常温常压下体积为4.48L
B、含有0.1mol N 和0.3mol H
C、常温下,所含原子有0.8mol
D、溶解到1L水中,所得溶液物质的量浓度为0.2mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振氢谱表明分子中只有一种类型的氢。
(1) A的结构简式为_________________________________________________.
(2) A中的碳原子是否都处于同一平面__________(填“是”或“不是”).
(3) 在下列框图中,D1、D2互为同分异构体,E1、E2互为同分异构体。
Cl2 NaOH、C2H5OH、△

 A B
A B
① ②
|

 D1
D1
③1,2-加成反应 ⑤
|
Br2/CCl2 NaOH、H2O、△

 D2 E2
D2 E2
④ ⑥
反应②的化学方程式为__________________________________________________;
C的化学名称是_________________________________________________________;
E2的结构简式是__________________________________________________________;
④ ⑥的反应类型依次是____________________、_________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com