
【题目】硝酸与金属反应时,浓度越稀还原产物价态越低。现用一定量的铝粉与镁粉组成的混合物与100mL硝酸钾溶液与硫酸组成的混合溶液充分反应,反应过程中无任何气体放出,向反应后的溶液中逐滴加入4.00mol/L的NaOH溶液,加入的溶液体积与产生的沉淀质量的关系如图所示:
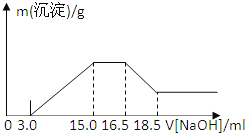
下列结论正确的是( )
A.铝与混合溶液反应的离子方程式为8Al+30H++3NO3=8Al3++3NH4++9H2O
B.参加反应硝酸根离子物质的量为0.06 mol
C.参加反应的铝与镁的质量之比为4:3
D.混合液中硫酸的物质的量的浓度为0.72 mol/L
【答案】A
【解析】
A. 硝酸根浓度很低时被氧化生成的产物是铵根离子,因此无气体放出,镁、铝反应生成金属阳离子,则离子反应分别为4Mg+10H++NO3=4Mg2++NH4++3H2O、8Al+30H++3NO3=8Al3++3NH4++9H2O,A项正确;
B. 由图示可以看出加入氢氧化钠溶液从15.0mL到16.5mL区间内发生的反应是氢氧根离子与铵根离子的反应,由氮原子守恒可知,铵根离子的物质的量即为原溶液中反应的硝酸根离子的物质的量,则原溶液中NO3物质的量是(16.5-15)×103L×4mol/L=0.006mol,B项错误;
C. 从图示提示中看出从氢氧化溶液体积16.5mL到18.5mL区间内发生的反应是氢氧化铝与氢氧化钠的反应,氢氧化铝与氢氧化钠等物质的量反应,由Al~Al3+~Al(OH)3~NaOH,则Al的物质的量为0.008mol,再由Mg2++2OH=Mg(OH)2↓、Al3++3OH=Al(OH)3↓,沉淀镁离子和铝离子共消耗氢氧化钠溶液体积(15.0-3.0)mL,由此可知:沉淀镁离子时消耗的氢氧根离子物质的量为(15.0-3.0)×103L×4.00mol/L-8×103mol×3=24×103mol,镁离子物质的量为1.2×102mol,参加反应的镁与铝的质量之比:8×103mol×27g/mol:1.2×102mol×24g/mol=3:4,C项错误;
D. 由4Mg+10H++NO3=4Mg2++NH4++3H2O、8Al+30H++3NO3=8Al3++3NH4++9H2O可知,消耗氢离子为0.008mol×![]() +1.2×102mol×
+1.2×102mol×![]() =0.06mol,图中开始3.0mLNaOH溶液消耗氢离子的物质的量为3×103L×4mol/L=0.012mol,原溶液中硫酸的物质的量为
=0.06mol,图中开始3.0mLNaOH溶液消耗氢离子的物质的量为3×103L×4mol/L=0.012mol,原溶液中硫酸的物质的量为![]() =0.036mol,混合液中硫酸的物质的量的浓度为
=0.036mol,混合液中硫酸的物质的量的浓度为![]() =0.36mol/L,D项错误;
=0.36mol/L,D项错误;
答案选A。


科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种物质的焰色反应都呈黄色,A、B分别与水反应都有气体放出,同时都生成C溶液,A与水反应放出的气体具有还原性,B与水反应放出的气体具有氧化性,C与适量的F气体反应生成D,D溶液与F气体反应生成E,E加热能够生成D和F气体。根据以上叙述回答下列问题:
(1)写出下列物质的化学式:B____,D____,E______。
(2)按要求完成方程式:
①加热E生成D和F的化学方程式____;
②C溶液和CO2反应生成D的离子方程式____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用滴定管量取一定体积的浓氯水置于锥形瓶中,用NaOH溶液以恒定速度来滴定该浓氯水,根据测定结果绘制出ClO-、ClO3-等离子的物质的量浓度c与时间t的关系曲线如下。下列说法正确的是( )
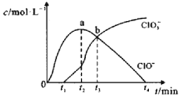
A.NaOH溶液和浓氯水可以使用同种滴定管盛装
B.a点溶液中存在如下关系:c(Na+)+c(H+)=c(ClO-)+c(ClO3-)+c(OH-)
C.b点溶液中各离子浓度:c(Na+)>c(Cl-)>c(ClO3-)=c(ClO-)
D.t2~t4,ClO-的物质的量下降的原因可能是ClO-自身歧化:2ClO-=Cl-+ClO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 石灰乳与过量碳酸氢钙溶液反应:HCO3—+Ca2++OH-==CaCO3↓+H2O
B. 向沸水中滴加饱和FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O(沸水)![]() Fe(OH)3(胶体)+3H+
Fe(OH)3(胶体)+3H+
C. 二氧化碳通入足量的氢氧化钠溶液:CO2 + OH-═ HCO3-
D. 氧化钠与盐酸反应:O2-+2H+ ==== H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,实验测得1.0mol/L NH4HCO3 溶液pH=8.0。平衡时碳的分布系数(各含碳微粒的浓度占含碳各种微粒浓度之和的分数)与pH的关系如图所示。下列说法正确的是( )
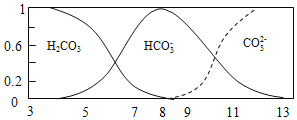
A. 常温下,Kb(NH3H2O)>Ka1(H2CO3)>Ka2(H2CO3)
B. pH=13时,溶液中不存在HCO3-的水解平衡
C. pH由8~11 时,随着pH值的增大,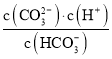 增大
增大
D. pH=3时,有c(NH4+)+c(NH3H2O)=c(HCO3-)+c(H2CO3)+c(CO32-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z为元素周期表中的主族元素,且原子序数均不大于20,W的原子序数最大,X位于第二周期且原子的最外层电子数是内层电子数的3倍,Y的单质在空气中易形成一层致密氧化膜,且Y原子的最外层电子数为奇数,Z与Y同周期且相邻,W、Y原子的最外层电子数之和等于Z原子的最外层电子数。下列说法正确的是( )
A. 最简单离子的半径:Y>W>X
B. 气态氢化物的稳定性:X>Z
C. 最高价氧化物对应水化物的碱性:Y>W
D. Y、Z的氧化物均不能溶解于水中,且均为碱性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pC类似于pH,是指极稀溶液中的溶质浓度的常用对数的负值。如某溶液中某溶质的浓度为1×10-3mol·L-1,则该溶液中该溶质的pC=-lg(1×10-3) = 3。下图为25℃时H2CO3溶液的pC-pH图(若离子浓度小于10-5 mol·L-1,可认为该离子不存在)。下列说法错误的是

A. 向Na2CO3溶液中滴加盐酸至pH等于11时,溶液中:c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(HCO3-)+c(Cl-)
B. 25℃时,H2CO3的一级电离平衡常数Ka1= 10-6
C. 25℃时,CO2饱和溶液的浓度是0.05 mol·L-1,其中1/5的CO2转变为H2CO3,若此时溶液的pH 约为5,据此可得该温度下CO2饱和溶液中H2CO3的电离度约为1%
D. 25℃时,0.1 mol·L-1,的Na2CO3和0.1 mol·L-1的NaHCO3混合溶液中离子浓度的大小为c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示两个常见固氮反应的平衡常数对数值(lgK)与温度的关系:①N2+3H22NH3;②N2+O22NO。根据图中的数据判断下列说法正确的是

A.升温,反应①的速率减小反应②的速率增大
B.反应①是放热反应
C.可以在常温下利用反应①进行工业固氮
D.曲线的交点表示反应①和反应②体系中 N2 的转化率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:2NO2(g) ![]() 2NO(g)+O2(g)在体积固定的密闭容器中进行,达到平衡状态的标志的是( )
2NO(g)+O2(g)在体积固定的密闭容器中进行,达到平衡状态的标志的是( )
①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO
③用NO2、NO、O2表示的反应速率的比为2∶2∶1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的平均相对分子质量不再改变的状态
A.①③⑥⑦B.①④⑥⑦C.②③④⑦D.①②④⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com