
| ��� |
| �ŵ� |
| A�����ʱ��������Ӧ����ԭ��Ӧ����6C+xLi++xe-�TLixC6 |
| B���ŵ�ʱ��������Ӧ����ԭ��Ӧ��Li1-xCoO2+xLi++xe-�TLiCoO2 |
| C�����ʱ����صĸ������Դ�ĸ������� |
| D���ŵ�ʱ��Li+���ƶ� |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
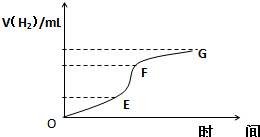 �� I���ô�����п����100mL2mol/Lϡ���ᷴӦ��ȡ��������ش�
�� I���ô�����п����100mL2mol/Lϡ���ᷴӦ��ȡ��������ش�| ���� |
| 500�� |
| SO2 | O2 | SO3 | |
| ��Ӧ��ʼʱ��Ũ��/mol?L-1 | 3.0 | 1.5 | 0 |
| 10min���Ũ��/mol?L-1 | |||
| ƽ����Ӧ����/mol?L-1?min-1 | 0.1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��AԪ��λ��Ԫ�����ڱ��еڶ����ڢ�A�� |
| B��B������C���Ӿ�����ͬ�ĵ��Ӳ�ṹ |
| C��C���Ӿ��к�ǿ�Ļ�ԭ�ԣ�B���Ӿ��к�ǿ�������� |
| D��B��C�����γ�BC2�ͻ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������11.2 L�ļ������庬�м��������Ϊ0.5 NA�� |
| B��14g��ϩ�ͱ�ϩ�Ļ��������ԭ����Ϊ3 NA�� |
| C��0.1 mol/L������������Һ�к���������Ϊ0.1 NA�� |
| D��5.6 g����������ϡ���ᷴӦʧȥ������Ϊ0.3 NA�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Na2CO3��Һ��NaHSO4��Һ��Ӧ��CO32-+2H+=H2O+CO2�� |
| B�����������Һ�м�������������Һ��Ba2+SO42-=BaSO4�� |
| C��Fe3O4��ϡ���ᷴӦ��Fe3O4+8H+=2Fe3++Fe2++4H2O |
| D�����������Ƽӵ���ˮ�У�Na+2H2O=Na++OH-+H2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��NaHCO3 |
| B��Al��NO3��3 |
| C��Fe2��SO4��3 |
| D����NH4��2CO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������Ͷ��FeSO4��Һ�У����Եõ������� |
| B������Cl2��S�ֱ�Ͷ��ݵ�������Na��Ӧ��ǰ�ߵõ����Ӷ� |
| C��Na2O��Na2O2���������ӵĸ����Ⱦ�Ϊ1��2 |
| D����2Na2O2+2H2O=4NaOH+O2��Ӧ�У�ÿ����1mol O2������2mol������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����״̬�£�33.6L�������к��з�ԭ�ӵ���ĿΪ1.5NA |
| B���ں���4mol Si-O����ʯӢ�����У���ԭ�ӵ���ĿΪ2NA�� |
| C��50mL18.4mol?L-1Ũ����������ͭ�ȷ�Ӧ������SO2���ӵ���ĿΪ0.46NA |
| D��ij�ܱ�����ʢ��0.1molN2��0.3molH2����һ�������³�ַ�Ӧ��ת�Ƶ��ӵ���ĿΪ0.6NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com