
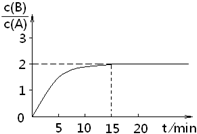
 已知,某温度下在2L密闭容器中加入一定量A,发生以下化学反应:
已知,某温度下在2L密闭容器中加入一定量A,发生以下化学反应:| A、该温度下此反应平衡常数为3.2 | B、A的初始物质的量为4 mol | C、反应到达平衡的过程中,放出的热量是154.4kJ | D、如使反应最终c(B)/c(A)=3,只能降低反应温度 |
| c(B) |
| c(A) |
| c(B)?c(C) |
| c2(A) |
| c(B) |
| c(A) |
| c(B) |
| c(A) |
| c(B)?c(C) |
| c2(A) |
| 1.6×1.6 |
| 0.82 |
| 6.4mol |
| 2 |
| c(B) |
| c(A) |


科目:高中化学 来源: 题型:阅读理解
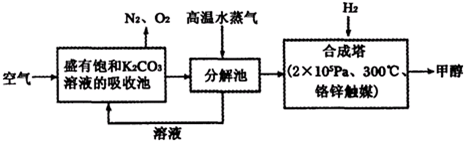
| 物质 | H2 | CO | CH3OH |
| 浓度/(mol?L-1) | 0.2 | 0.2 | 0.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
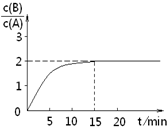 已知,某温度下在2L密闭容器中加入一定量A,发生以下化学反应:
已知,某温度下在2L密闭容器中加入一定量A,发生以下化学反应:| A、反应在前15min的平均速率ν(A)=0.11 mol?L-1?min-1 | B、A的初始物质的量为8 mol | C、反应到达平衡的过程中,放出的热量是77.2kJ | D、如使反应最终c(B)/c(A)=1.5,恒温恒容时,加入一定量的A可以实现 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年北京市房山区高三第二次模拟化学试卷(解析版) 题型:选择题
已知,某温度下在2L密闭容器中加入一定量A,发生以下化学反应:2A(g) 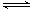 B(g)+C(g);ΔH =-48.25 kJ
· mol-1反应过程中时间t与A 、B浓度有下图所示关系,若测得第15min时c(B)=1.6 mol·L-1,则下列结论正确的是
B(g)+C(g);ΔH =-48.25 kJ
· mol-1反应过程中时间t与A 、B浓度有下图所示关系,若测得第15min时c(B)=1.6 mol·L-1,则下列结论正确的是

A.该温度下此反应平衡常数为3.2
B.A的初始物质的量为4 mol
C.反应到达平衡的过程中,放出的热量是154.4kJ
D.如使反应最终c(B)/c(A)=3,只能降低反应温度
查看答案和解析>>
科目:高中化学 来源: 题型:
已知合成氨反应N2(g)+3H2(g)![]() 2NH3(g)△H=-92.30kJ ·mol-1,在某温度下,2L的密闭容器中进行,测得如下数据:
2NH3(g)△H=-92.30kJ ·mol-1,在某温度下,2L的密闭容器中进行,测得如下数据:

下列说法正确的是
A.反应进行到1小时时放出的热量为9.23kJ
B.反应3h内,反应速率v(N2)为0.17mol·L-1·h-1
C.此温度下,该反应的平衡常数为0.037
D.4h时,若再加入1mol N2,达到新的平衡时,N2的转化率是原来的两倍
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com